1 . 钒是人体不可缺少的元素,Heyliger 等首次报道了偏钒酸钠显著降低糖尿病大鼠血糖的作用后,钒化学的研究得到了很大发展。钒及其化合物也广泛应用于特种钢、催化剂、颜料、染料、电子材料及防腐剂等等领域。
(1)钒酸盐与磷酸盐结构相似。请画出VO 、H2VO
、H2VO 、VO2(H2O)
、VO2(H2O)  和V2O
和V2O 的空间构型
的空间构型__________ 。
(2)生理条件下的钒以多种氧化态存在,各种氧化态可以相互转化。通常细胞外的钒是V(V), 。而细胞内的钒是V(IV)。研究表明,钒酸二氢根离子可与亚铁血红素(Mtrc-Fe2+)反应,写出该反应的离子方程式__________ 。
(3)①已知配合物[VON(CH2COO)3]在水溶液中的几何构型是唯一 的,画出它的空间构型图__________ 。
②理论推测上述配合物分子在晶体中是有手性的,指出产生手性的原因__________ 。
(4)钒酸钇晶体是近年来新开发出的优良双折射光学晶体,在光电产业中得到广泛应用。可以在弱碱性溶液中用偏钒酸铵和硝酸钇合成。写出以Y2O3与V2O5为主要原料合成钒酸钇的化学方程式__________ 。
(5)若以市售分析纯偏钒酸铵为原料制备高纯钒酸钇单晶,需将杂质铁离子含量降至一定数量级。设每升偏钒酸铵溶液中含三价铁离子为5.0 ×10-5 mol,用0.01 mol dm-3的鏊合剂除铁。
①说明不采取使铁离子水解析出沉淀的方法除铁的理由__________ 。
②通过计算说明如何选择螯合剂使偏钒酸铵含铁量降至10-30moldm-3以下__________ 。
(1)钒酸盐与磷酸盐结构相似。请画出VO
 、H2VO
、H2VO 、VO2(H2O)
、VO2(H2O)  和V2O
和V2O 的空间构型
的空间构型(2)生理条件下的钒以多种氧化态存在,各种氧化态可以相互转化。通常细胞外的钒是V(V), 。而细胞内的钒是V(IV)。研究表明,钒酸二氢根离子可与亚铁血红素(Mtrc-Fe2+)反应,写出该反应的离子方程式
(3)①已知配合物[VON(CH2COO)3]在水溶液中的几何构型是唯一 的,画出它的空间构型图
②理论推测上述配合物分子在晶体中是有手性的,指出产生手性的原因
(4)钒酸钇晶体是近年来新开发出的优良双折射光学晶体,在光电产业中得到广泛应用。可以在弱碱性溶液中用偏钒酸铵和硝酸钇合成。写出以Y2O3与V2O5为主要原料合成钒酸钇的化学方程式
(5)若以市售分析纯偏钒酸铵为原料制备高纯钒酸钇单晶,需将杂质铁离子含量降至一定数量级。设每升偏钒酸铵溶液中含三价铁离子为5.0 ×10-5 mol,用0.01 mol dm-3的鏊合剂除铁。
①说明不采取使铁离子水解析出沉淀的方法除铁的理由
②通过计算说明如何选择螯合剂使偏钒酸铵含铁量降至10-30moldm-3以下
| 配离子 |  |
| [Fe(edta)]2- [Fe(edta)]- [Fe(phen)3]2+ [Fe(phen)3]3+ | 2.1×1014 1.7×1024 2.0×1021 1.3×1014 |
| 沉淀 | Ksp |
| Fe(OH)2 Fe(OH)3 | 8.0×10-16 4.0×10-38 |
您最近一年使用:0次
2 . 甲醛亦称“蚁醛”。含甲醛37%~40%、甲醇8%的水溶液俗称“福尔马林”。甲醛是重要的有机合成原料,大量用于生产树脂、合成纤维、药物、涂料以及用于房屋、家具和种子的消毒等。利用下表所给数据回答问题(设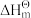 和
和 均不随温度而变化)。
均不随温度而变化)。
一些物质的热力学数据(298.15K)
(1)甲醇脱氢是制甲醛最简单的工业方法:CH3OH(g)=HCHO(g)+H2(g)。甲醇氧化是制甲醛的另一种工业方法,即甲醇蒸气和一定量的空气通过Ag催化剂层,甲醇即被氧化得到甲醛:CH3OH(g)+ O2(g)=HCHO(g)+H2O(g)。试通过简单的热力学分析,对298.15K时的上述2种方法作出评价
O2(g)=HCHO(g)+H2O(g)。试通过简单的热力学分析,对298.15K时的上述2种方法作出评价_______ 。
(2)实际上,甲醇氧化制甲醛的反应,是甲醇脱氢反应和氢氧化合反应的结合。试通过计算分析两反应结合对制甲醛的实际意义_______ 。
(3)下图是甲醇制甲醛有关反应的lgK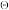 随温度T的变化。试指出图中曲线(1)、(2)、(3)分别对应哪个化学反应
随温度T的变化。试指出图中曲线(1)、(2)、(3)分别对应哪个化学反应_______ 、_______ 、_______ ?为什么_______ ?
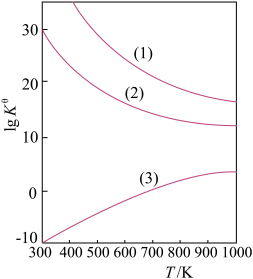
有关反应有:
CH3OH(g)=HCHO(g)+H2(g)
CH3OH(g)+ O2(g)=HCHO(g)+H2O(g)
O2(g)=HCHO(g)+H2O(g)
和在氧化法中不可避免的深度氧化反应:HCHO(g)+ O2(g)=CO(g)+H2O(g)
O2(g)=CO(g)+H2O(g)
(4)氧化法制甲醛时,温度为550℃、总压为101325Pa的甲醇与空气混合物通过银催化剂,银逐渐失去光泽并且碎裂。试通过计算判断上述现象是否由于Ag氧化成Ag2O(s)所致_______ 。
(5)以CO和H2为原料可以合成甲醇。500℃和25MPa时,CO和H2的体积比为1:2的合成气,在催化剂ZnO-Cr2O3-Al2O3存在下,发生如下两平行反应①和②:
CO+2H2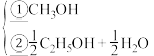
试计算平衡产物CH3OH和C2H5OH的摩尔分数之比_______ 。
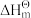 和
和 均不随温度而变化)。
均不随温度而变化)。一些物质的热力学数据(298.15K)
| 物质 |  /kJ·mol-1 /kJ·mol-1 |  /J·K·mol-1 /J·K·mol-1 |
| C2H5OH(g) H3OH(g) HCHO(g) H2O(g) CO(g) Ag2O(s) Ag(s) H2(g) O2(g) | -235.10 -200.66 -108.57 -241.818 -110.525 -31.05 0 0 0 | 282.70 239.81 218.77 188.825 197.674 121.3 42.55 130.684 205.138 |
(1)甲醇脱氢是制甲醛最简单的工业方法:CH3OH(g)=HCHO(g)+H2(g)。甲醇氧化是制甲醛的另一种工业方法,即甲醇蒸气和一定量的空气通过Ag催化剂层,甲醇即被氧化得到甲醛:CH3OH(g)+
 O2(g)=HCHO(g)+H2O(g)。试通过简单的热力学分析,对298.15K时的上述2种方法作出评价
O2(g)=HCHO(g)+H2O(g)。试通过简单的热力学分析,对298.15K时的上述2种方法作出评价(2)实际上,甲醇氧化制甲醛的反应,是甲醇脱氢反应和氢氧化合反应的结合。试通过计算分析两反应结合对制甲醛的实际意义
(3)下图是甲醇制甲醛有关反应的lgK
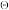 随温度T的变化。试指出图中曲线(1)、(2)、(3)分别对应哪个化学反应
随温度T的变化。试指出图中曲线(1)、(2)、(3)分别对应哪个化学反应
有关反应有:
CH3OH(g)=HCHO(g)+H2(g)
CH3OH(g)+
 O2(g)=HCHO(g)+H2O(g)
O2(g)=HCHO(g)+H2O(g)和在氧化法中不可避免的深度氧化反应:HCHO(g)+
 O2(g)=CO(g)+H2O(g)
O2(g)=CO(g)+H2O(g)(4)氧化法制甲醛时,温度为550℃、总压为101325Pa的甲醇与空气混合物通过银催化剂,银逐渐失去光泽并且碎裂。试通过计算判断上述现象是否由于Ag氧化成Ag2O(s)所致
(5)以CO和H2为原料可以合成甲醇。500℃和25MPa时,CO和H2的体积比为1:2的合成气,在催化剂ZnO-Cr2O3-Al2O3存在下,发生如下两平行反应①和②:
CO+2H2
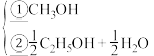
试计算平衡产物CH3OH和C2H5OH的摩尔分数之比
您最近一年使用:0次



