名校
1 . N2CO分子呈链状结构,最稳定Lewis结构式中形式电荷为0的N原子数为x,采用sp2杂化的N原子数为y,则x、y分别为
| A.1,2 | B.4,1.2 | C.2,2 | D.2,1 |
您最近一年使用:0次
名校
解题方法
2 . 硫酸与Cl2反应的生成物的结构如图所示。有关说法不正确的是
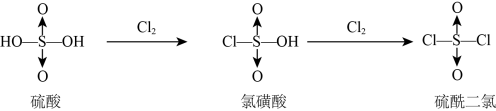
| A.氯磺酸钠NaSO3Cl与水反应:NaSO3Cl+H2O=Na++OH-+HSO3Cl- |
B.硫酰二氯与水反应的离子方程式:SO2Cl2+6H2O=4H3O++ +2Cl- +2Cl- |
| C.氯磺酸与BaCl2溶液反应的化学方程式:HSO3Cl+BaCl2+H2O=BaSO4↓+3HCl |
| D.硫酰二氯可脱去金属氯化物中的水:MgCl2·6H2O+3SO2Cl2=MgCl2+3H2SO4+6HCl |
您最近一年使用:0次
名校
解题方法
3 . 吡啶( )是类似于苯的芳香化合物,2—乙烯基吡啶(VPy)是合成治疗矽肺病药物的原料,可由如下路线合成,下列叙述正确的是
)是类似于苯的芳香化合物,2—乙烯基吡啶(VPy)是合成治疗矽肺病药物的原料,可由如下路线合成,下列叙述正确的是
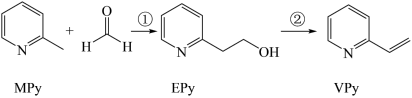
| A.Mpy只有两种芳香同分异构体 | B.反应①条件是碱性 |
| C.Vpy与苯乙烯是同分异构体 | D.反应①②都是消去反应 |
您最近一年使用:0次
4 . 金银花有效活性成分为绿原酸,又名咖啡鞣酸,具有广泛的杀菌消炎功效,结构如图所示,下列有关绿原酸的说法不正确的是
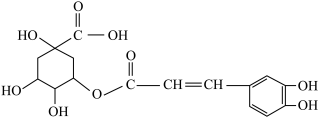
| A.绿原酸的分子式为C16H16O9 |
| B.1mol绿原酸最多与4molNaOH反应 |
| C.1个绿原酸分子中含有4个手性碳原子 |
| D.绿原酸分子能与1.3-丁二烯加热条件下进行D-A反应 |
您最近一年使用:0次
名校
5 . 下列化合物或离子中有芳香性的是
A.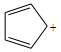 | B.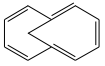 | C.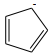 | D.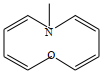 |
您最近一年使用:0次
名校
6 . 世博会中国馆建筑使用光伏并网发电,总功率达4兆瓦,是历届世博会之最,通过并网,使用半导体照明(LED)。已知发出白光的LED是由GaN芯片和钇铝石榴石(YAG,化学式:Y3Al5O12)芯片封装在一起做成的。下列有关叙述正确的是

| A.光伏电池是将太阳能直接转变为电能 |
| B.N型半导体以电子导电为主,P型半导体以空穴导电为主 |
| C.电流从a流向b,Р型半导体为负极 |
| D.LED中的Ga和Y都显+3价 |
您最近一年使用:0次
名校
7 . 化合物[Cu(PydC)(amp)]·3H2O的组成为C14H14CuN4O7.热重分析曲线表明,该化合物受热分解发生两步失重:第一个失重峰在200-250°C,失重的质量分数为15.2%;第二个失重峰在400-500°C,失重后的固态残渣质量为原化合物质量的20.0%。PydC和amp是含有芳环的有机配体。经过计算,判断第二步失重后的固体残渣应含有
| A.Cu2O | B.CuO | C.Cu2C2 | D.CuH |
您最近一年使用:0次
名校
8 . 在恒温恒容的密闭容器中,发生反应3A(g)+B(g)⇌xC(g)。
I.将3molA和2moB在一定条件下反应,达平衡时C的体积分数为a;
II.若起始时A、B、C投入的物质的量分别为nA、nB、nC,平衡时C的体积分数也为a
下列说法正确的是
I.将3molA和2moB在一定条件下反应,达平衡时C的体积分数为a;
II.若起始时A、B、C投入的物质的量分别为nA、nB、nC,平衡时C的体积分数也为a
下列说法正确的是
| A.若I达平衡时,A、B、C各增加1mol,则B的转化率将一定增大 |
| B.若向I平衡体系中再加入3molA和2molB,C的体积分数若大于a,可断定x<4 |
| C.若x=2,则II体系起始物质的量应当满足3nB=nA+3 |
| D.若II体系起始物质的量满足3nC+8nA=12nB时,可判断x=4 |
您最近一年使用:0次
名校
解题方法
9 . 韩国首尔大学的科学家将水置于一个足够强的电场中,在20℃时,水分子瞬间凝固形成“暖冰”。下列关于“暖冰”的说法正确的是
| A.暖冰中水分子对称性由C2轴变为C∞ |
| B.在电场作用下,水分子间更易形成氢键,因而可以制得“暖冰” |
| C.暖冰中水分子的氧原子的杂化方式为sp3,氢键键能可达到250kJ/mol |
| D.水凝固形成20℃时的“暖冰”氢键键长有变化 |
您最近一年使用:0次
名校
10 . 已知HClO的Ka=2.98×10-8,HN3的Ka=1.7×10-5,下列有关说法正确的是
| A.温度一定时在pH=3的叠氮酸中加入少量0.001mol/L的稀盐酸,溶液的pH不会改变 |
| B.等浓度等体积的NaClO和溶液NaN3前者所含离子总数比后者小 |
| C.100mL pH=2的新制氯水中:n(OH-)+n(ClO-)+n(HClO)=0.001mol |
| D.将Cl2通入NaOH溶液中,若溶液呈中性,则溶液中存在4种微粒 |
您最近一年使用:0次



