1 . 硫代硫酸钠(Na2S2O3·5H2O)的俗名是大苏打,在化学实验中有广泛应用。
(1)实验室可通过向含Na2S和Na2CO3的溶液中通入SO2来制备Na2S2O3(其简单流程如图所示)。

①写出制备Na2S2O3的化学方程式:____ 。
②“一系列操作”包括____ 、____ 、过滤、洗涤、干燥。(填操作名称)
(2)工业上,常用Na2S2O3溶液吸收尾气中的Cl2,氧化产物为SO 。写出发生反应的离子方程式:
。写出发生反应的离子方程式:____ 。
(3)临床上,Na2S2O3可用于氰化物解毒,解毒原理:S2O +CN-=SCN-+SO
+CN-=SCN-+SO 。检验该转化生成了SCN-的操作为
。检验该转化生成了SCN-的操作为____ 。
(4)探究Na2S2O3和稀硫酸反应速率与浓度、温度关系的实验方案如表:
已知:Na2S2O3+H2SO4=S↓+SO2↑+Na2SO4+H2O。
变浑浊时间最短的实验是____ (填实验编号)。
(5)工业上,测定V2O5样品纯度的方法:取wg样品溶于稀硫酸,加入足量KI溶液,再加入cmol·L-1的Na2S2O3溶液至恰好完全反应,消耗Na2S2O3溶液VmL。
相关反应:V2O5+2KI+3H2SO4=2VOSO4+I2+K2SO4+3H2O;I2+2Na2S2O3=2NaI+Na2S4O6。
①该样品中V2O5的质量分数为____ (假设杂质不参与反应)。
②如果稀硫酸过多,测得结果会____ (填“偏高”、“偏低”或“无影响”)。
(1)实验室可通过向含Na2S和Na2CO3的溶液中通入SO2来制备Na2S2O3(其简单流程如图所示)。

①写出制备Na2S2O3的化学方程式:
②“一系列操作”包括
(2)工业上,常用Na2S2O3溶液吸收尾气中的Cl2,氧化产物为SO
 。写出发生反应的离子方程式:
。写出发生反应的离子方程式:(3)临床上,Na2S2O3可用于氰化物解毒,解毒原理:S2O
 +CN-=SCN-+SO
+CN-=SCN-+SO 。检验该转化生成了SCN-的操作为
。检验该转化生成了SCN-的操作为(4)探究Na2S2O3和稀硫酸反应速率与浓度、温度关系的实验方案如表:
| 实验编号 | 0.1mol·L-1Na2S2O3溶液的体积/mL | 蒸馏水的体积/mL | 0.1mol·L-1稀硫酸的体积/mL | 温度/℃ | 变浑浊时间/s |
| ① | 10 | 0 | 10 | 25 | a |
| ② | 10 | 0 | 10 | 35 | b |
| ③ | 5 | 5 | 10 | 35 | c |
变浑浊时间最短的实验是
(5)工业上,测定V2O5样品纯度的方法:取wg样品溶于稀硫酸,加入足量KI溶液,再加入cmol·L-1的Na2S2O3溶液至恰好完全反应,消耗Na2S2O3溶液VmL。
相关反应:V2O5+2KI+3H2SO4=2VOSO4+I2+K2SO4+3H2O;I2+2Na2S2O3=2NaI+Na2S4O6。
①该样品中V2O5的质量分数为
②如果稀硫酸过多,测得结果会
您最近一年使用:0次
2022-05-03更新
|
418次组卷
|
4卷引用:江西省重点2021-2022学年高一下学期5月联考化学试题
解题方法
2 . I.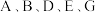 为原子序数依次增大的五种短周期主族元素,非金属元素A最外层电子数与其周期数相同,B原子的最外层电子数是其所在周期数的2倍。B单质在D单质中充分燃烧能生成其最高价化合物
为原子序数依次增大的五种短周期主族元素,非金属元素A最外层电子数与其周期数相同,B原子的最外层电子数是其所在周期数的2倍。B单质在D单质中充分燃烧能生成其最高价化合物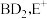 与
与 具有相同的电子层结构。A单质在G单质中燃烧,产物溶于水得到一种强酸。回答下列问题:
具有相同的电子层结构。A单质在G单质中燃烧,产物溶于水得到一种强酸。回答下列问题:
(1)G在元素周期表中的位置是_______ 。
(2)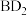 的电子式为
的电子式为_______ ;
(3) 分别形成的简单离子的半径由大到小的顺序为
分别形成的简单离子的半径由大到小的顺序为_______ (用离子符号表示);
(4)由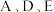 三种元素组成的化合物含有的化学键类型为
三种元素组成的化合物含有的化学键类型为_______ ;
(5)设计一个简单的实验证明G和B的非金属性强弱:_______ (用化学方程式表示)。
Ⅱ、人体血液里 的浓度一般采用
的浓度一般采用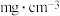 来表示。抽取一定体积的血样,加适量的草酸铵
来表示。抽取一定体积的血样,加适量的草酸铵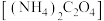 溶液,可析出草酸钙
溶液,可析出草酸钙 沉淀:
沉淀: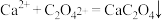 。将此草酸钙沉淀洗涤后溶于强酸可得草酸
。将此草酸钙沉淀洗涤后溶于强酸可得草酸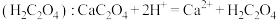 ,再用酸性
,再用酸性 溶液滴定即可测定血液样品中
溶液滴定即可测定血液样品中 的浓度。取血液样品
的浓度。取血液样品 ,经过上述处理后得到草酸,再加入
,经过上述处理后得到草酸,再加入 酸性
酸性 溶液滴定使草酸全部转化成
溶液滴定使草酸全部转化成 逸出,这时共消耗
逸出,这时共消耗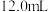 酸性
酸性 溶液。已知草酸与酸性
溶液。已知草酸与酸性 溶液反应的离子方程式为:
溶液反应的离子方程式为: (未配平)
(未配平)
(6)请将该离子方程式配平:_______ 。


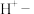



(7)经过计算,血液样品中 的浓度为
的浓度为_______ 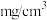 。
。
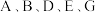 为原子序数依次增大的五种短周期主族元素,非金属元素A最外层电子数与其周期数相同,B原子的最外层电子数是其所在周期数的2倍。B单质在D单质中充分燃烧能生成其最高价化合物
为原子序数依次增大的五种短周期主族元素,非金属元素A最外层电子数与其周期数相同,B原子的最外层电子数是其所在周期数的2倍。B单质在D单质中充分燃烧能生成其最高价化合物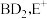 与
与 具有相同的电子层结构。A单质在G单质中燃烧,产物溶于水得到一种强酸。回答下列问题:
具有相同的电子层结构。A单质在G单质中燃烧,产物溶于水得到一种强酸。回答下列问题:(1)G在元素周期表中的位置是
(2)
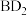 的电子式为
的电子式为(3)
 分别形成的简单离子的半径由大到小的顺序为
分别形成的简单离子的半径由大到小的顺序为(4)由
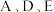 三种元素组成的化合物含有的化学键类型为
三种元素组成的化合物含有的化学键类型为(5)设计一个简单的实验证明G和B的非金属性强弱:
Ⅱ、人体血液里
 的浓度一般采用
的浓度一般采用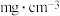 来表示。抽取一定体积的血样,加适量的草酸铵
来表示。抽取一定体积的血样,加适量的草酸铵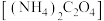 溶液,可析出草酸钙
溶液,可析出草酸钙 沉淀:
沉淀: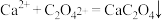 。将此草酸钙沉淀洗涤后溶于强酸可得草酸
。将此草酸钙沉淀洗涤后溶于强酸可得草酸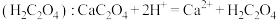 ,再用酸性
,再用酸性 溶液滴定即可测定血液样品中
溶液滴定即可测定血液样品中 的浓度。取血液样品
的浓度。取血液样品 ,经过上述处理后得到草酸,再加入
,经过上述处理后得到草酸,再加入 酸性
酸性 溶液滴定使草酸全部转化成
溶液滴定使草酸全部转化成 逸出,这时共消耗
逸出,这时共消耗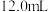 酸性
酸性 溶液。已知草酸与酸性
溶液。已知草酸与酸性 溶液反应的离子方程式为:
溶液反应的离子方程式为: (未配平)
(未配平)(6)请将该离子方程式配平:


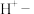



(7)经过计算,血液样品中
 的浓度为
的浓度为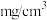 。
。
您最近一年使用:0次
2022-01-22更新
|
131次组卷
|
2卷引用:江西省新余市2021-2022学年高一上学期期末考试化学试题



