1 . 下列离子方程式书写错误的是
A.过氧化钠溶于硫酸铜溶液中: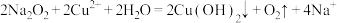 |
B.向 溶液中通入少量 溶液中通入少量 气体: 气体: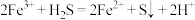 |
C.向碳酸氢钠溶液中滴加盐酸: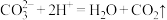 |
D.向次氯酸钠溶液中通入少量 : :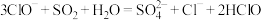 |
您最近一年使用:0次
2 . “吹出法”提溴工艺流程示意图如下:不正确 的是
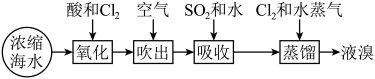
A.“氧化”过程中Cl2使 转化为Br2 转化为Br2 |
| B.“吹出”过程中利用了Br2的挥发性 |
C.“吸收”过程中化学方程式: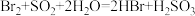 |
| D.“蒸馏”的目的是得到液溴 |
您最近一年使用:0次
3 . 下列化学用语不正确 的是
A.硫酸铝的电离方程式: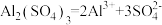 |
B.碳酸氢钠受热分解的化学方程式: 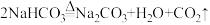 |
C.用电子式表示氯化钠的形成过程: 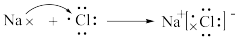 |
D.碳酸钙与盐酸反应的离子方程式: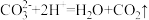 |
您最近一年使用:0次
解题方法
4 . 请回答:
(1)①氧化铝的化学式_______ ,②氯气的电子式是_______ 。
(2)向FeCl3溶液中滴加NaOH,产生_______ 色沉淀。
(3)浓硝酸见光分解的化学方程式是_______ 。
(1)①氧化铝的化学式
(2)向FeCl3溶液中滴加NaOH,产生
(3)浓硝酸见光分解的化学方程式是
您最近一年使用:0次
解题方法
5 . 制作豆腐过程一般有如图步操作,其中操作⑤CaSO4或MgCl2作凝固剂根据图示,下列说法不正确的是

| A.操作①与操作②的目的是为了更多的蛋白质溶解于水 |
| B.操作③属于固液分离,取其袋子内的固体作为操作④的原料 |
| C.在适宜温度下,操作⑤用MgCl2,作凝固剂可使蛋白质沉淀 |
| D.操作⑥使豆腐“成形”,此过程主要发生的是物理变化 |
您最近一年使用:0次
解题方法
6 . 下列反应的离子方程式书写正确的是
A. 与足量NaOH溶液: 与足量NaOH溶液: |
B. 溶液与 溶液与 溶液: 溶液: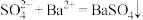 |
C. 与浓盐酸: 与浓盐酸: |
D. 与NaOH溶液: 与NaOH溶液: |
您最近一年使用:0次
名校
7 .  为阿伏加德罗常数的值。下列叙述错误的是
为阿伏加德罗常数的值。下列叙述错误的是
 为阿伏加德罗常数的值。下列叙述错误的是
为阿伏加德罗常数的值。下列叙述错误的是A.1mol 中 中 键的个数为 键的个数为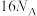 |
B.46g 中 中 杂化的碳原子数为 杂化的碳原子数为 |
C.1L 的HCN溶液中, 的HCN溶液中,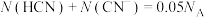 |
D.1mol 晶体中含有 晶体中含有 共价键 共价键 |
您最近一年使用:0次
解题方法
8 . 以石英砂(主要成分为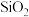 )为原料,经三步反应制得高纯硅,其中第一步反应的化学方程式如下。
)为原料,经三步反应制得高纯硅,其中第一步反应的化学方程式如下。
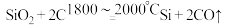
(1)作还原剂的物质是_______ ,碳元素的化合价_______ (填“升高”或“降低”)。
(2)若反应中消耗了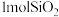 ,则生成
,则生成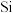 的物质的量为
的物质的量为_______  ,转移电子的物质的量为
,转移电子的物质的量为_______  。
。
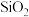 )为原料,经三步反应制得高纯硅,其中第一步反应的化学方程式如下。
)为原料,经三步反应制得高纯硅,其中第一步反应的化学方程式如下。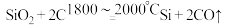
(1)作还原剂的物质是
(2)若反应中消耗了
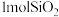 ,则生成
,则生成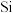 的物质的量为
的物质的量为 ,转移电子的物质的量为
,转移电子的物质的量为 。
。
您最近一年使用:0次
9 . 氯化钠(NaCl)是生活中常用的化学品,也是重要的化工生产原料。
Ⅰ.实验室研究氯化钠的性质及制备
(1)下图表示NaCl在水中溶解过程的微观状态示意图。___________ 。
a.干燥的NaCl固体不导电,是由于其中不存在Na+和Cl-
b.由上图可知,水分子在形成自由移动的Na+和Cl-中起到了至关重要的作用
c.NaCl溶液能导电,是由于在电流作用下,其可解离出自由移动的Na+和Cl-
(2)某同学用含钠元素的不同类别物质制备NaCl。化学反应方程式如下:
a.2Na + Cl2 2NaCl
2NaCl
b.NaOH + HCl = NaCl + H2O
c.Na2O + 2HCl = 2NaCl + H2O
d.___________。
① 反应d可为某物质与HCl反应来制得氯化钠,该物质的化学式为___________ 。
② 反应d也可为两种盐溶液相互反应获得氯化钠,该反应的化学方程式为___________ 。
③ 反应c中的原料Na2O的物质类别是碱性氧化物,请依据其类别通性,再列举2个能与Na2O反应的其他物质(用化学式表示)___________ 。
Ⅱ.工业生产中氯化钠的制备
我国食盐的来源主要为海盐、湖盐、井矿盐。粗食盐中除了含泥沙等难溶性杂质外,还含有Ca2+、Mg2+、SO 等可溶性杂质。为得到精制食盐,某同学设计如下除杂流程,向粗盐中依次加入:过量BaCl2溶液、过量Na2CO3溶液、过量NaOH溶液,然后过滤,再在滤液中加入适量盐酸后加热蒸发结晶得纯净的NaCl。
等可溶性杂质。为得到精制食盐,某同学设计如下除杂流程,向粗盐中依次加入:过量BaCl2溶液、过量Na2CO3溶液、过量NaOH溶液,然后过滤,再在滤液中加入适量盐酸后加热蒸发结晶得纯净的NaCl。
(3)①过滤操作中所用到的玻璃仪器有烧杯、漏斗和___________ 。
②用离子方程式表示加入过量Na2CO3溶液的作用Ca2++CO =CaCO3↓和
=CaCO3↓和___________ 。
③ 用离子方程式表示盐酸的作用H+ + OH-=H2O 和___________ 。
Ⅰ.实验室研究氯化钠的性质及制备
(1)下图表示NaCl在水中溶解过程的微观状态示意图。

a.干燥的NaCl固体不导电,是由于其中不存在Na+和Cl-
b.由上图可知,水分子在形成自由移动的Na+和Cl-中起到了至关重要的作用
c.NaCl溶液能导电,是由于在电流作用下,其可解离出自由移动的Na+和Cl-
(2)某同学用含钠元素的不同类别物质制备NaCl。化学反应方程式如下:
a.2Na + Cl2
 2NaCl
2NaCl b.NaOH + HCl = NaCl + H2O
c.Na2O + 2HCl = 2NaCl + H2O
d.___________。
① 反应d可为某物质与HCl反应来制得氯化钠,该物质的化学式为
② 反应d也可为两种盐溶液相互反应获得氯化钠,该反应的化学方程式为
③ 反应c中的原料Na2O的物质类别是碱性氧化物,请依据其类别通性,再列举2个能与Na2O反应的其他物质(用化学式表示)
Ⅱ.工业生产中氯化钠的制备
我国食盐的来源主要为海盐、湖盐、井矿盐。粗食盐中除了含泥沙等难溶性杂质外,还含有Ca2+、Mg2+、SO
 等可溶性杂质。为得到精制食盐,某同学设计如下除杂流程,向粗盐中依次加入:过量BaCl2溶液、过量Na2CO3溶液、过量NaOH溶液,然后过滤,再在滤液中加入适量盐酸后加热蒸发结晶得纯净的NaCl。
等可溶性杂质。为得到精制食盐,某同学设计如下除杂流程,向粗盐中依次加入:过量BaCl2溶液、过量Na2CO3溶液、过量NaOH溶液,然后过滤,再在滤液中加入适量盐酸后加热蒸发结晶得纯净的NaCl。(3)①过滤操作中所用到的玻璃仪器有烧杯、漏斗和
②用离子方程式表示加入过量Na2CO3溶液的作用Ca2++CO
 =CaCO3↓和
=CaCO3↓和③ 用离子方程式表示盐酸的作用H+ + OH-=H2O 和
您最近一年使用:0次
解题方法
10 . 食品包装中的铁系脱氧剂由还原铁粉、氯化钠和炭粉等组成,利用铁的吸氧腐蚀除去氧气,主要反应有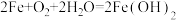 ,
,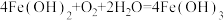 。已知某脱氧剂中含有2.24g还原铁粉,请计算:
。已知某脱氧剂中含有2.24g还原铁粉,请计算:
(1)还原铁粉的物质的量是_______ mol。
(2)若还原铁粉完全转化为Fe(OH)3,则转移电子的物质的量是_______ mol。
(3)在25 和101kPa的条作下,气体摩尔体积约为24.5L/mol,空气中氧气的体积分数约为21%,则该脱氧剂理论上最多能处理
和101kPa的条作下,气体摩尔体积约为24.5L/mol,空气中氧气的体积分数约为21%,则该脱氧剂理论上最多能处理_______ mL包装盒中的空气。
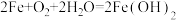 ,
,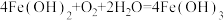 。已知某脱氧剂中含有2.24g还原铁粉,请计算:
。已知某脱氧剂中含有2.24g还原铁粉,请计算:(1)还原铁粉的物质的量是
(2)若还原铁粉完全转化为Fe(OH)3,则转移电子的物质的量是
(3)在25
 和101kPa的条作下,气体摩尔体积约为24.5L/mol,空气中氧气的体积分数约为21%,则该脱氧剂理论上最多能处理
和101kPa的条作下,气体摩尔体积约为24.5L/mol,空气中氧气的体积分数约为21%,则该脱氧剂理论上最多能处理
您最近一年使用:0次



