名校
解题方法
1 . “价-类”二维图是研究物质性质的常用工具,下图是铁元素的部分“价-类”二维图。回答下列问题:

(1) 是一种用途广泛的盐类物质。
是一种用途广泛的盐类物质。
①用煤埚钳夹住一束铁丝,灼烧后立即放入充满氯气的集气瓶中,观察到的现象是___________ ,发生反应的化学方程式为___________ 。
②实验室中制取 胶体的步骤依次为:a.用洁净的烧杯取少量蒸馏水;b.用酒精灯加热至沸腾;c.………;d.至液体呈透明的红褐色。其中步骤c是
胶体的步骤依次为:a.用洁净的烧杯取少量蒸馏水;b.用酒精灯加热至沸腾;c.………;d.至液体呈透明的红褐色。其中步骤c是___________ ,证明胶体制备成功的实验是___________ 。
(2)写出一个能生成 且属于氧化还原反应的化学方程式
且属于氧化还原反应的化学方程式___________ 。
(3)根据上述“价-类”二维图,判断 中Fe元素价态有
中Fe元素价态有___________ ,写出 与稀盐酸反应的离子方程式
与稀盐酸反应的离子方程式___________ 。

(1)
 是一种用途广泛的盐类物质。
是一种用途广泛的盐类物质。①用煤埚钳夹住一束铁丝,灼烧后立即放入充满氯气的集气瓶中,观察到的现象是
②实验室中制取
 胶体的步骤依次为:a.用洁净的烧杯取少量蒸馏水;b.用酒精灯加热至沸腾;c.………;d.至液体呈透明的红褐色。其中步骤c是
胶体的步骤依次为:a.用洁净的烧杯取少量蒸馏水;b.用酒精灯加热至沸腾;c.………;d.至液体呈透明的红褐色。其中步骤c是(2)写出一个能生成
 且属于氧化还原反应的化学方程式
且属于氧化还原反应的化学方程式(3)根据上述“价-类”二维图,判断
 中Fe元素价态有
中Fe元素价态有 与稀盐酸反应的离子方程式
与稀盐酸反应的离子方程式
您最近一年使用:0次
2 . 下列关于物质的性质与用途,说法正确的是
A.将饱和氯化铁加热即可制取 胶体 胶体 |
| B.二氧化氯有氧化性,可用作自来水消毒 |
| C.浓硫酸有强腐蚀性,工业生产中用浓硫酸刻蚀石英制成艺术品 |
| D.铁在潮湿的空气中能生成氧化铁,可以保护内层的金属,故铁制品不需要涂保护层 |
您最近一年使用:0次
名校
3 .  是一种常用的试剂。下列探究其用途的装置或操作能达到相应实验目的的是
是一种常用的试剂。下列探究其用途的装置或操作能达到相应实验目的的是

 是一种常用的试剂。下列探究其用途的装置或操作能达到相应实验目的的是
是一种常用的试剂。下列探究其用途的装置或操作能达到相应实验目的的是
A.用操作甲鉴别 溶液和 溶液和 溶液 溶液 |
B.用装置乙除去 气体中的 气体中的 |
C.用装置丙吸收多余的 |
D.用操作丁制备少量 固体 固体 |
您最近一年使用:0次
名校
4 . 下列物质用途或操作正确且与盐类水解有关的一组是
①用热饱和硫酸铵溶液清洗铁器表面的铁锈
②用 水溶液制备
水溶液制备
③用氯化铁溶液和氨水制备氢氧化铁胶体
④实验室通常使用热的纯碱溶液去除油污
⑤在氯化氢氛围中灼烧氯化镁晶体制备无水氯化镁
⑥配制 溶液时将
溶液时将 晶体溶于浓硝酸中并加蒸馏水稀释至指定浓度
晶体溶于浓硝酸中并加蒸馏水稀释至指定浓度
⑦刻蚀印刷电路板用氯化铁作腐蚀液
⑧用泡沫灭火器灭火
①用热饱和硫酸铵溶液清洗铁器表面的铁锈
②用
 水溶液制备
水溶液制备
③用氯化铁溶液和氨水制备氢氧化铁胶体
④实验室通常使用热的纯碱溶液去除油污
⑤在氯化氢氛围中灼烧氯化镁晶体制备无水氯化镁
⑥配制
 溶液时将
溶液时将 晶体溶于浓硝酸中并加蒸馏水稀释至指定浓度
晶体溶于浓硝酸中并加蒸馏水稀释至指定浓度⑦刻蚀印刷电路板用氯化铁作腐蚀液
⑧用泡沫灭火器灭火
| A.①②④⑤⑧ | B.③④⑤⑦⑧ | C.①②④⑤⑥ | D.②③④⑤⑥ |
您最近一年使用:0次
5 . 氯化铁FeCl3是一种化学常用试剂,在化学实验和工农业生产有着重要的用途。
(1)实验室常用饱和FeCl3溶液来制备Fe(OH)3胶体。
已知:常温25℃下FeCl3溶解度为90g/100g水。
实验I:配置20.0g饱和FeCl3溶液溶液。
①需要用到的仪器有:钥匙、托盘天平、玻璃棒、_______ 、_______ 、烧杯。
②该实验需称量FeCl3固体________ g。
实验II:制备Fe(OH)3胶体。
甲同学取一小烧杯,加入25mL蒸馏水,加热至沸腾,向沸水中逐滴加入l~2mL饱和氯化铁溶液,继续煮沸至透明的红褐色液体,停止加热。

③写出此过程中的化学方程式:_______ 。
④乙同学提议用自来水(自来水因用Cl2消毒常含有Cl-)代替蒸馏水,请回答乙同学的方案是否正确________ (若认为正确答“是”,若认为不正确答“否”并指出错误的原因)。
⑤除去氢氧化铁胶体中的氯化铁采用的方法是______ (填写字母)。
A.过滤B.渗析C.蒸发
(2)工业上制印刷电路板时常用FeCl3溶液做“腐蚀液”,原理为利用FeCl3溶液将Cu溶解。
高一化学学生兴趣小组根据此原理在覆铜板上制作“我爱化学”字样的图案。
实验III:利用覆铜板制作图案
①已知FeCl3与Cu反应生成Fe2+,请写出该反应的离子方程式:________ 。
②使用过的“腐蚀液”会失效,但还可以回收利用,其中有一步反应需要将Fe2+转化为Fe3+,下列试剂能实现上述变化的是_________ (填序号)。
A.氯气B.铁C.铜D.稀硫酸
(1)实验室常用饱和FeCl3溶液来制备Fe(OH)3胶体。
已知:常温25℃下FeCl3溶解度为90g/100g水。
实验I:配置20.0g饱和FeCl3溶液溶液。
①需要用到的仪器有:钥匙、托盘天平、玻璃棒、
②该实验需称量FeCl3固体
实验II:制备Fe(OH)3胶体。
甲同学取一小烧杯,加入25mL蒸馏水,加热至沸腾,向沸水中逐滴加入l~2mL饱和氯化铁溶液,继续煮沸至透明的红褐色液体,停止加热。

③写出此过程中的化学方程式:
④乙同学提议用自来水(自来水因用Cl2消毒常含有Cl-)代替蒸馏水,请回答乙同学的方案是否正确
⑤除去氢氧化铁胶体中的氯化铁采用的方法是
A.过滤B.渗析C.蒸发
(2)工业上制印刷电路板时常用FeCl3溶液做“腐蚀液”,原理为利用FeCl3溶液将Cu溶解。
高一化学学生兴趣小组根据此原理在覆铜板上制作“我爱化学”字样的图案。
实验III:利用覆铜板制作图案
| 实验原理 | 利用FeCl3溶液做“腐蚀液”,将覆铜板上不需要的铜腐蚀。 |
| 实验操作 | 1.取一小块覆铜板,用油性笔在覆铜板画上设计好的“化学”图案; 2.浸入盛有FeCl3溶液的小烧杯中; 3.一段时间后,取出覆铜板并用水清洗干净; 4.观察实验现象,并展示制作的图案。  |
| 实验现象 | 用油性笔画出的图案处不被腐蚀,洗净后板上留下设计的“化学”图案。 |
| 离子方程式 | _______ |
| 实验结论 | 铜可以被FeCl3溶液腐蚀。 |
②使用过的“腐蚀液”会失效,但还可以回收利用,其中有一步反应需要将Fe2+转化为Fe3+,下列试剂能实现上述变化的是
A.氯气B.铁C.铜D.稀硫酸
您最近一年使用:0次
6 . 氯化铁 FeCl3是一种化学常用试剂,在化学实验和工农业生产有着重要的用途。
(1)实验室常用饱和FeCl3溶液来制备Fe(OH)3胶体。
已知:在25℃时,FeCl3的溶解度为90g/100g水。
实验Ⅰ:配置20.0g饱和FeCl3溶液。
①需要用到的仪器有:药匙、托盘天平、玻璃棒、___________ 、___________ 、烧杯。
②该实验需称量FeCl3固体___________ g。
实验Ⅱ:制备Fe(OH)3胶体。
甲同学取一小烧杯,加入25mL蒸馏水,加热至沸腾,向沸水中逐滴加入1~2mL饱和氯化铁溶液,继续煮沸至液体呈红褐色,停止加热。
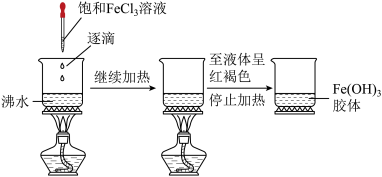
③写出此过程中的化学方程式:___________ 。
④除去氢氧化铁胶体中的氯化铁采用的方法是___________ (填写字母)。
A.过滤 B.渗析 C.蒸发
(2)工业上制印刷电路板时常用FeCl3溶液做“腐蚀液”,原理为利用FeCl3溶液将Cu溶解。某化学兴趣小组根据此原理在覆铜板上制作“化学”字样的图案。
实验Ⅲ:利用覆铜板制作图案
①写出制作过程发生反应的离子方程式:___________ 。
②使用过的“腐蚀液”会失效,但还可以回收利用,其中有一步反应需要将Fe2+转化为Fe3+,下列试剂能实现上述变化的是___________ (填序号)。
A.氯气 B.铁 C.酸性KMnO4溶液 D.稀硫酸
(1)实验室常用饱和FeCl3溶液来制备Fe(OH)3胶体。
已知:在25℃时,FeCl3的溶解度为90g/100g水。
实验Ⅰ:配置20.0g饱和FeCl3溶液。
①需要用到的仪器有:药匙、托盘天平、玻璃棒、
②该实验需称量FeCl3固体
实验Ⅱ:制备Fe(OH)3胶体。
甲同学取一小烧杯,加入25mL蒸馏水,加热至沸腾,向沸水中逐滴加入1~2mL饱和氯化铁溶液,继续煮沸至液体呈红褐色,停止加热。

③写出此过程中的化学方程式:
④除去氢氧化铁胶体中的氯化铁采用的方法是
A.过滤 B.渗析 C.蒸发
(2)工业上制印刷电路板时常用FeCl3溶液做“腐蚀液”,原理为利用FeCl3溶液将Cu溶解。某化学兴趣小组根据此原理在覆铜板上制作“化学”字样的图案。
实验Ⅲ:利用覆铜板制作图案
| 实验原理 | 利用FeCl3溶液做“腐蚀液”,将覆铜板上不需要的铜腐蚀。 |
| 实验操作 | 1.取一小块覆铜板,用油性笔在覆铜板画上设计好的“化学”图案; 2.浸入盛有FeCl3溶液的小烧杯中; 3.一段时间后,取出覆铜板并用水清洗干净; 4.观察实验现象,并展示制作的图案。  |
| 实验现象 | 用油性笔画出的图案处不被腐蚀,洗净后板上留下设计的“化学”图案。 |
| 离子方程式 | |
| 实验结论 | 铜可以被FeCl3溶液腐蚀。 |
②使用过的“腐蚀液”会失效,但还可以回收利用,其中有一步反应需要将Fe2+转化为Fe3+,下列试剂能实现上述变化的是
A.氯气 B.铁 C.酸性KMnO4溶液 D.稀硫酸
您最近一年使用:0次
解题方法
7 . 已知:A、B、C、D是短周期主族元素,E、F为长周期元素,请根据下列信息回答有关问题。
(1)写出A元素的最高价氧化物的电子式:___________ ;C、D、E的简单离子半径由大到小的顺序为___________ (填离子符号)。
(2)写出E元素的氧化物(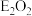 )与水反应的离子方程式:
)与水反应的离子方程式:___________ 。
(3)F元素的单质可以在C元素的单质中燃烧,其产物的饱和溶液与沸水反应可以得到能产生丁达尔效应的分散系,写出该产物的浓溶液与沸水反应的化学方程式:___________ 。
(4)C元素的最高价氧化物对应的水化物与E元素的最高价氧化物对应的水化物反应的离子方程式为___________ 。
(5)B元素与E元素形成的化合物属于___________ (填“离子”或“共价”)化合物,该化合物中所含的化学键为___________ (填“共价键”或“离子键”)。
| ① | A的一种氧化物可用于人工降雨 |
| ② | B元素的简单阳离子中没有电子 |
| ③ | C的单质为黄绿色气体 |
| ④ | D是地壳中含量最高的金属元素 |
| ⑤ | E位于元素周期表第ⅠA族,核外电子层数为4 |
| ⑥ | F是用途最广泛的金属,它的一种氧化物可以作磁性材料 |
(2)写出E元素的氧化物(
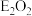 )与水反应的离子方程式:
)与水反应的离子方程式:(3)F元素的单质可以在C元素的单质中燃烧,其产物的饱和溶液与沸水反应可以得到能产生丁达尔效应的分散系,写出该产物的浓溶液与沸水反应的化学方程式:
(4)C元素的最高价氧化物对应的水化物与E元素的最高价氧化物对应的水化物反应的离子方程式为
(5)B元素与E元素形成的化合物属于
您最近一年使用:0次
解题方法
8 . 向少量 粉末中加入适量盐酸,反应后得到的
粉末中加入适量盐酸,反应后得到的 溶液呈棕黄色。回答下列问题:
溶液呈棕黄色。回答下列问题:
(1)赤铁矿的主要成分为 ,
, 俗称
俗称_______ ,请写出 的一种用途:
的一种用途:_______ 。
(2)取少量 溶液置于试管中,加入过量铁粉,该反应的离子方程式为
溶液置于试管中,加入过量铁粉,该反应的离子方程式为_______ 。
(3)向(2)反应后的溶液中加入NaOH溶液,产生的白色沉淀最终变为红褐色,请解释沉淀颜色变化的原因:_______ (用化学方程式表示)。
(4)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴 溶液,继续煮沸至溶液呈
溶液,继续煮沸至溶液呈_______ 色,即可制得 胶体。
胶体。
(5)取另一烧杯也加入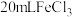 溶液,将此烧杯(编号甲)与盛有
溶液,将此烧杯(编号甲)与盛有 胶体的烧杯(编号乙)一起放黑暗处:分别用激光笔照射烧杯中的液体,可以看到
胶体的烧杯(编号乙)一起放黑暗处:分别用激光笔照射烧杯中的液体,可以看到_______ (填“编号甲”或“编号乙”)烧杯中的液体会产生丁达尔效应。这个实验可以用来区别_______ 。
 粉末中加入适量盐酸,反应后得到的
粉末中加入适量盐酸,反应后得到的 溶液呈棕黄色。回答下列问题:
溶液呈棕黄色。回答下列问题:(1)赤铁矿的主要成分为
 ,
, 俗称
俗称 的一种用途:
的一种用途:(2)取少量
 溶液置于试管中,加入过量铁粉,该反应的离子方程式为
溶液置于试管中,加入过量铁粉,该反应的离子方程式为(3)向(2)反应后的溶液中加入NaOH溶液,产生的白色沉淀最终变为红褐色,请解释沉淀颜色变化的原因:
(4)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴
 溶液,继续煮沸至溶液呈
溶液,继续煮沸至溶液呈 胶体。
胶体。(5)取另一烧杯也加入
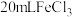 溶液,将此烧杯(编号甲)与盛有
溶液,将此烧杯(编号甲)与盛有 胶体的烧杯(编号乙)一起放黑暗处:分别用激光笔照射烧杯中的液体,可以看到
胶体的烧杯(编号乙)一起放黑暗处:分别用激光笔照射烧杯中的液体,可以看到
您最近一年使用:0次
2022高一·上海·专题练习
解题方法
9 . 铁及其化合物在生产生活中有极其重要的用途,请回答下列问题:
(1)氢氧化铁胶体具有良好的净水效果,胶体中分散质微粒大小为_______ 。制备时,将_______ 逐滴滴加至_______ 中,待液体呈红褐色后,停止加热;反应方程式为_______ 。
(2)鉴别氯化铁溶液和氢氧化铁胶体,除了可通过观察颜色以外,还有的方法是_______ 。
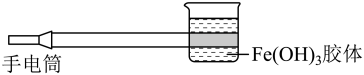
(3)如下图是在实验室中进行 Fe(OH)3胶体丁达尔效应实验的示意图,该图中有一处明显错误是_______ ,原因是_______ (试从分散系分类的角度进行解释说明)。
(4)Fe(OH)3胶体中逐滴加入了稀H2SO4溶液,结果出现了一系列变化。
a. 先出现红褐色沉淀,原因是_______ 。
b. 随后沉淀溶解,此反应的化学方程式是_______ 。
(1)氢氧化铁胶体具有良好的净水效果,胶体中分散质微粒大小为
(2)鉴别氯化铁溶液和氢氧化铁胶体,除了可通过观察颜色以外,还有的方法是
(3)如下图是在实验室中进行 Fe(OH)3胶体丁达尔效应实验的示意图,该图中有一处明显错误是

(4)Fe(OH)3胶体中逐滴加入了稀H2SO4溶液,结果出现了一系列变化。
a. 先出现红褐色沉淀,原因是
b. 随后沉淀溶解,此反应的化学方程式是
您最近一年使用:0次
名校
10 . X、Y、Z、W、V是原子序数依次增大的短周期元素,X为金属元素,其半径在同周期中最大, 元素原子最外层电子数为次外层的两倍,
元素原子最外层电子数为次外层的两倍, 的最简单氢化物为甲,甲能使湿润的红色石蕊试纸变蓝,
的最简单氢化物为甲,甲能使湿润的红色石蕊试纸变蓝, 的气态氢化物为乙,甲、乙混合时有白烟生成,
的气态氢化物为乙,甲、乙混合时有白烟生成, 的最外层电子数等于其电子层数,
的最外层电子数等于其电子层数, 为第四周期常见的元素,其合金在我国用量最多,用途最广。下列说法正确的是
为第四周期常见的元素,其合金在我国用量最多,用途最广。下列说法正确的是
 元素原子最外层电子数为次外层的两倍,
元素原子最外层电子数为次外层的两倍, 的最简单氢化物为甲,甲能使湿润的红色石蕊试纸变蓝,
的最简单氢化物为甲,甲能使湿润的红色石蕊试纸变蓝, 的气态氢化物为乙,甲、乙混合时有白烟生成,
的气态氢化物为乙,甲、乙混合时有白烟生成, 的最外层电子数等于其电子层数,
的最外层电子数等于其电子层数, 为第四周期常见的元素,其合金在我国用量最多,用途最广。下列说法正确的是
为第四周期常见的元素,其合金在我国用量最多,用途最广。下列说法正确的是| A.离子半径:V>W>Z |
| B.甲、乙混合时所生成的白烟为离子化合物,但其中含有共价键 |
C. 、 、 分别在足量氧气中燃烧分别生成X2O2,YO2 分别在足量氧气中燃烧分别生成X2O2,YO2 |
| D.在足量的沸水中滴入含有16.25gNV3的溶液可得到0.1molN(OH)3胶粒 |
您最近一年使用:0次
2022-05-06更新
|
165次组卷
|
2卷引用:四川省眉山市仁寿县2022-2023学年高一下学期4月期中考试化学试题



