解题方法
1 . 如图是元素①~⑥在元素周期表中的位置。
(1)①的原子结构示意图是___________ 。
(2)③在周期表中的位置是___________ 。
(3)③、④、⑤、⑥形成的简单离子中,半径最小的是___________ (填离子符号)。
(4)非金属性:②___________ ③(填“>”或“<”),从原子结构角度解释其原因___________ 。
(5)⑤的最高价氧化物的水化物可以与⑥的单质反应,请写出反应的离子方程式___________ 。
(6)下列关于①的说法正确的是___________ 。
a.在同主族元素中,①最高价氧化物的水化物的碱性最强
b.①在空气中加热生成的产物是过氧化物
c.①可以与水反应生成氢气
(7)已知电负性的数值表示原子对电子吸引能力的相对大小。以下是几种原子的电负性数值:
x的范围是___________ 。请根据以上数据推测,在目前已知的118种元素中,电负性最大的元素为___________ (填元素符号)。
| ① | ② | ③ | ④ | ||||
| ⑤ | ⑥ | ||||||
(2)③在周期表中的位置是
(3)③、④、⑤、⑥形成的简单离子中,半径最小的是
(4)非金属性:②
(5)⑤的最高价氧化物的水化物可以与⑥的单质反应,请写出反应的离子方程式
(6)下列关于①的说法正确的是
a.在同主族元素中,①最高价氧化物的水化物的碱性最强
b.①在空气中加热生成的产物是过氧化物
c.①可以与水反应生成氢气
(7)已知电负性的数值表示原子对电子吸引能力的相对大小。以下是几种原子的电负性数值:
| 元素 | 铝 | 硅 | 磷 | 硫 | 氯 |
| 电负性 | 1.5 | 1.8 | 2.1 | x | 3.0 |
您最近一年使用:0次
名校
解题方法
2 . 下列表示物质结构的化学用语或模型正确的是
A.Se的原子结构示意图: |
B.基态铬原子的价电子排布式: |
C.基态氧原子的轨道表示式: |
| D.Fe3+的价电子排布式:3d5 |
您最近一年使用:0次
解题方法
3 . 下图为元素周期表的一部分,用化学用语回答下列问题:
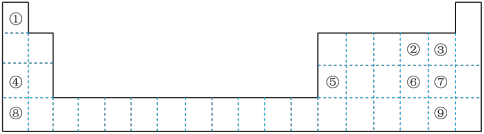
(1)请画出上述九种元素中非金属性最强的元素的原子结构示意图___________ 。
(2)④⑤⑧的阳离子中氧化性最强的是___________ (填离子符号)。
(3)上述元素中最高价氧化物对应的水化物中酸性最强的酸与氢氧化钠反应的化学方程式为___________ 。
(4)用电子式表示⑥和④形成化合物的过程___________ 。
(5)②和④形成原子个数比为1 :1的化合物中所含化学键类型为___________ 。
(6)现在含有元素硒(Se)的保健品开始进入市场,已知硒元素与氧元素同主族,比氧多2个电子层,则下列叙述中正确的是___________。
(7)①和④可形成AB型离子化合物,该离子化合物的电子式为___________ ,其与水反应放出气体的化学方程式为___________ 。

(1)请画出上述九种元素中非金属性最强的元素的原子结构示意图
(2)④⑤⑧的阳离子中氧化性最强的是
(3)上述元素中最高价氧化物对应的水化物中酸性最强的酸与氢氧化钠反应的化学方程式为
(4)用电子式表示⑥和④形成化合物的过程
(5)②和④形成原子个数比为1 :1的化合物中所含化学键类型为
(6)现在含有元素硒(Se)的保健品开始进入市场,已知硒元素与氧元素同主族,比氧多2个电子层,则下列叙述中正确的是___________。
| A.原子序数为34 |
| B.气态氢化物的还原性H2Se>H2S |
| C.SeO2不能与氢氧化钠反应 |
| D.SeO2既有氧化性又有还原性 |
(7)①和④可形成AB型离子化合物,该离子化合物的电子式为
您最近一年使用:0次
名校
解题方法
4 . 下列化学用语表示不正确的是
A. 、 、 、 、 互为同位素 互为同位素 |
B.中子数为18的氯原子: |
C. 的电离方程式: 的电离方程式: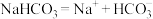 |
D. 的结构示意图 的结构示意图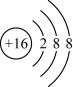 |
您最近一年使用:0次
2024-01-25更新
|
129次组卷
|
2卷引用:天津市第四十七中学2023-2024学年高一上学期12月月考化学试题
名校
5 . 元素X、Y、Z、M、R均为短周期主族元素,且原子序数依次增大。已知:Y为地壳中含量最多的元素;M原子的最外层电子数与次外层电子数之比为3:4; 、
、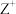 、
、 的离子半径逐渐减小;化合物XR常温下为气体。请回答下列问题:
的离子半径逐渐减小;化合物XR常温下为气体。请回答下列问题:
(1)M元素周期表中的位置为___________ ;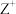 的结构示意图为
的结构示意图为___________ 。
(2)写出X、Y、R按原子个数之比1:1:1形成的化合物的结构式:___________ 。
(3)X与Y可分别形成10电子分子和18电子分子,写出18电子分子转化成10电子分子的化学方程式:___________ 。
(4)R的非金属性强于M的,下列能证明这一事实的是___________(填字母)。
 、
、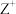 、
、 的离子半径逐渐减小;化合物XR常温下为气体。请回答下列问题:
的离子半径逐渐减小;化合物XR常温下为气体。请回答下列问题:(1)M元素周期表中的位置为
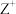 的结构示意图为
的结构示意图为(2)写出X、Y、R按原子个数之比1:1:1形成的化合物的结构式:
(3)X与Y可分别形成10电子分子和18电子分子,写出18电子分子转化成10电子分子的化学方程式:
(4)R的非金属性强于M的,下列能证明这一事实的是___________(填字母)。
| A.常温下的R单质熔沸点比M单质的高 |
| B.R的简单氢化物比M的更稳定 |
| C.一定条件下,R和M的单质都能与NaOH溶液反应 |
D.最高价氧化物对应水化物的酸性强弱: |
您最近一年使用:0次
名校
6 . 近来医学界通过用放射性 标记的
标记的 ,发现一种
,发现一种 的羧酸衍生物在特定条件下可通过断裂DNA杀死细胞,从而抑制艾滋病病毒(AIDS)。则有关
的羧酸衍生物在特定条件下可通过断裂DNA杀死细胞,从而抑制艾滋病病毒(AIDS)。则有关 的下列说法中正确的是
的下列说法中正确的是
 标记的
标记的 ,发现一种
,发现一种 的羧酸衍生物在特定条件下可通过断裂DNA杀死细胞,从而抑制艾滋病病毒(AIDS)。则有关
的羧酸衍生物在特定条件下可通过断裂DNA杀死细胞,从而抑制艾滋病病毒(AIDS)。则有关 的下列说法中正确的是
的下列说法中正确的是A. 原子与 原子与 中普通碳原子的化学性质不同 中普通碳原子的化学性质不同 |
B. 原子与 原子与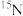 原子所含中子数不同 原子所含中子数不同 |
C.电子式表示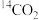 的形成过程为: 的形成过程为: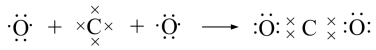 |
D. 与 与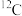 、 、 互为同素异形体 互为同素异形体 |
您最近一年使用:0次
2024-01-25更新
|
80次组卷
|
3卷引用:四川省绵阳市绵阳中学2023-2024学年高一上学期期末模拟测试化学试题
名校
7 . 下表是元素周期表的一部分,请用规范的化学用语回答有关问题:
(1)元素⑨在周期表中所处位置 ___________ 。
(2)表中化学性质最不活泼的元素,其原子结构示意图为___________ 。
(3)④⑦⑨元素形成的化合物中含有的化学键类型为___________ 。
(4)④、⑧、⑨三种元素的常见离子的半径由小到大的顺序为___________ 。(填离子符号)
(5)①、⑥、⑦三种元素的最高价氧化物的水化物中碱性最强的是___________ 。
(6)写出⑥、⑧元素的最高价氧化物的水化物发生反应的离子方程式___________ 。
(7)②、③、④的简单氢化物中最稳定的是___________ ;写出⑧的最高价氧化物与⑥的最高价氧化物对应水化物反应的离子方程式___________ 。
(8)用电子式表示⑥与⑨形成的化合物的形成过程___________ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 二 | ① | ② | ③ | ④ | ⑤ | |||
| 三 | ⑥ | ⑦ | ⑧ | ⑨ |
(2)表中化学性质最不活泼的元素,其原子结构示意图为
(3)④⑦⑨元素形成的化合物中含有的化学键类型为
(4)④、⑧、⑨三种元素的常见离子的半径由小到大的顺序为
(5)①、⑥、⑦三种元素的最高价氧化物的水化物中碱性最强的是
(6)写出⑥、⑧元素的最高价氧化物的水化物发生反应的离子方程式
(7)②、③、④的简单氢化物中最稳定的是
(8)用电子式表示⑥与⑨形成的化合物的形成过程
您最近一年使用:0次
名校
8 . 氯化钠是日常生活必需品和重要的化工原料。
(1)请写出氯化钠的电子式___________ 。
(2)氯碱工业是以电解饱和食盐水为基础,生产一系列含氯、含钠化工产品的工业,请写出相关的化学方程___________ 。
(3)电解饱和食盐水装置中,产生氯气的电极为___________。
(4)如何检验该极产生氯气___________ 。
(5)下列物质属于电解质,熔融状态下不能导电的是___________。
(6)该方法制得的烧碱中可能混有少量 ,请写出检验是否混有
,请写出检验是否混有 的买验方法
的买验方法___________ 。
(7)生活中常用漂白粉对衣物进行漂白,已知 漂白效果优于漂白粉,下列物质对提高漂白粉的漂白作用无明显效果的是___________。
漂白效果优于漂白粉,下列物质对提高漂白粉的漂白作用无明显效果的是___________。
(8)用玻璃棒蘸取饱和氯水滴在pH试纸中部,观察到的现象如图所示:
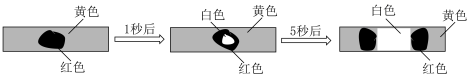
使pH试纸变红的物质X是___________ (填化学式),使pH试纸变白的物质Y是___________ (填化学式)。通过pH试纸颜色变化情况说出X、Y两种物质某项性质的差异___________ (任写一条)。
(1)请写出氯化钠的电子式
(2)氯碱工业是以电解饱和食盐水为基础,生产一系列含氯、含钠化工产品的工业,请写出相关的化学方程
(3)电解饱和食盐水装置中,产生氯气的电极为___________。
| A.正极 | B.负极 | C.阴极 | D.阳极 |
(4)如何检验该极产生氯气
(5)下列物质属于电解质,熔融状态下不能导电的是___________。
A. | B. | C. | D.Cu |
(6)该方法制得的烧碱中可能混有少量
 ,请写出检验是否混有
,请写出检验是否混有 的买验方法
的买验方法(7)生活中常用漂白粉对衣物进行漂白,已知
 漂白效果优于漂白粉,下列物质对提高漂白粉的漂白作用无明显效果的是___________。
漂白效果优于漂白粉,下列物质对提高漂白粉的漂白作用无明显效果的是___________。| A.食盐 | B. 和水蒸气 和水蒸气 | C.稀盐酸 | D.食醋 |
(8)用玻璃棒蘸取饱和氯水滴在pH试纸中部,观察到的现象如图所示:

使pH试纸变红的物质X是
您最近一年使用:0次
名校
解题方法
9 . 《自然》杂志曾报道我国科学家通过测量 中
中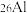 和
和 两种核素的比例确定“北京人”生存年代的研究结果,这种测量方法叫“铝铍测年法”。自然界一共存在三种硅的稳定同位素,分别是
两种核素的比例确定“北京人”生存年代的研究结果,这种测量方法叫“铝铍测年法”。自然界一共存在三种硅的稳定同位素,分别是 。
。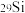 和
和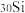 。完成下列填空:
。完成下列填空:
(1)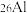 和
和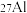 ___________。
___________。
(2)Si原子的结构示意图为___________ 。
(3)基态Si原子能量最高的能层和该能层中电子排布式分别为___________。
(4) 的中子数为
的中子数为___________ ;一个 原子的质量为
原子的质量为___________ g。(用 表示)
表示)
(5)计算硅元素的近似相对原子质量的计算式为: %
% %
% %,其中
%,其中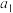 %。
%。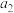 %……指各同位素的
%……指各同位素的___________ 。
(6) 空间结构与
空间结构与 相似,
相似, 分子中存在的化学键
分子中存在的化学键___________ , 空间构型
空间构型___________ 。
A.离子键 B.共价键 C.金属键
(7)向盐酸中逐滴滴加硅酸钠溶液,当pH达到6~7时得到一种乳白色、半透明的分散系,其分散质为粒径在 的
的 粒子。该分散系属于
粒子。该分散系属于___________ 。
A.溶液 B.悬浊液 C.胶体
 中
中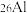 和
和 两种核素的比例确定“北京人”生存年代的研究结果,这种测量方法叫“铝铍测年法”。自然界一共存在三种硅的稳定同位素,分别是
两种核素的比例确定“北京人”生存年代的研究结果,这种测量方法叫“铝铍测年法”。自然界一共存在三种硅的稳定同位素,分别是 。
。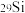 和
和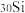 。完成下列填空:
。完成下列填空:(1)
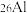 和
和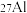 ___________。
___________。| A.是不同核素,具有相同的物理性质 | B.是同一种核素 |
| C.具有相同的中子数 | D.具有相同的化学性质 |
(3)基态Si原子能量最高的能层和该能层中电子排布式分别为___________。
A.K层,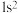 | B.M层,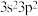 | C.M层,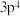 | D.L层,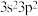 |
 的中子数为
的中子数为 原子的质量为
原子的质量为 表示)
表示)(5)计算硅元素的近似相对原子质量的计算式为:
 %
% %
% %,其中
%,其中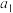 %。
%。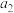 %……指各同位素的
%……指各同位素的(6)
 空间结构与
空间结构与 相似,
相似, 分子中存在的化学键
分子中存在的化学键 空间构型
空间构型A.离子键 B.共价键 C.金属键
(7)向盐酸中逐滴滴加硅酸钠溶液,当pH达到6~7时得到一种乳白色、半透明的分散系,其分散质为粒径在
 的
的 粒子。该分散系属于
粒子。该分散系属于A.溶液 B.悬浊液 C.胶体
您最近一年使用:0次
名校
10 . 下列表示相关微粒的化学用语正确的是
| A.含6个质子和8个中子的碳元素的核素符号:l2C |
| B.NH4Cl中N元素的化合价:+3 |
C.氯离子的结构示意图: |
D.用电子式表示氯化氢的形成过程: |
您最近一年使用:0次
2024-01-23更新
|
83次组卷
|
3卷引用:湖南省邵阳市2023-2024学年高一上学期1月期末联考化学试题



