1 . 二氧化碳的捕集和转化是科学研究中的热点问题,我国科研人员提出了由 和
和 转化为
转化为 和
和 的反应历程如图,下列说法正确的是
的反应历程如图,下列说法正确的是
 和
和 转化为
转化为 和
和 的反应历程如图,下列说法正确的是
的反应历程如图,下列说法正确的是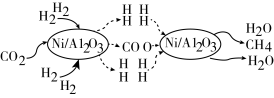
A.该反应的化学方程式为: |
B.反应中使用的催化剂为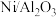 ,Al和 ,Al和 是同周期元素 是同周期元素 |
C. 分子的电子式为: 分子的电子式为: |
D.上述反应中捕集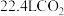 ,转移电子数为 ,转移电子数为 |
您最近一年使用:0次
解题方法
2 . 回答下列问题。
(1)氮元素在元素周期表中的位置是第___________ 周期,第___________ 族。
(2) 是元素周期表中第
是元素周期表中第___________ 号元素。
(3) 的M能层电子排布式是
的M能层电子排布式是___________ ,价层电子排布图是___________ ,原子结构示意图是___________ 。
(1)氮元素在元素周期表中的位置是第
(2)
 是元素周期表中第
是元素周期表中第(3)
 的M能层电子排布式是
的M能层电子排布式是
您最近一年使用:0次
3 . 近日,科学家揭示丙烷在氮化硼上的氧化脱氢反应中自由基和含氧化合物的转化路径如图所示:

A.图中电负性最大的元素对应基态原子的电子排布式为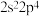 |
B.物质b的结构简式为 |
| C.耐高温、耐磨新型无机非金属材料氮化硼为分子晶体 |
D.物质c的电子式为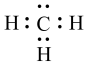 |
您最近一年使用:0次
4 . 1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力,历经142年,元素周期表体现了元素位构性的关系,揭示了元素间的内在联系。人体必需的一些元素在周期表中的分布情况如下:
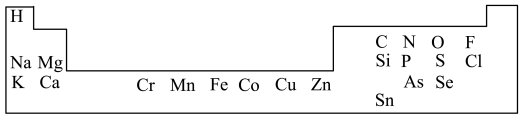
(1)碳、氢、氧、氮是人体内的主要元素。碳有多种同位素,其中考古时用于测定文物年代的是______ 。 是一种绿色氧化剂,电子式为
是一种绿色氧化剂,电子式为______ 。
(2)第三周期半径最小的简单离子为______ 。
(3)钙元素和磷元素促进了我们骨骼发育与牙齿的正常生长。从物质分类的角度看,羟基磷灰石 属于
属于______ (填“酸”、“碱”、“盐”或“氧化物”)。Ca与Mg在元素周期表同一族,化学性质相似同时也有递变性,试写出Ca与 反应的化学方程式:
反应的化学方程式:____________ 。
(4)硒(Se)具有抗氧化、增强人体抵抗力的功效。Se在元素周期表中的位置是______ ,原子序数为______ 。
(5)由元素C和O形成的三核直线形分子的结构式为______ 。
(6)用电子式表示元素Na和S的原子形成的化合物(该化合物含有三个原子核)的形成过程:____________ 。
(7)能比较元素S和Cl非金属性强弱的实验事实是______ (填字母)。
a. 的酸性比HCl的酸性弱
的酸性比HCl的酸性弱
b.单质 与
与 化合比单质S与
化合比单质S与 化合容易,且HCl的稳定性比
化合容易,且HCl的稳定性比 的强
的强
c.向 的水溶液中通入少量
的水溶液中通入少量 可置换出单质S
可置换出单质S

(1)碳、氢、氧、氮是人体内的主要元素。碳有多种同位素,其中考古时用于测定文物年代的是
 是一种绿色氧化剂,电子式为
是一种绿色氧化剂,电子式为(2)第三周期半径最小的简单离子为
(3)钙元素和磷元素促进了我们骨骼发育与牙齿的正常生长。从物质分类的角度看,羟基磷灰石
 属于
属于 反应的化学方程式:
反应的化学方程式:(4)硒(Se)具有抗氧化、增强人体抵抗力的功效。Se在元素周期表中的位置是
(5)由元素C和O形成的三核直线形分子的结构式为
(6)用电子式表示元素Na和S的原子形成的化合物(该化合物含有三个原子核)的形成过程:
(7)能比较元素S和Cl非金属性强弱的实验事实是
a.
 的酸性比HCl的酸性弱
的酸性比HCl的酸性弱b.单质
 与
与 化合比单质S与
化合比单质S与 化合容易,且HCl的稳定性比
化合容易,且HCl的稳定性比 的强
的强c.向
 的水溶液中通入少量
的水溶液中通入少量 可置换出单质S
可置换出单质S
您最近一年使用:0次
5 . A、B、C、D、E、F是原子序数依次增大的前四周期元素,A元素电子只有一种自旋取向;B元素原子的价电子排布是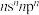 ,C是地壳中含量最多的非金属元素;
,C是地壳中含量最多的非金属元素; 第三周期中半径最小的简单离子;E元素负一价离子的能层结构与氩相同;F元素基态原子核外有7个能级上有电子且有4个未成对电子。
第三周期中半径最小的简单离子;E元素负一价离子的能层结构与氩相同;F元素基态原子核外有7个能级上有电子且有4个未成对电子。
请回答:
(1)A是_______ 区的元素,BC元素形成的双原子分子结构与 相似,写出该双原子分子的电子式
相似,写出该双原子分子的电子式_______ 。
(2)C、D、E的简单离子的半径从大到小的顺序_______ (用离子符号表示)。
(3)F元素有两种常见的价态,比较这两种价态阳离子的稳定性
_______ 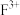 (填“>”、“<”或“=”),理由是
(填“>”、“<”或“=”),理由是_______ 。
(4)与D元素成“对角线规则”关系的某短周期元素的最高价氧化物对应的水化物具有两性,写出该两性物质与E元素的最高价氧化物对应的水化物反应的化学方程式_______ 。
(5)物质X由ABC三种元素构成。按下图实验装置(部分装置略)对X进行元素分析:

①依次点燃煤气灯_______ →_______ ,进行实验。实验过程中CuO的作用是_______ (举1例,用化学方程式表示)。
②若样品X质量为2.36g,实验结束后,c管增重1.08g,d管增重3.52g。质谱测得该有机物的相对分子量为118,其分子式为_______ 。
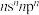 ,C是地壳中含量最多的非金属元素;
,C是地壳中含量最多的非金属元素; 第三周期中半径最小的简单离子;E元素负一价离子的能层结构与氩相同;F元素基态原子核外有7个能级上有电子且有4个未成对电子。
第三周期中半径最小的简单离子;E元素负一价离子的能层结构与氩相同;F元素基态原子核外有7个能级上有电子且有4个未成对电子。请回答:
(1)A是
 相似,写出该双原子分子的电子式
相似,写出该双原子分子的电子式(2)C、D、E的简单离子的半径从大到小的顺序
(3)F元素有两种常见的价态,比较这两种价态阳离子的稳定性

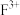 (填“>”、“<”或“=”),理由是
(填“>”、“<”或“=”),理由是(4)与D元素成“对角线规则”关系的某短周期元素的最高价氧化物对应的水化物具有两性,写出该两性物质与E元素的最高价氧化物对应的水化物反应的化学方程式
(5)物质X由ABC三种元素构成。按下图实验装置(部分装置略)对X进行元素分析:

①依次点燃煤气灯
②若样品X质量为2.36g,实验结束后,c管增重1.08g,d管增重3.52g。质谱测得该有机物的相对分子量为118,其分子式为
您最近一年使用:0次
解题方法
6 . 回答下列问题。
(1)请写出NH4Br的电子式___________ ;请写出H2O2的结构式:___________ 。
(2)请写出亚硫酸在水中电离的方程式:___________ 。
(3)请写出一种能比较碳元素和硅元素非金属性强弱的方程式:___________ 。
(4)水晶中主要成分的化学式为:___________ 。
(1)请写出NH4Br的电子式
(2)请写出亚硫酸在水中电离的方程式:
(3)请写出一种能比较碳元素和硅元素非金属性强弱的方程式:
(4)水晶中主要成分的化学式为:
您最近一年使用:0次
解题方法
7 . 请回答下列问题:
(1)氯原子的最外层电子数为___________ ;其最高价氧化物的化学式是___________ 。
(2)维生素 又称“抗坏血酸”,能将
又称“抗坏血酸”,能将 转化为
转化为 ,说明维生素
,说明维生素 具有
具有___________ 性(填“还原”或“氧化”)。
(3)写出白色的氢氧化亚铁沉淀在空气中变色的化学反应方程式___________ 。
(1)氯原子的最外层电子数为
(2)维生素
 又称“抗坏血酸”,能将
又称“抗坏血酸”,能将 转化为
转化为 ,说明维生素
,说明维生素 具有
具有(3)写出白色的氢氧化亚铁沉淀在空气中变色的化学反应方程式
您最近一年使用:0次
名校
8 . 一种液化石油气在活性炭作用下脱硫机理如图所示,下列说法正确的是
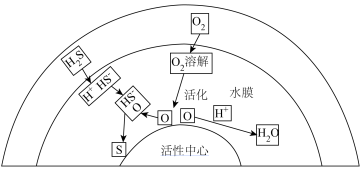

A.总反应为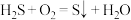 |
B.在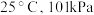 下,反应中每转移 下,反应中每转移 ,消耗 ,消耗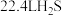 |
| C.反应过程中有极性键和非极性键的断裂 |
D. 的分子结构模型为 的分子结构模型为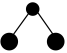 |
您最近一年使用:0次
名校
解题方法
9 . 按要求填空。
(1)当食盐不慎洒落在天然气的火焰上,观察到的现象是___________ ;该变化属于___________ (填:“物理变化”或“化学变化”)。
(2) 在食品行业中应用广泛,溶于水后电离方程式
在食品行业中应用广泛,溶于水后电离方程式___________ 。
(3)已知某主族元素的原子结构示意图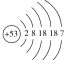 ,请写出它在周期表中的位置
,请写出它在周期表中的位置___________ ;该元素属于___________ 元素(填“金属”、“非金属”或“稀有气体”)。
(4)少量的淀粉 溶液中滴加几滴
溶液中滴加几滴 溶液,溶液变成蓝色,反应的离子方程式为:
溶液,溶液变成蓝色,反应的离子方程式为:___________ 。
(5)下列各组物质之间关系互为同位素的是___________。
(1)当食盐不慎洒落在天然气的火焰上,观察到的现象是
(2)
 在食品行业中应用广泛,溶于水后电离方程式
在食品行业中应用广泛,溶于水后电离方程式(3)已知某主族元素的原子结构示意图
 ,请写出它在周期表中的位置
,请写出它在周期表中的位置(4)少量的淀粉
 溶液中滴加几滴
溶液中滴加几滴 溶液,溶液变成蓝色,反应的离子方程式为:
溶液,溶液变成蓝色,反应的离子方程式为:(5)下列各组物质之间关系互为同位素的是___________。
| A.D和T | B.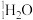 与 与 | C.金刚石与石墨 | D. 与 与 |
您最近一年使用:0次
名校
解题方法
10 . a、b、c、d、e、f为前20号主族元素,其最高正化合价或最低负化合价与原子序数的关系如图所示:
(1)e在元素周期表中的位置是_______ 。
(2)写出b的简单氢化物的电子式_______ ,f的最高价氧化物的水化物含_______ 键(填字母)。
A.离子键 B.极性非价键 C.非极性共价键
(3)d单质与c的最高价氧化物的水化物是家庭厨卫管道疏通剂的主要成分,疏通管道时发生反应的化学方程式是_______ 。
(4)①用电子式表示化合物ce的形成过程______ 。
②b、c、d元素所形成离子的半径从大到小的顺序为:_______ (用离子符号表示)。
(5)化合物fb2可与水缓慢反应,常用作鱼塘的供氧剂,同时生成一种碱,试写出其反应的化学方程式是_______ 。

(1)e在元素周期表中的位置是
(2)写出b的简单氢化物的电子式
A.离子键 B.极性非价键 C.非极性共价键
(3)d单质与c的最高价氧化物的水化物是家庭厨卫管道疏通剂的主要成分,疏通管道时发生反应的化学方程式是
(4)①用电子式表示化合物ce的形成过程
②b、c、d元素所形成离子的半径从大到小的顺序为:
(5)化合物fb2可与水缓慢反应,常用作鱼塘的供氧剂,同时生成一种碱,试写出其反应的化学方程式是
您最近一年使用:0次
2024-02-26更新
|
162次组卷
|
2卷引用:河北省石家庄市第一中学西校区2023-2024高一上学期期末考试化学试题



