解题方法
1 . 有A、B、C、D、E五种短周期主族元素,原子序数依次增大。①A元素最外层电子数是次外层电子数的2倍。②B的阴离子和C的阳离子与氖原子的电子层结构相同。③在通常状况下,B的单质是气体,0.1molB的气体与足量的氢气完全反应共有0.4mol电子转移。④C的单质在点燃时与B的单质充分反应,生成淡黄色的固体,此淡黄色固体能与AB2反应可生成B的单质。⑤D与B同主族且D的气态氢化物与其最高价含氧酸间能发生氧化还原反应。
(1)A元素的最高价氧化物的电子式_____ 。
(2)D元素在周期表的位置是_____ ,其简单阴离子的结构示意图为_____ 。B、C、D、E的简单离子半径由小到大的顺序为_____ (用化学式表示)。
(3)①下列表述能证明D非金属性比E弱这一事实的有_____ (填序号)。
A.常温下D的单质和E的单质状态不同
B.E的氢化物比D的氢化物稳定
C.一定条件下D和E的单质都能与钠反应
D.D的最高价含氧酸酸性弱于E的最高价含氧酸
E.D的单质能与E的氢化物反应生成E单质
②请从原子结构角度解释D非金属性比E弱的原因_____ 。
③请设计一个简单的实验证明D非金属性比E弱:_____ 。
(4)D元素的低价氧化物与E的单质的水溶液反应的离子方程式为_____ 。
(5)C与D能形成2:1的化合物,用电子式表示该化合物的形成过程:_____ 。
(1)A元素的最高价氧化物的电子式
(2)D元素在周期表的位置是
(3)①下列表述能证明D非金属性比E弱这一事实的有
A.常温下D的单质和E的单质状态不同
B.E的氢化物比D的氢化物稳定
C.一定条件下D和E的单质都能与钠反应
D.D的最高价含氧酸酸性弱于E的最高价含氧酸
E.D的单质能与E的氢化物反应生成E单质
②请从原子结构角度解释D非金属性比E弱的原因
③请设计一个简单的实验证明D非金属性比E弱:
(4)D元素的低价氧化物与E的单质的水溶液反应的离子方程式为
(5)C与D能形成2:1的化合物,用电子式表示该化合物的形成过程:
您最近一年使用:0次
名校
2 . 下列是几种粒子的结构示意图,有关说法正确的是


| A.①②是离子,③④是原子 | B.②③④对应的元素化学性质相似 |
| C.③④两种粒子可结合成一种分子 | D.①③对应的元素在同一周期 |
您最近一年使用:0次
3 . 下列说法不正确 的是
| A.12C与14C属于碳的两种核素 |
| B.水的摩尔质量:18g |
C.Na+的结构示意图: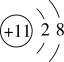 |
D.碳酸钠的电离方程式Na2CO3=2Na++ |
您最近一年使用:0次
4 . AgCl可溶于氨水生成Ag(NH3)2Cl,Ag(NH3)2Cl与NH3反应可生成Ag。反应如下:4Ag(NH3)2Cl + N2H4 + 4H2O = 4Ag↓ + N2↑ + 4NH4Cl + 4NH3·H2O。下列关于该反应说法正确的是
| A.Ag(NH3)2Cl发生氧化反应 |
| B.还原性:N2H4<Ag |
C.N2H4的结构式为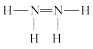 |
| D.每生成标准状况下11.2LN2,反应中转移2mol电子 |
您最近一年使用:0次
名校
解题方法
5 . 实验室用如图所示的方法制备饮用水消毒剂ClO2。已知: NCl3为强氧化剂,其中N元素为-3价,下列说法不正确的是
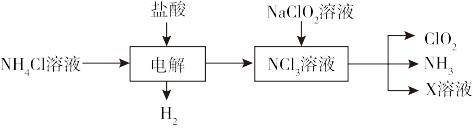

A.NH4Cl的电子式为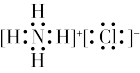 |
| B.NCl3分子中各原子均达到8电子稳定结构 |
| C.若NaClO2与NCl3恰好完全反应,则X溶液中溶质只有NaCl |
D.35Cl和37Cl的结构示意图均可表示为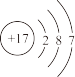 |
您最近一年使用:0次
解题方法
6 . 水解反应可用于无机化合物的制备,如制备TiO2的反应:TiCl4+(x+2)H2O⇌TiO2·xH2O↓+4HCl。下列说法错误的是
A.含中子数为27的49Ti原子: | B.Cl-的结构示意图为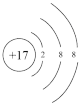 |
| C.H2O结构式为H—O—H | D.HCl电子式为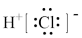 |
您最近一年使用:0次
2021-12-31更新
|
452次组卷
|
4卷引用:云南省大理白族自治州实验中学2021-2022学年高一上学期期末考试化学试题
云南省大理白族自治州实验中学2021-2022学年高一上学期期末考试化学试题石家庄示范性高中2022届高三上学期调研考试化学试题(已下线)一轮巩固卷1-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(北京专用)河北省示范性高中2023届高三9月份考试化学试题
名校
解题方法
7 . 人类在金星大气中探测到 ,实验室制备
,实验室制备 的方法有:①
的方法有:①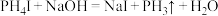 ;②
;② 。已知
。已知 是弱酸,其结构式为
是弱酸,其结构式为 。
。
下列说法不正确的是
 ,实验室制备
,实验室制备 的方法有:①
的方法有:①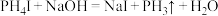 ;②
;② 。已知
。已知 是弱酸,其结构式为
是弱酸,其结构式为 。
。下列说法不正确的是
| A.反应①为非氧化还原反应 | B. 的结构示意图: 的结构示意图: |
C. 是三元酸 是三元酸 | D.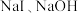 和 和 都是电解质 都是电解质 |
您最近一年使用:0次
2023-11-04更新
|
127次组卷
|
2卷引用:重庆市第一中学校2023-2024学年高一上学期定时练习化学试题
8 . 次磷酸钠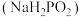 属于正盐,次磷酸根
属于正盐,次磷酸根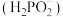 的球棍模型如图所示,下列说法错误的是
的球棍模型如图所示,下列说法错误的是
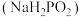 属于正盐,次磷酸根
属于正盐,次磷酸根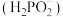 的球棍模型如图所示,下列说法错误的是
的球棍模型如图所示,下列说法错误的是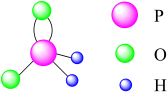
A.P的原子结构示意图为: |
B.次磷酸根 的化合价为 的化合价为 |
C.次磷酸钠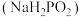 的电离方程式为: 的电离方程式为: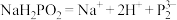 |
D.红磷和白磷, 和 和 互为同素异形体 互为同素异形体 |
您最近一年使用:0次
2023-10-10更新
|
276次组卷
|
2卷引用:四川省成都市第七中学2023-2024学年高一上学期10月月考化学试题
解题方法
9 . 从微观角度认识物质是掌握物质性质的途径之一、下列有关说法不正确的是
| A.乙烯的分子式:C2H4 | B.乙酸中含有的官能团:-COOH |
C.甲烷分子的空间填充模型: | D.蔗糖、果糖的分子式均为:C12H22O11 |
您最近一年使用:0次
名校
解题方法
10 . 卤族元素相关物质在生产、生活中应用广泛。回答下列问题:
(1) 的离子结构示意图为
的离子结构示意图为______ 。
(2)卤素单质有着相似的化学性质,但同时也有差别。比如 与NaOH反应生成NaCl、NaClO和水,而
与NaOH反应生成NaCl、NaClO和水,而 与NaOH发生如下反应:
与NaOH发生如下反应: 。其中
。其中 的电子式为
的电子式为______ ,用电子式描述NaF的形成过程:______ 。
(3)根据卤族元素性质的相似性和递变性,推测元素砹(At)的单质为有色固体,HAt的稳定性______ (填“大于”或“小于”)HI的稳定性,AgAt______ (填“易”或“难”)溶于水。
(4)不同卤素原子之间以共价键相结合形成的化合物称为卤素互化物,如 等。它们与卤素单质性质相似。
等。它们与卤素单质性质相似。
① 与水反应的产物可能为
与水反应的产物可能为______ (填化学式)。
②下列说法不正确的是______ 。
A.HF、HCl、HBr的沸点依次升高
B. 沸点依次升高
沸点依次升高
C.已知离子半径大小会影响离子键的强弱,从而影响物质的熔点:若离子半径越大,离子键越弱。据此推测NaF、NaCl、NaBr熔点依次降低
D. (X代表F、Cl、Br)的酸性随着X的原子序数递增逐渐减弱
(X代表F、Cl、Br)的酸性随着X的原子序数递增逐渐减弱
(1)
 的离子结构示意图为
的离子结构示意图为(2)卤素单质有着相似的化学性质,但同时也有差别。比如
 与NaOH反应生成NaCl、NaClO和水,而
与NaOH反应生成NaCl、NaClO和水,而 与NaOH发生如下反应:
与NaOH发生如下反应: 。其中
。其中 的电子式为
的电子式为(3)根据卤族元素性质的相似性和递变性,推测元素砹(At)的单质为有色固体,HAt的稳定性
(4)不同卤素原子之间以共价键相结合形成的化合物称为卤素互化物,如
 等。它们与卤素单质性质相似。
等。它们与卤素单质性质相似。①
 与水反应的产物可能为
与水反应的产物可能为②下列说法不正确的是
A.HF、HCl、HBr的沸点依次升高
B.
 沸点依次升高
沸点依次升高C.已知离子半径大小会影响离子键的强弱,从而影响物质的熔点:若离子半径越大,离子键越弱。据此推测NaF、NaCl、NaBr熔点依次降低
D.
 (X代表F、Cl、Br)的酸性随着X的原子序数递增逐渐减弱
(X代表F、Cl、Br)的酸性随着X的原子序数递增逐渐减弱
您最近一年使用:0次
2024-04-04更新
|
201次组卷
|
2卷引用:重庆市巴蜀中学校2023-2024学年高一下学期3月月考化学试题



