名校
解题方法
1 . 画出硒的原子结构示意图为___________ 。
您最近一年使用:0次
2 . 氮气的结构式___________ ,铵根离子的电子式___________ 。
您最近一年使用:0次
名校
解题方法
3 . 研究发现,一种新型储氢材料(C16S8)其结构如图所示,每个平面上下最多可吸附10个 分子。
分子。___________ 。
(2)用电子式表示硫元素气态氢化物的形成过程___________ 。
(3)构成该新型储氢材料的基本微粒是___________ 。
(4) 中C—S键的共用电子对偏向
中C—S键的共用电子对偏向___________ 。
A.C原子 B.S原子
 分子。
分子。
(2)用电子式表示硫元素气态氢化物的形成过程
(3)构成该新型储氢材料的基本微粒是
(4)
 中C—S键的共用电子对偏向
中C—S键的共用电子对偏向A.C原子 B.S原子
您最近一年使用:0次
4 . 填空
(1)化学用语是学习化学的重要工具,是国际通用的化学语言,请用化学用语填空:
①高锰酸钾中锰元素的化合价_____ ;②5个氖原子_____ ;③甲烷_____ ;④3个硝酸根离子_____ 。
(2)写出“3 ”中数字及符号的含义: “3”表示:
”中数字及符号的含义: “3”表示:_____ ;“2”表示:_____ 。
(1)化学用语是学习化学的重要工具,是国际通用的化学语言,请用化学用语填空:
①高锰酸钾中锰元素的化合价
(2)写出“3
 ”中数字及符号的含义: “3”表示:
”中数字及符号的含义: “3”表示:
您最近一年使用:0次
名校
解题方法
5 . 卤族元素相关物质在生产、生活中应用广泛。回答下列问题:
(1) 的离子结构示意图为
的离子结构示意图为______ 。
(2)卤素单质有着相似的化学性质,但同时也有差别。比如 与NaOH反应生成NaCl、NaClO和水,而
与NaOH反应生成NaCl、NaClO和水,而 与NaOH发生如下反应:
与NaOH发生如下反应: 。其中
。其中 的电子式为
的电子式为______ ,用电子式描述NaF的形成过程:______ 。
(3)根据卤族元素性质的相似性和递变性,推测元素砹(At)的单质为有色固体,HAt的稳定性______ (填“大于”或“小于”)HI的稳定性,AgAt______ (填“易”或“难”)溶于水。
(4)不同卤素原子之间以共价键相结合形成的化合物称为卤素互化物,如 等。它们与卤素单质性质相似。
等。它们与卤素单质性质相似。
① 与水反应的产物可能为
与水反应的产物可能为______ (填化学式)。
②下列说法不正确的是______ 。
A.HF、HCl、HBr的沸点依次升高
B. 沸点依次升高
沸点依次升高
C.已知离子半径大小会影响离子键的强弱,从而影响物质的熔点:若离子半径越大,离子键越弱。据此推测NaF、NaCl、NaBr熔点依次降低
D. (X代表F、Cl、Br)的酸性随着X的原子序数递增逐渐减弱
(X代表F、Cl、Br)的酸性随着X的原子序数递增逐渐减弱
(1)
 的离子结构示意图为
的离子结构示意图为(2)卤素单质有着相似的化学性质,但同时也有差别。比如
 与NaOH反应生成NaCl、NaClO和水,而
与NaOH反应生成NaCl、NaClO和水,而 与NaOH发生如下反应:
与NaOH发生如下反应: 。其中
。其中 的电子式为
的电子式为(3)根据卤族元素性质的相似性和递变性,推测元素砹(At)的单质为有色固体,HAt的稳定性
(4)不同卤素原子之间以共价键相结合形成的化合物称为卤素互化物,如
 等。它们与卤素单质性质相似。
等。它们与卤素单质性质相似。①
 与水反应的产物可能为
与水反应的产物可能为②下列说法不正确的是
A.HF、HCl、HBr的沸点依次升高
B.
 沸点依次升高
沸点依次升高C.已知离子半径大小会影响离子键的强弱,从而影响物质的熔点:若离子半径越大,离子键越弱。据此推测NaF、NaCl、NaBr熔点依次降低
D.
 (X代表F、Cl、Br)的酸性随着X的原子序数递增逐渐减弱
(X代表F、Cl、Br)的酸性随着X的原子序数递增逐渐减弱
您最近一年使用:0次
2024-04-04更新
|
191次组卷
|
2卷引用:重庆市巴蜀中学校2023-2024学年高一下学期3月月考化学试题
名校
6 . 按要求回答下列问题:
(1)写出漂白粉的有效成分的化学式_______ 。
(2)写出CaCl2的电子式_______ 。
(3)写出CO2的结构式_______ 。
(4)写出红热的铁与水蒸气反应的化学方程式_______ 。
(1)写出漂白粉的有效成分的化学式
(2)写出CaCl2的电子式
(3)写出CO2的结构式
(4)写出红热的铁与水蒸气反应的化学方程式
您最近一年使用:0次
名校
解题方法
7 . 请用化学用语(化学方程式或离子方程式或电子式等)解释以下事实:
(1)NaCl固体溶于水可导电_______ 。
(2)工业酸性废水中含有的重铬酸根离子(Cr2O )有毒,可用硫酸亚铁转化成无毒的Cr3+处理达标后安全排放(离子方程式)
)有毒,可用硫酸亚铁转化成无毒的Cr3+处理达标后安全排放(离子方程式)________ 。
(3)钠与水剧烈反应(离子方程式)________ 。
(4)过氧化钠可做潜水艇氧气来源_______ 。
(5)实验室常用舎勒的方法制备氯气________ 。
(6)氯气溶于水能杀菌消毒(离子方程式)________ 。
(7)工业上将Cl2转化成更易保存的漂白粉________ 。
(8)炽热的铁水或钢水注入模具之前,模具必须进行充分的干燥处理_______ 。
(9)工业上用FeCl3溶液刻蚀覆铜板(离子方程式)________ 。
(10)由Na和Cl形成离子键的过程:________ 。
(1)NaCl固体溶于水可导电
(2)工业酸性废水中含有的重铬酸根离子(Cr2O
 )有毒,可用硫酸亚铁转化成无毒的Cr3+处理达标后安全排放(离子方程式)
)有毒,可用硫酸亚铁转化成无毒的Cr3+处理达标后安全排放(离子方程式)(3)钠与水剧烈反应(离子方程式)
(4)过氧化钠可做潜水艇氧气来源
(5)实验室常用舎勒的方法制备氯气
(6)氯气溶于水能杀菌消毒(离子方程式)
(7)工业上将Cl2转化成更易保存的漂白粉
(8)炽热的铁水或钢水注入模具之前,模具必须进行充分的干燥处理
(9)工业上用FeCl3溶液刻蚀覆铜板(离子方程式)
(10)由Na和Cl形成离子键的过程:
您最近一年使用:0次
解题方法
8 . 人体必需的一些元素在周期表中的分布情况如下:
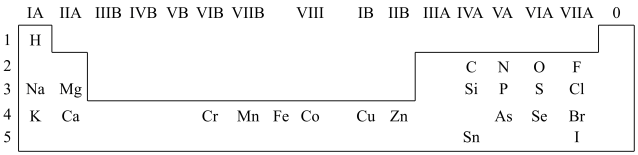
(1)请在上图中画出金属与非金属的分界线______ 。
(2)Na与O形成的原子个数比为1:1的化合物所含的化学键类型为______ 。
(3)锡(Sn)与C为同一主族元素,Sn原子比C原子多三个电子层,则Sn的原子序数为______ 。
(4)X射线衍射法可以测定某些分子的结构,下列分子结构模型中正确是______ (填字母)。
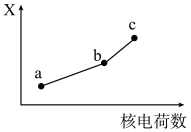
(5)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是______(填字母)。
(6)某小组为探究 、
、 、
、 的氧化性强弱,设计实验如下:
的氧化性强弱,设计实验如下:
资料:稀溴水呈黄色;浓溴水呈红棕色;碘水呈棕黄色。
实验②观察到的现象是______ ,甲同学根据此现象得出结论:氧化性 。乙同学认为实验②不能充分证明氧化性
。乙同学认为实验②不能充分证明氧化性 ,其理由是
,其理由是______ 。试从原子结构的角度解释卤素单质的氧化性递变规律:同一主族元素从上到下,______ ,因此,元素的非金属性逐渐减弱,对应的单质的氧化性逐渐减弱。

(1)请在上图中画出金属与非金属的分界线
(2)Na与O形成的原子个数比为1:1的化合物所含的化学键类型为
(3)锡(Sn)与C为同一主族元素,Sn原子比C原子多三个电子层,则Sn的原子序数为
(4)X射线衍射法可以测定某些分子的结构,下列分子结构模型中正确是
| A | B | C | D |
| HCl | H₂O | CO₂ | CH₄ |
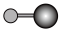 | 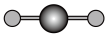 | 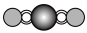 | 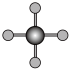 |
| 直线形 | 直线形 | 直线形 | 平面正方形 |
(5)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是______(填字母)。

| A.若a、b、c表示碱金属元素,则X表示对应单质的密度 |
| B.若a、b、c表示卤族元素,则X表示对应简单离子的还原性 |
| C.若a、b、c表示第ⅥA族元素,则X表示对应氢化物的稳定性 |
| D.若a、b、c表示第ⅡA族元素,则X表示最高价氧化物对应水化物的碱性 |
(6)某小组为探究
 、
、 、
、 的氧化性强弱,设计实验如下:
的氧化性强弱,设计实验如下:资料:稀溴水呈黄色;浓溴水呈红棕色;碘水呈棕黄色。
| 序号 | 实验① | 实验② |
| 实验操作 |  |  |
| 现象 | 溶液变为黄色 |
 。乙同学认为实验②不能充分证明氧化性
。乙同学认为实验②不能充分证明氧化性 ,其理由是
,其理由是
您最近一年使用:0次
解题方法
9 . 写出下列物质的化学式 :
硝酸钡___________ ;硫酸铝___________ ;硫酸钠___________ ;氢氧化铜___________ ;碳酸钙___________ ;氯化铵___________ 。
硝酸钡
您最近一年使用:0次
名校
10 . 回答下列问题
(1)用化学符号表示:
钙元素___________ ,两个硫原子___________ ,一个钠离子___________ ,氢氧化钾___________ ,硝酸银___________ ,铵根离子 ___________ 。
(2)标出下列物质化学式中加点元素的化合价?
H2S _____ ;P 2O5_____ ;CaC O3______ ;Na2O 2______ ;H 2______ ;HN O3______ ;
(1)用化学符号表示:
钙元素
(2)标出下列物质化学式中加点元素的化合价?
H2
您最近一年使用:0次



