名校
1 . 短周期主族元素W、X、Y、Z的原子序数依次增大已知几种元素的性质或原子结构的相关叙述如表所示,回答下列问题。
(1)元素X的一种同位素可用来测定文物所属年代,这种同位素的原子符号是_______ 。
(2)Y形成的一种单质,主要存在于地球的平流层中,被称作地球生物的保护伞,该单质的化学式是_______ 。
(3)画出Z的原子结构示意图:_______ 。
(4)比较Y、Z简单离子的半径大小_______ 。
(5)由X元素组成的单质在Y元素组成的常见单质中完全燃烧,生成的产物用足量的氢氧化钠溶液吸收,反应的离子程式为_______ 。
(6)Z元素在元素周期表中的位置是:_______ ,其与Y组成的种二元化合物可以与水反应产生氧气,因此该化合物常用作供氧剂,该化合物与水反应的化学方程式为_______ ,常温常压反应产生气体32g时,转移电子数是_______ (阿伏伽德罗常数的值为NA)。
| 元素编号 | 元素性质或原子结构的相关叙述 |
| W | 单质是密度最小的气体 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 地球含量最高的元素 |
| Z | 单质与氯气化合的产物是厨房的调味剂 |
(2)Y形成的一种单质,主要存在于地球的平流层中,被称作地球生物的保护伞,该单质的化学式是
(3)画出Z的原子结构示意图:
(4)比较Y、Z简单离子的半径大小
(5)由X元素组成的单质在Y元素组成的常见单质中完全燃烧,生成的产物用足量的氢氧化钠溶液吸收,反应的离子程式为
(6)Z元素在元素周期表中的位置是:
您最近一年使用:0次
名校
解题方法
2 . 吸食“冰毒”会严重破坏人的生理和免疫功能,冰毒的主要成分是甲基苯丙胺(C10H15N)。下列关于甲基苯丙胺的说法正确的是
| A.甲基苯丙胺含26个原子 | B.甲基苯丙胺中碳元素的质量分数为80% |
| C.甲基苯丙胺由碳、氢、氮三种元素组成 | D.甲基苯丙胺中各元素的质量比为10:15:1 |
您最近一年使用:0次
名校
3 . 用化学用语填空:空气中含量最多的气体是___________ ;地壳中含量最多的金属元素与人体中含量最多的非金属元素形成化合物的化学式为___________ 。保持水化学性质的最小粒子是___________ 。
您最近一年使用:0次
解题方法
4 . 化学用语是学习化学的基本工具,请用化学用语填空:
(1)相对分子质量最小的氧化物的化学式是_______ 。
(2)地壳中含量居前两位的元素所形成化合物的化学式为_______ 。
(3)氯化钠是由_______ 和_______ 构成;
(4)标出氧化钙中钙元素的化合价_______ 。
(5)写出硝酸钾的化学式_______ 。
(1)相对分子质量最小的氧化物的化学式是
(2)地壳中含量居前两位的元素所形成化合物的化学式为
(3)氯化钠是由
(4)标出氧化钙中钙元素的化合价
(5)写出硝酸钾的化学式
您最近一年使用:0次
解题方法
5 . 镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知镍镉电池的电池总反应为: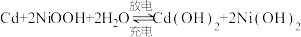 ,利用废旧镍镉电池回收铬的流程如下:
,利用废旧镍镉电池回收铬的流程如下:
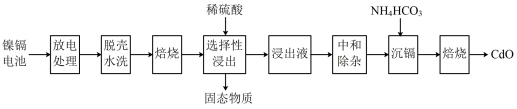
已知:中和除杂后的溶液中主要含有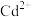 、
、 、
、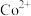 。
。
回答下列问题:
(1)NiOOH中,Ni的化合价为:______ 。
(2)写出“焙烧”过程中含镍物质变化的化学反应方程式:______ 。
(3)在“选择性浸出”一步中,40℃时,不同的金属氧化物在稀 中2小时后的浸出率随PH的变化如下图1所示,则:
中2小时后的浸出率随PH的变化如下图1所示,则:

①“选择性浸出”时,最适宜的pH为______ (填选项字母),写出在此pH下发生的主要离子方程式:______ 。
A.5 B.4 C.3 D.2
②浸出液中各元素含量如表1所示。Co的浓度比镍还小的原因可能是:______ 。
表1 浸出液组成
(4)沉铬时生成 的离子反应方程式:
的离子反应方程式:______ 。
(5)镍铬电池充电时, 移向
移向______ (填“明极”或“阳极”),写出阳极的电极反应式:______ 。
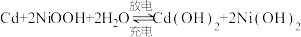 ,利用废旧镍镉电池回收铬的流程如下:
,利用废旧镍镉电池回收铬的流程如下:
已知:中和除杂后的溶液中主要含有
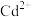 、
、 、
、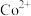 。
。回答下列问题:
(1)NiOOH中,Ni的化合价为:
(2)写出“焙烧”过程中含镍物质变化的化学反应方程式:
(3)在“选择性浸出”一步中,40℃时,不同的金属氧化物在稀
 中2小时后的浸出率随PH的变化如下图1所示,则:
中2小时后的浸出率随PH的变化如下图1所示,则:
①“选择性浸出”时,最适宜的pH为
A.5 B.4 C.3 D.2
②浸出液中各元素含量如表1所示。Co的浓度比镍还小的原因可能是:
| 元素Elements | Cd | Ni | Co | Fe |
浓度(Concentrations/( ) ) | 77.5 | 2.61 | 0.406 | 0.176 |
表1 浸出液组成
(4)沉铬时生成
 的离子反应方程式:
的离子反应方程式:(5)镍铬电池充电时,
 移向
移向
您最近一年使用:0次
2022-08-18更新
|
155次组卷
|
2卷引用:贵州省遵义市新高考协作体2022-2023学年高三上学期入学质量检测理综化学试题
名校
解题方法
6 . 化学用语是化学学科的国际通用语言,是学习化学的重要工具。请你使用化学用语完成下列填空:
(1)铝、铁、铜是重要的金属资源,广泛的应用于生产生活。请写出世界上这三种金属的年产量从高到低的排列顺序:____ 。
(2)熔点最低的金属是____ ;在树木上涂刷含有____ (淡黄色粉末)等的石灰浆,可以保护树木,防止冻伤,并防止害虫生卵。
(3)赤铁矿、磁铁矿的主要成分分别是:____ 、____ 。
(4)地壳中含量最多的金属元素和地壳中含量最多的元素组成化合物的化学式____ 。
(5)请写出溶洞中石灰岩遇到溶有CO2的水时,生成溶解性较大的碳酸氢钙的化学方程式:____ 。
(1)铝、铁、铜是重要的金属资源,广泛的应用于生产生活。请写出世界上这三种金属的年产量从高到低的排列顺序:
(2)熔点最低的金属是
(3)赤铁矿、磁铁矿的主要成分分别是:
(4)地壳中含量最多的金属元素和地壳中含量最多的元素组成化合物的化学式
(5)请写出溶洞中石灰岩遇到溶有CO2的水时,生成溶解性较大的碳酸氢钙的化学方程式:
您最近一年使用:0次
7 . 顺式Pt(NH3)2Cl2(相对分子质量为300)是临床广泛使用的抗肿瘤药物。下列有关该物质的说法中正确的是( )
| A.由4种元素组成 | B.该物质由NH3和PtCl2组成,属于混合物 |
| C.Pt的化合价为+4价 | D.铂元素的质量分数为75% |
您最近一年使用:0次
2020-11-13更新
|
103次组卷
|
2卷引用:山西省太原市十二中学2020-2021学年高一上学期10月月考化学试题
8 . 下列化学用语和描述均正确的是
A.空气中电子式为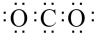 的分子含量过多会造成温室效应 的分子含量过多会造成温室效应 |
B. 原子价电子轨道表示式 原子价电子轨道表示式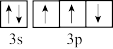 |
C.比例模型为 的分子可发生加成反应 的分子可发生加成反应 |
D.核内质子数为117,核内中子数为174的核素 可表示为: 可表示为: |
您最近一年使用:0次
名校
9 . 我国神舟十三号载人飞船中,宇航员要呼出 ,为使返回舱内
,为使返回舱内 浓度降低,同时保持舱内
浓度降低,同时保持舱内 含量相对稳定,要在返回舱内放入过氧化钠,其反应为:
含量相对稳定,要在返回舱内放入过氧化钠,其反应为: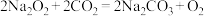 。下列有关说法正确的是
。下列有关说法正确的是
 ,为使返回舱内
,为使返回舱内 浓度降低,同时保持舱内
浓度降低,同时保持舱内 含量相对稳定,要在返回舱内放入过氧化钠,其反应为:
含量相对稳定,要在返回舱内放入过氧化钠,其反应为: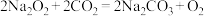 。下列有关说法正确的是
。下列有关说法正确的是| A.钠元素位于周期表中第二周期第ⅣA族 | B. 的结构示意图: 的结构示意图: |
C. 的结构式为 的结构式为 | D. 的电子式为 的电子式为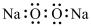 |
您最近一年使用:0次
2022-01-24更新
|
208次组卷
|
2卷引用:重庆市2021-2022学年高一上学期期末联合检测化学试题
10 . 工业上利用氧化铝基废催化剂(主要成分为Al2O3,少量Pd)回收Al2(SO4)3及Pd 流程如图:

说明:上述流程中焙烧温度不宜过高,否则会导致硫酸铵固体的分解。
(1)焙烧时产生气体X的结构式为________ 。
(2)水浸分离中,滤渣Pd的颗粒比较大,一般可以采用的分离方法是_________ (填字母)
A.过滤 B.抽滤 C.倾析 D.渗析
(3)写出酸浸时发生反应的离子方式______ (已知氯钯酸为弱酸)
(4)某同学在实验室用如下图所示装置完成Pd的热还原实验,并计算滤渣中 (NH4)2PdCl6的百分含量(滤渣中的杂质不参与热还原反应)。

①写出热还原法过程中发生反应的化学方程式________ 。
②i.将石英玻璃管中(带开关;K1和K2)(设为装置A )称重,记为mi g。将滤渣 [(NH4)2PdCl6]装入石英玻璃管中,再次将装置A称重,记为m2 g。
ii.连接好装置后,按d→ → →b→ →e(填标号)顺序进行实验。_______
a.关闭K1和K2 b.熄灭酒精灯 c.点燃酒精灯,加热
d.打开K1和K2 e.称量A f.缓缓通入H2 g.冷却至室温
iii.重复上述操作步骤,直至A恒重,记为m3g。
③根据实验记录,计算滤渣中(NH4)2PdCl6的百分含量__________ [列式表示,其中(NH4)2PdCl6相对分子质量为355]。
④实验结束时,发现硬质试管右端有少量白色固体,可能是____ (填化学式),这种情况导致实验结果_________ (填“偏高”、“偏低”、“无影响”)

说明:上述流程中焙烧温度不宜过高,否则会导致硫酸铵固体的分解。
(1)焙烧时产生气体X的结构式为
(2)水浸分离中,滤渣Pd的颗粒比较大,一般可以采用的分离方法是
A.过滤 B.抽滤 C.倾析 D.渗析
(3)写出酸浸时发生反应的离子方式
(4)某同学在实验室用如下图所示装置完成Pd的热还原实验,并计算滤渣中 (NH4)2PdCl6的百分含量(滤渣中的杂质不参与热还原反应)。

①写出热还原法过程中发生反应的化学方程式
②i.将石英玻璃管中(带开关;K1和K2)(设为装置A )称重,记为mi g。将滤渣 [(NH4)2PdCl6]装入石英玻璃管中,再次将装置A称重,记为m2 g。
ii.连接好装置后,按d→ → →b→ →e(填标号)顺序进行实验。
a.关闭K1和K2 b.熄灭酒精灯 c.点燃酒精灯,加热
d.打开K1和K2 e.称量A f.缓缓通入H2 g.冷却至室温
iii.重复上述操作步骤,直至A恒重,记为m3g。
③根据实验记录,计算滤渣中(NH4)2PdCl6的百分含量
④实验结束时,发现硬质试管右端有少量白色固体,可能是
您最近一年使用:0次
2020-01-01更新
|
501次组卷
|
2卷引用:2019年湖南省郴州市高三第一次教学质量监测化学试题



