解题方法
1 . 化学用语是学习化学的基本工具,请用化学用语填空:
(1)相对分子质量最小的氧化物的化学式是_______ 。
(2)地壳中含量居前两位的元素所形成化合物的化学式为_______ 。
(3)氯化钠是由_______ 和_______ 构成;
(4)标出氧化钙中钙元素的化合价_______ 。
(5)写出硝酸钾的化学式_______ 。
(1)相对分子质量最小的氧化物的化学式是
(2)地壳中含量居前两位的元素所形成化合物的化学式为
(3)氯化钠是由
(4)标出氧化钙中钙元素的化合价
(5)写出硝酸钾的化学式
您最近一年使用:0次
解题方法
2 . 镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知镍镉电池的电池总反应为: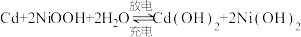 ,利用废旧镍镉电池回收铬的流程如下:
,利用废旧镍镉电池回收铬的流程如下:
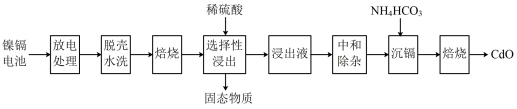
已知:中和除杂后的溶液中主要含有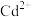 、
、 、
、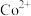 。
。
回答下列问题:
(1)NiOOH中,Ni的化合价为:______ 。
(2)写出“焙烧”过程中含镍物质变化的化学反应方程式:______ 。
(3)在“选择性浸出”一步中,40℃时,不同的金属氧化物在稀 中2小时后的浸出率随PH的变化如下图1所示,则:
中2小时后的浸出率随PH的变化如下图1所示,则:

①“选择性浸出”时,最适宜的pH为______ (填选项字母),写出在此pH下发生的主要离子方程式:______ 。
A.5 B.4 C.3 D.2
②浸出液中各元素含量如表1所示。Co的浓度比镍还小的原因可能是:______ 。
表1 浸出液组成
(4)沉铬时生成 的离子反应方程式:
的离子反应方程式:______ 。
(5)镍铬电池充电时, 移向
移向______ (填“明极”或“阳极”),写出阳极的电极反应式:______ 。
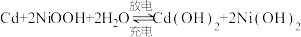 ,利用废旧镍镉电池回收铬的流程如下:
,利用废旧镍镉电池回收铬的流程如下:
已知:中和除杂后的溶液中主要含有
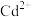 、
、 、
、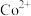 。
。回答下列问题:
(1)NiOOH中,Ni的化合价为:
(2)写出“焙烧”过程中含镍物质变化的化学反应方程式:
(3)在“选择性浸出”一步中,40℃时,不同的金属氧化物在稀
 中2小时后的浸出率随PH的变化如下图1所示,则:
中2小时后的浸出率随PH的变化如下图1所示,则:
①“选择性浸出”时,最适宜的pH为
A.5 B.4 C.3 D.2
②浸出液中各元素含量如表1所示。Co的浓度比镍还小的原因可能是:
| 元素Elements | Cd | Ni | Co | Fe |
浓度(Concentrations/( ) ) | 77.5 | 2.61 | 0.406 | 0.176 |
表1 浸出液组成
(4)沉铬时生成
 的离子反应方程式:
的离子反应方程式:(5)镍铬电池充电时,
 移向
移向
您最近一年使用:0次
2022-08-18更新
|
155次组卷
|
2卷引用:贵州省遵义市新高考协作体2022-2023学年高三上学期入学质量检测理综化学试题
名校
解题方法
3 . 化学用语是化学学科的国际通用语言,是学习化学的重要工具。请你使用化学用语完成下列填空:
(1)铝、铁、铜是重要的金属资源,广泛的应用于生产生活。请写出世界上这三种金属的年产量从高到低的排列顺序:____ 。
(2)熔点最低的金属是____ ;在树木上涂刷含有____ (淡黄色粉末)等的石灰浆,可以保护树木,防止冻伤,并防止害虫生卵。
(3)赤铁矿、磁铁矿的主要成分分别是:____ 、____ 。
(4)地壳中含量最多的金属元素和地壳中含量最多的元素组成化合物的化学式____ 。
(5)请写出溶洞中石灰岩遇到溶有CO2的水时,生成溶解性较大的碳酸氢钙的化学方程式:____ 。
(1)铝、铁、铜是重要的金属资源,广泛的应用于生产生活。请写出世界上这三种金属的年产量从高到低的排列顺序:
(2)熔点最低的金属是
(3)赤铁矿、磁铁矿的主要成分分别是:
(4)地壳中含量最多的金属元素和地壳中含量最多的元素组成化合物的化学式
(5)请写出溶洞中石灰岩遇到溶有CO2的水时,生成溶解性较大的碳酸氢钙的化学方程式:
您最近一年使用:0次
解题方法
4 . 砷的化合物可用于半导体领域,如我国“天宫”空间站的核心舱“天和号”就是采用砷化镓薄膜电池来供电。一种从酸性高浓度含砷废水[砷主要以亚砷酸( )形式存在]中回收砷的工艺流程如下:
)形式存在]中回收砷的工艺流程如下:
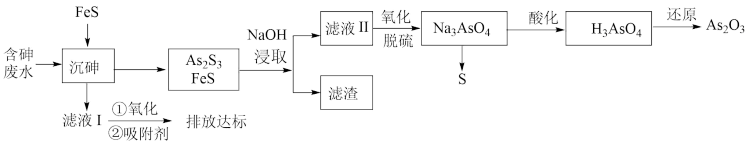
已知:
Ⅰ.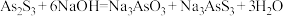
Ⅱ.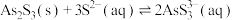
Ⅲ.砷酸( )在酸性条件下有强氧化性,能被
)在酸性条件下有强氧化性,能被 、氢碘酸等还原
、氢碘酸等还原
(1) 中砷元素的化合价为
中砷元素的化合价为___________ 价。
(2)“沉砷”过程中FeS是否可以用过量的 替换
替换___________ (填“是”或“否”);请从平衡移动的角度解释原因:___________ 。
(3)向滤液Ⅱ中通入氧气进行“氧化脱硫”,请写出脱硫的离子反应方程式___________ 。
(4)用 “还原”过程中,若需检验还原后溶液中是否仍存在砷酸。则还需要的实验试剂有
“还原”过程中,若需检验还原后溶液中是否仍存在砷酸。则还需要的实验试剂有___________ 。
(5)已知:常温下,pH>7.1时,吸附剂表面带负电,pH越大,吸附剂表面带的负电荷越多;pH<7.1时,吸附剂表面带正电,pH越小,吸附剂表面带的正电荷越多。
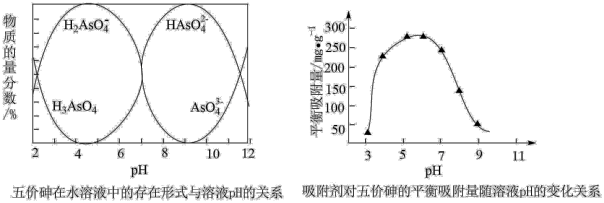
当溶液pH介于7~9,吸附剂对五价砷的平衡吸附量随pH的升高而下降,试分析其原因_____ 。
(6)含砷废水也可采用另一种化学沉降法处理:向废水中先加入适量氧化剂,再加入生石灰调节pH,将砷元素转化为 沉淀。若沉降后上层清液中
沉淀。若沉降后上层清液中 为
为 mol/L,则溶液中
mol/L,则溶液中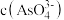 的浓度为
的浓度为_____ mol/L。该处理后的溶液是否符合国家排放标准___________ (填“是”或“否”)。(已知: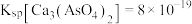 ,国家规定工业废水排放中砷元素含量<0.5mg/L)
,国家规定工业废水排放中砷元素含量<0.5mg/L)
 )形式存在]中回收砷的工艺流程如下:
)形式存在]中回收砷的工艺流程如下:
已知:
Ⅰ.
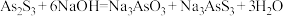
Ⅱ.
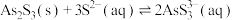
Ⅲ.砷酸(
 )在酸性条件下有强氧化性,能被
)在酸性条件下有强氧化性,能被 、氢碘酸等还原
、氢碘酸等还原(1)
 中砷元素的化合价为
中砷元素的化合价为(2)“沉砷”过程中FeS是否可以用过量的
 替换
替换(3)向滤液Ⅱ中通入氧气进行“氧化脱硫”,请写出脱硫的离子反应方程式
(4)用
 “还原”过程中,若需检验还原后溶液中是否仍存在砷酸。则还需要的实验试剂有
“还原”过程中,若需检验还原后溶液中是否仍存在砷酸。则还需要的实验试剂有(5)已知:常温下,pH>7.1时,吸附剂表面带负电,pH越大,吸附剂表面带的负电荷越多;pH<7.1时,吸附剂表面带正电,pH越小,吸附剂表面带的正电荷越多。

当溶液pH介于7~9,吸附剂对五价砷的平衡吸附量随pH的升高而下降,试分析其原因
(6)含砷废水也可采用另一种化学沉降法处理:向废水中先加入适量氧化剂,再加入生石灰调节pH,将砷元素转化为
 沉淀。若沉降后上层清液中
沉淀。若沉降后上层清液中 为
为 mol/L,则溶液中
mol/L,则溶液中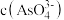 的浓度为
的浓度为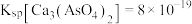 ,国家规定工业废水排放中砷元素含量<0.5mg/L)
,国家规定工业废水排放中砷元素含量<0.5mg/L)
您最近一年使用:0次
名校
5 . 我国神舟十三号载人飞船中,宇航员要呼出 ,为使返回舱内
,为使返回舱内 浓度降低,同时保持舱内
浓度降低,同时保持舱内 含量相对稳定,要在返回舱内放入过氧化钠,其反应为:
含量相对稳定,要在返回舱内放入过氧化钠,其反应为: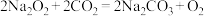 。下列有关说法正确的是
。下列有关说法正确的是
 ,为使返回舱内
,为使返回舱内 浓度降低,同时保持舱内
浓度降低,同时保持舱内 含量相对稳定,要在返回舱内放入过氧化钠,其反应为:
含量相对稳定,要在返回舱内放入过氧化钠,其反应为: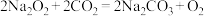 。下列有关说法正确的是
。下列有关说法正确的是| A.钠元素位于周期表中第二周期第ⅣA族 | B. 的结构示意图: 的结构示意图: |
C. 的结构式为 的结构式为 | D. 的电子式为 的电子式为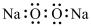 |
您最近一年使用:0次
2022-01-24更新
|
208次组卷
|
2卷引用:重庆市2021-2022学年高一上学期期末联合检测化学试题
6 . 可用“沉淀法”除去粗盐中的 、
、 、
、 杂质。某小组探究沉淀剂添加顺序及过滤方式对产品中硫酸根杂质含量的影响,实验流程及结果如下。
杂质。某小组探究沉淀剂添加顺序及过滤方式对产品中硫酸根杂质含量的影响,实验流程及结果如下。
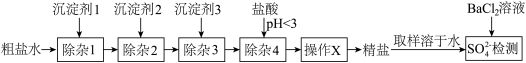
(1)实验1中加入沉淀剂3后会生成_______ (填化学式)。
(2)“除杂4”发生反应的离子方程式有_______ 。
(3)“操作X”为_______ 。
(4)查阅资料:难溶电解质的溶解度会受到溶液中其它离子的影响。加入与难溶电解质相同离子的电解质,因“同离子效应”溶解度降低;加入与难溶电解质不同离子的电解质,因“盐效应”溶解度增大。
①提出假设:
②设计实验:探究不同试剂对硫酸钡溶解度的影响程度
“滤液处理”需用到的试剂有_______ 。
③实验分析:实验3中 溶液的用量为理论值的1.5倍,最后仍检出
溶液的用量为理论值的1.5倍,最后仍检出 的原因是该体系中“同离子效应”
的原因是该体系中“同离子效应”_______ “盐效应”(填“大于”或“小于”)。
④实验结论:粗盐提纯时,为了有效降低产品中 含量,必须
含量,必须_______ 。
 、
、 、
、 杂质。某小组探究沉淀剂添加顺序及过滤方式对产品中硫酸根杂质含量的影响,实验流程及结果如下。
杂质。某小组探究沉淀剂添加顺序及过滤方式对产品中硫酸根杂质含量的影响,实验流程及结果如下。
| 沉淀剂1 | 沉淀剂1 | 沉淀剂1 | 过滤方式 |  检测结果 检测结果 | |
| 实验1 |  溶液 溶液 | NaOH溶液 |  溶液 溶液 | 逐一过滤 | 少量浑浊 |
| 实验2 |  溶液 溶液 |  溶液 溶液 | NaOH溶液 | 逐一过滤 | 少量浑浊 |
| 实验3 | NaOH溶液 |  溶液 溶液 |  溶液 溶液 | 逐一过滤 | 大量沉淀 |
| 实验4 |  溶液 溶液 | NaOH溶液 |  溶液 溶液 | 一起过滤 | 大量沉淀 |
(2)“除杂4”发生反应的离子方程式有
(3)“操作X”为
(4)查阅资料:难溶电解质的溶解度会受到溶液中其它离子的影响。加入与难溶电解质相同离子的电解质,因“同离子效应”溶解度降低;加入与难溶电解质不同离子的电解质,因“盐效应”溶解度增大。
①提出假设:
| 依据 | 假设 | |
| 假设1 | 实验1和2中 检测时出现少量浑浊 检测时出现少量浑浊 |  溶解度 溶解度 |
| 假设2 | 实验3中 检出量明显高于1和2 检出量明显高于1和2 | NaOH能明显增大 溶解度 溶解度 |
| 假设3 | NaOH或 能明显增大 能明显增大 溶解度 溶解度 |
| 探究1 | 探究2 | 探究3 | 探究4 | |
| 实验流程 | 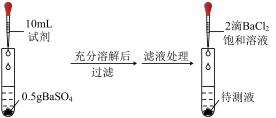 | |||
| 试剂 | 饱和食盐水 | 2 NaOH溶液 NaOH溶液 | 0.5  溶液 溶液 | 蒸馏水 |
| 现象 | 少量浑浊 | 大量沉淀 | 大量沉淀 | 无明显现象 |
③实验分析:实验3中
 溶液的用量为理论值的1.5倍,最后仍检出
溶液的用量为理论值的1.5倍,最后仍检出 的原因是该体系中“同离子效应”
的原因是该体系中“同离子效应”④实验结论:粗盐提纯时,为了有效降低产品中
 含量,必须
含量,必须
您最近一年使用:0次
2022-04-02更新
|
490次组卷
|
2卷引用:福建省八地市(福州、厦门、泉州、莆田、南平、宁德、三明、龙岩)2022届高三毕业班4月诊断性联考化学试题



