名校
1 .  为阿伏伽德罗常数,下列说法中正确的是
为阿伏伽德罗常数,下列说法中正确的是
 为阿伏伽德罗常数,下列说法中正确的是
为阿伏伽德罗常数,下列说法中正确的是A. 与 与 充分反应,当固体增重 充分反应,当固体增重 ,转移电子数为 ,转移电子数为 |
B.向 的 的 溶液中加入 溶液中加入 至溶液呈中性,溶液中醋酸根离子数目为 至溶液呈中性,溶液中醋酸根离子数目为 |
C. 钠与 钠与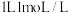 的盐酸反应时,转移电子数为 的盐酸反应时,转移电子数为 |
D.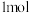 二氧化硅晶体中,所含硅氧键数目为 二氧化硅晶体中,所含硅氧键数目为 |
您最近一年使用:0次
2 . 设NA表示阿伏加德罗常数的值,下列判断正确的是
| A.在常温常压下,48g氧气和臭氧的混合气体含氧原子数是3NA |
| B.标准状况下,22.4LH2O中含有的原子数目为3NA |
| C.1molCl2参加反应转移电子数一定为2NA |
| D.Na2O2与水充分反应生成1molO2时,转移的电子数为4NA |
您最近一年使用:0次
3 . 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.标准状况下,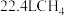 与 与 充分反应,生成的 充分反应,生成的 分子数为 分子数为 |
B. 与 与 的混合气体中含有的质子数为 的混合气体中含有的质子数为 |
C. 正丁烷和 正丁烷和 异丁烷的混合物中共价键数目为 异丁烷的混合物中共价键数目为 |
D.向密闭容器中充入 和 和 ,充分反应时转移电子 ,充分反应时转移电子 |
您最近一年使用:0次
4 . 用NA表示阿伏加德罗常数,下列叙述正确的是
| A.常温常压下,7.8g Na2O2中含有0.3NA个离子 |
| B.0.5mol/L的MgCl2溶液中含有NA个Cl- |
| C.常温常压下, NA个CO2分子占有的体积为22.4L |
| D.标准状况下,O2和O3的混合物共64g,所含氧原子数目为2NA |
您最近一年使用:0次
解题方法
5 . 在标准状况下,实验甲、乙、丙各取30.0mL相同浓度的盐酸,然后分别慢慢加入组成相同的镁铝合金粉末,得下表中有关数据(假设反应前后溶液体积不变)。
下列说法不正确的是
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/mg | 255 | 385 | 459 |
| 气体体积/mL | 280 | 336 | 336 |
| A.实验甲中盐酸过量 |
| B.实验乙中盐酸不足 |
| C.实验中c(HCl)=1.0mol/L |
| D.该镁铝合金粉末中Mg、Al的物质的量之比为2:1 |
您最近一年使用:0次
解题方法
6 . 联合国大会将2019年定为“化学元素周期表国际年”,显示了元素周期表的重要性。下表列出了a~j10种元素在周期表中的位置:
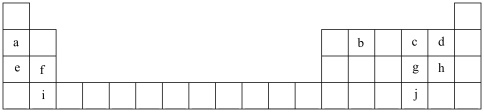
(1)元素a的原子结构示意图为___________ 。
(2)元素b可以形成多种单质,写出其中的两种___________ (填名称)。
(3)元素a~j中非金属性最强的是___________ (填元素符号)。
(4)若e单质着火,可用于灭火的物质是___________(填字母)。
(5)h单质与NaOH溶液反应的离子方程式为___________ 。
(6)元素b、e的最高价氧化物发生反应的化学方程式为___________ 。
(7)3位科学家因在基于a的电池研究方面的成就获得了2019年诺贝尔化学奖。基于e的电池也日益受到重视。下列关于a和e的说法中正确的有___________(填字母)。
(8)NA为阿伏加德罗常数的值,已知ag某气体中含有的分子数为b,则该气体的摩尔质量为___________  。标准状况下,密度为
。标准状况下,密度为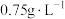 的
的 与
与 组成的混合气体中,
组成的混合气体中, 的体积分数为
的体积分数为___________ 。取均为0.2mol的金属钠、铁、铝,分别投入 盐酸中,产生
盐酸中,产生 的体积(相同状况下)比为
的体积(相同状况下)比为___________ 。

(1)元素a的原子结构示意图为
(2)元素b可以形成多种单质,写出其中的两种
(3)元素a~j中非金属性最强的是
(4)若e单质着火,可用于灭火的物质是___________(填字母)。
| A.自来水 | B. | C.干沙子 | D.湿抹布 |
(5)h单质与NaOH溶液反应的离子方程式为
(6)元素b、e的最高价氧化物发生反应的化学方程式为
(7)3位科学家因在基于a的电池研究方面的成就获得了2019年诺贝尔化学奖。基于e的电池也日益受到重视。下列关于a和e的说法中正确的有___________(填字母)。
| A.a的金属性比e的弱 | B.自然界中,e的储量比a的高 |
| C.a的原子半径比e的大 | D.基于a的电池质量轻、易携带 |
(8)NA为阿伏加德罗常数的值,已知ag某气体中含有的分子数为b,则该气体的摩尔质量为
 。标准状况下,密度为
。标准状况下,密度为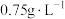 的
的 与
与 组成的混合气体中,
组成的混合气体中, 的体积分数为
的体积分数为 盐酸中,产生
盐酸中,产生 的体积(相同状况下)比为
的体积(相同状况下)比为
您最近一年使用:0次
名校
7 . 完成下列问题:
(1)在元素周期表中,元素Ts跟氯元素位于同一主族。它的一种核素可由核反应 得到,Ts的原子结构示意图可表示为
得到,Ts的原子结构示意图可表示为 ,则m=
,则m=___________ , 的中子数为
的中子数为___________ 。
(2)若用无水 固体配制0.2
固体配制0.2
 溶液250mL,需用托盘天平称取无水
溶液250mL,需用托盘天平称取无水 固体的质量为
固体的质量为___________ g;如果用4mol/L的 溶液稀释配制,需用量筒量取
溶液稀释配制,需用量筒量取___________ mL。
(3)有 、
、 的混合溶液400mL,将其分为两等份,向其中一份中加入1
的混合溶液400mL,将其分为两等份,向其中一份中加入1
 溶液,至恰好不再产生沉淀,消耗50mL,向另一份溶液中加入铁片,充分反应后,取出铁片,洗涤、烘干,称其质量比原来轻0.56g。请计算原溶液中
溶液,至恰好不再产生沉淀,消耗50mL,向另一份溶液中加入铁片,充分反应后,取出铁片,洗涤、烘干,称其质量比原来轻0.56g。请计算原溶液中 的物质的量浓度为
的物质的量浓度为___________  。
。
(4)某硫酸厂使用含杂质25%的黄铁矿(主要成分为 ,杂质中不含硫元素)为原料制取硫酸,在反应过程中有3%的硫元素损失(其余硫元素均可转化为硫酸)。则1吨该黄铁理论上可制取98%的硫酸
,杂质中不含硫元素)为原料制取硫酸,在反应过程中有3%的硫元素损失(其余硫元素均可转化为硫酸)。则1吨该黄铁理论上可制取98%的硫酸___________ 吨?(结果保留三位有效数字)
(1)在元素周期表中,元素Ts跟氯元素位于同一主族。它的一种核素可由核反应
 得到,Ts的原子结构示意图可表示为
得到,Ts的原子结构示意图可表示为 ,则m=
,则m= 的中子数为
的中子数为(2)若用无水
 固体配制0.2
固体配制0.2
 溶液250mL,需用托盘天平称取无水
溶液250mL,需用托盘天平称取无水 固体的质量为
固体的质量为 溶液稀释配制,需用量筒量取
溶液稀释配制,需用量筒量取(3)有
 、
、 的混合溶液400mL,将其分为两等份,向其中一份中加入1
的混合溶液400mL,将其分为两等份,向其中一份中加入1
 溶液,至恰好不再产生沉淀,消耗50mL,向另一份溶液中加入铁片,充分反应后,取出铁片,洗涤、烘干,称其质量比原来轻0.56g。请计算原溶液中
溶液,至恰好不再产生沉淀,消耗50mL,向另一份溶液中加入铁片,充分反应后,取出铁片,洗涤、烘干,称其质量比原来轻0.56g。请计算原溶液中 的物质的量浓度为
的物质的量浓度为 。
。(4)某硫酸厂使用含杂质25%的黄铁矿(主要成分为
 ,杂质中不含硫元素)为原料制取硫酸,在反应过程中有3%的硫元素损失(其余硫元素均可转化为硫酸)。则1吨该黄铁理论上可制取98%的硫酸
,杂质中不含硫元素)为原料制取硫酸,在反应过程中有3%的硫元素损失(其余硫元素均可转化为硫酸)。则1吨该黄铁理论上可制取98%的硫酸
您最近一年使用:0次
名校
8 . 设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.0.5mol/L的NaOH溶液中含有的 数目为0.5 数目为0.5 |
B.1L 1  溶液中含有的钠离子数为2 溶液中含有的钠离子数为2 |
C.通常状况下,1 个 个 分子占有的体积为22.4L 分子占有的体积为22.4L |
D.1mol  与足量 与足量 反应时,转移电子数为2 反应时,转移电子数为2 |
您最近一年使用:0次
9 . 用NA表示阿伏加德罗常数的值,下列说法正确的是
| A.1molN2所含有的原子数为NA |
| B.标准状况下,16gNH3中含有的分子数为NA |
| C.标准状况下,22.4L氯化氢所含的原子数为NA |
| D.500mL1.0mol•L﹣1硫酸钠溶液中所含的钠离子数为NA |
您最近一年使用:0次
名校
10 . 用 表示阿伏加德罗常数的值。下列叙述正确的有
表示阿伏加德罗常数的值。下列叙述正确的有
①78g过氧化钠存在的阴阳离子总数为
②标准状况下,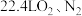 和CO的混合气体中所含有的原子数目为
和CO的混合气体中所含有的原子数目为
③浓度为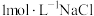 溶液中,阴、阳离子数目之和为
溶液中,阴、阳离子数目之和为
④常温下,2g氦气所含的原子数目为 。
。
⑤ 和
和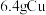 分别与
分别与 充分反应,转移的电子数目均为
充分反应,转移的电子数目均为
⑥ 时,
时,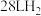 中所含质子的数目为
中所含质子的数目为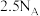
⑦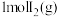 和
和 在密闭容器中充分反应,生成的
在密闭容器中充分反应,生成的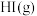 分子数目小于
分子数目小于
 表示阿伏加德罗常数的值。下列叙述正确的有
表示阿伏加德罗常数的值。下列叙述正确的有①78g过氧化钠存在的阴阳离子总数为

②标准状况下,
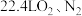 和CO的混合气体中所含有的原子数目为
和CO的混合气体中所含有的原子数目为
③浓度为
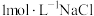 溶液中,阴、阳离子数目之和为
溶液中,阴、阳离子数目之和为
④常温下,2g氦气所含的原子数目为
 。
。⑤
 和
和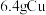 分别与
分别与 充分反应,转移的电子数目均为
充分反应,转移的电子数目均为
⑥
 时,
时,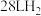 中所含质子的数目为
中所含质子的数目为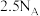
⑦
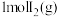 和
和 在密闭容器中充分反应,生成的
在密闭容器中充分反应,生成的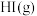 分子数目小于
分子数目小于
| A.1个 | B.2个 | C.3个 | D.4个 |
您最近一年使用:0次
2024-03-28更新
|
128次组卷
|
2卷引用:云南省大理市云南省下关第一中学2023-2024学年高一下学期3月月考化学试题



