11-12高一上·广东·期中
名校
1 . 相等物质的量的CO和CO2相比较,则
①它们所含的分子数目之比为_______________
②它们所含的氧原子数目之比为__________________
③它们所含的原子总数目之比为_______________
④它们所含的C原子数目之比为________________
⑤它们所含的电子数目之比为____________
①它们所含的分子数目之比为
②它们所含的氧原子数目之比为
③它们所含的原子总数目之比为
④它们所含的C原子数目之比为
⑤它们所含的电子数目之比为
您最近一年使用:0次
2016-12-09更新
|
1132次组卷
|
3卷引用:海南省海口市华侨中学2019-2020学年高一(上)期末化学必修一期末复习试卷
海南省海口市华侨中学2019-2020学年高一(上)期末化学必修一期末复习试卷(已下线)2011-2012学年广东省翠园中学高一上学期期中考试化学试卷江西省赣州市大余县梅关中学2023-2024学年高一上学期11月期中化学试题
2014高三·全国·专题练习
解题方法
2 . 铜单质及其化合物是应用极其广泛的物质。
(1)铜是氢后金属,不能与盐酸发生置换反应,但将单质铜置于浓氢碘酸中,会有可燃性气体及白色沉淀生成,又知氧化性:Cu2+>I2,则铜与氢碘酸反应的化学方程式为__________________________________
(2)已知Cu2O能溶于醋酸溶液或盐酸中,同时得到蓝色溶液和红色固体,则Cu2O与稀硫酸反应的离子方程式为____________________________________ ;
Cu2O与稀硝酸反应的离子方程式为_____________________________ ;
只用稀硫酸来确定某红色固体是 Cu2O与Cu组成的混合物的方法:称取m g该红色固体置于足量稀硫酸中,充分反应后过滤,然后___________________ 。
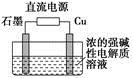
(3)Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解装置如图所示,电解总反应:2Cu+H2O Cu2O+H2↑,则石墨应与电源的
Cu2O+H2↑,则石墨应与电源的________ 极相连,铜电极上的电极反应式为________ ;电解过程中,阴极区周围溶液pH________ (填“变大”、“变小”或“不变”)。
(4)现向Cu、Cu2O、CuO组成的混合物中加入1 L 0.6 mol/L HNO3恰好使混合物溶解,同时收集到2 240 mL NO(标准状况)。若将上述混合物用足量的氢气还原,所得固体的质量为________ ;若混合物中含有0.1 mol Cu,将该混合物与稀硫酸充分反应,至少消耗硫酸的物质的量为________ 。
(1)铜是氢后金属,不能与盐酸发生置换反应,但将单质铜置于浓氢碘酸中,会有可燃性气体及白色沉淀生成,又知氧化性:Cu2+>I2,则铜与氢碘酸反应的化学方程式为
(2)已知Cu2O能溶于醋酸溶液或盐酸中,同时得到蓝色溶液和红色固体,则Cu2O与稀硫酸反应的离子方程式为
Cu2O与稀硝酸反应的离子方程式为
只用稀硫酸来确定某红色固体是 Cu2O与Cu组成的混合物的方法:称取m g该红色固体置于足量稀硫酸中,充分反应后过滤,然后

(3)Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解装置如图所示,电解总反应:2Cu+H2O
 Cu2O+H2↑,则石墨应与电源的
Cu2O+H2↑,则石墨应与电源的(4)现向Cu、Cu2O、CuO组成的混合物中加入1 L 0.6 mol/L HNO3恰好使混合物溶解,同时收集到2 240 mL NO(标准状况)。若将上述混合物用足量的氢气还原,所得固体的质量为
您最近一年使用:0次
2014高三·全国·专题练习
名校
3 . 标准状况下336 L的NH3溶于1 L水中,所得溶液的质量分数为______ ,若该溶液的密度为a g/cm3,则物质的量浓度为______ 。将上述氨水全部转化为NH4Cl,所需4 mol·L-1的盐酸的体积为______ 。
您最近一年使用:0次
4 . 如图所示,两个连通容器用活塞分开,左右两室(体积相同)各充入一定量NO和O2,且恰好使两容器内气体密度相同。打开活塞,使NO与O2充分反应。(不考虑NO2与N2O4的转化)
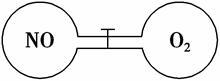
(1)开始时左右两室分子数_________ (填“相同”或“不相同”)。
(2)反应前后NO室压强_________ (填“增大”或“减小”) 。
(3)最终容器内密度与原来_________ (填“相同”或“不相同”)。
(4)最终容器内_________ (填“有”或“无”)O2存在。

(1)开始时左右两室分子数
(2)反应前后NO室压强
(3)最终容器内密度与原来
(4)最终容器内
您最近一年使用:0次



