2024高三·全国·专题练习
解题方法
1 . 向MgCl2和AlCl3的混合溶液中逐滴加入NaOH溶液直至过量。经测定,加入NaOH的物质的量(mol)和所得沉淀的物质的量(mol)的关系如图所示。

(1)写出各段所发生反应的离子方程式:
OD段___________________________________________ ;
DC段___________________________________________ 。
(2)原溶液中Mg2+、Al3+的物质的量浓度之比为__________ 。
(3)图中C点表示当加入__________ molNaOH时,Al3+已经__________ ,Mg2+已经__________ 。
(4)图中OA=_____ mol;AB=_______ mol。

(1)写出各段所发生反应的离子方程式:
OD段
DC段
(2)原溶液中Mg2+、Al3+的物质的量浓度之比为
(3)图中C点表示当加入
(4)图中OA=
您最近一年使用:0次
2024高三·全国·专题练习
2 . 采用热重分析法测定NiSO4·nH2O样品中所含结晶水数。将该样品在900℃下进行煅烧,失重率随时间变化如图所示,A点时失掉3个结晶水,则n值为___________ 。
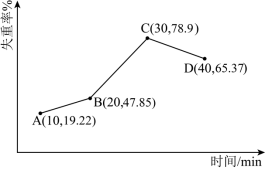

您最近一年使用:0次
2024高三·全国·专题练习
3 . 某铝土矿的主要成分为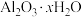 ,还含有
,还含有 和
和 杂质。称取
杂质。称取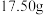 铝土矿样品,加入
铝土矿样品,加入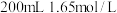 的稀硫酸,恰好完全反应,过滤得沉淀
的稀硫酸,恰好完全反应,过滤得沉淀 ,然后在滤液中加入足量的
,然后在滤液中加入足量的 溶液,得到沉淀
溶液,得到沉淀 。
。
(1)该试样中 的物质的量为
的物质的量为___________ mol。
(2)样品中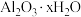 的x=
的x=___________ 。
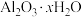 ,还含有
,还含有 和
和 杂质。称取
杂质。称取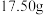 铝土矿样品,加入
铝土矿样品,加入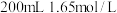 的稀硫酸,恰好完全反应,过滤得沉淀
的稀硫酸,恰好完全反应,过滤得沉淀 ,然后在滤液中加入足量的
,然后在滤液中加入足量的 溶液,得到沉淀
溶液,得到沉淀 。
。(1)该试样中
 的物质的量为
的物质的量为(2)样品中
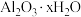 的x=
的x=
您最近一年使用:0次
2024高三·全国·专题练习
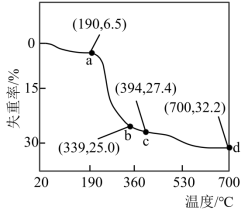
4 . 用热重分析法测定碱式碳酸钴晶体[Co5(CO3)2(OH)6·xH2O]所含结晶水数,将纯净碱式碳酸钴晶体在空气中加热,加热过程中钴元素无损失,失重率与温度的关系如图所示。已知20~190℃为失去结晶水阶段,则 的值为式为
的值为式为___________ ,在 点时剩余固体为氧化物,其化学式为
点时剩余固体为氧化物,其化学式为___________ 。
 的值为式为
的值为式为 点时剩余固体为氧化物,其化学式为
点时剩余固体为氧化物,其化学式为
您最近一年使用:0次
2023高三·全国·专题练习
5 . 从含铜丰富的自然资源黄铜矿(CuFeS2)冶炼铜的工艺流程如下:
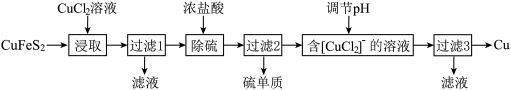
已知:CuFeS2+3CuCl2=4CuCl+FeCl2+2S。过滤3所得滤液中可以循环使用的物质有_______ ,为保持流程持续循环,每生成1molCu,理论上需补充CuCl2的物质的量为_______ 。

已知:CuFeS2+3CuCl2=4CuCl+FeCl2+2S。过滤3所得滤液中可以循环使用的物质有
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
6 . 某工厂用m1 kg铬铁矿粉(含Cr2O3 40%)制备K2Cr2O7,最终得到产品m2 kg,产率为_______ 。
您最近一年使用:0次
2023高三·全国·专题练习
7 . 在一定条件下,有a L O2和O3的混合气体,当其中的O3全部转化为O2时,体积变为1.2a L,求原混合气中O2和O3的质量百分含量_______ 。
您最近一年使用:0次
2023高三·全国·专题练习
8 . 某实验小组以 溶液为原料制备
溶液为原料制备 ,并用重量法测定产品中
,并用重量法测定产品中 的含量。设计了如下实验方案:
的含量。设计了如下实验方案:
步骤2,产品中 的含量测定
的含量测定
①称取产品 ,用
,用 水溶解,酸化,加热至近沸;
水溶解,酸化,加热至近沸;
②在不断搅拌下,向①所得溶液逐滴加入热的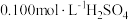 溶液,
溶液,
③沉淀完全后, 水浴40分钟,经过滤、洗涤、烘干等步骤,称量白色固体,质量为
水浴40分钟,经过滤、洗涤、烘干等步骤,称量白色固体,质量为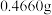 。
。
产品中 的质量分数为
的质量分数为_______ (保留三位有效数字)。
 溶液为原料制备
溶液为原料制备 ,并用重量法测定产品中
,并用重量法测定产品中 的含量。设计了如下实验方案:
的含量。设计了如下实验方案:步骤2,产品中
 的含量测定
的含量测定①称取产品
 ,用
,用 水溶解,酸化,加热至近沸;
水溶解,酸化,加热至近沸;②在不断搅拌下,向①所得溶液逐滴加入热的
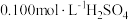 溶液,
溶液,③沉淀完全后,
 水浴40分钟,经过滤、洗涤、烘干等步骤,称量白色固体,质量为
水浴40分钟,经过滤、洗涤、烘干等步骤,称量白色固体,质量为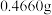 。
。产品中
 的质量分数为
的质量分数为
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
9 . 计算后填空:
(1)在标准状况下,448mL某气体的质量为0.64g,这种气体的相对分子质量为_______ 。
(2)某氯化铁与氯化钠的混合液,已知c(Fe3+)=0.2mol•L-1,c(Cl-)=1mol•L-1。则c(Na+)为________ 。
(3)19g某二价金属的氯化物RCl2中含有0.4molCl-,则R的相对原子质量为_______ 。
(4)如图所示,分别向密闭容器内可移动活塞的两边充入空气(已知空气体积占整个容器容积的 )、H2和O2的混合气体。在标准状况下,若将H2、O2的混合气体点燃引爆,活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央,则原来H2、O2的体积之比可能为
)、H2和O2的混合气体。在标准状况下,若将H2、O2的混合气体点燃引爆,活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央,则原来H2、O2的体积之比可能为________ 。
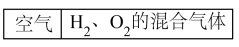
(1)在标准状况下,448mL某气体的质量为0.64g,这种气体的相对分子质量为
(2)某氯化铁与氯化钠的混合液,已知c(Fe3+)=0.2mol•L-1,c(Cl-)=1mol•L-1。则c(Na+)为
(3)19g某二价金属的氯化物RCl2中含有0.4molCl-,则R的相对原子质量为
(4)如图所示,分别向密闭容器内可移动活塞的两边充入空气(已知空气体积占整个容器容积的
 )、H2和O2的混合气体。在标准状况下,若将H2、O2的混合气体点燃引爆,活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央,则原来H2、O2的体积之比可能为
)、H2和O2的混合气体。在标准状况下,若将H2、O2的混合气体点燃引爆,活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央,则原来H2、O2的体积之比可能为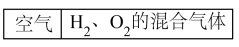
您最近一年使用:0次
名校
解题方法
10 . 请阅读下列资料,获取重要信息点,回答下列问题。
信息I:“物质的量”是一个物理量,表示含有一定数目粒子的集体,符号为n,单位为摩尔 。
。
国际上规定,1mol微粒A所含有的该粒子A的数量为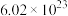 个。例如,
个。例如, 中含有
中含有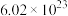 个H2O,含有
个H2O,含有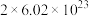 个H。
个H。
信息II:1mol物质B所具有的总质量称为物质B的摩尔质量,符号为M,单位为g/mol。经研究,物质B的摩尔质量在数值上等于物质B的相对原子质量或相对分子质量。 ,即
,即 的质量为44g。
的质量为44g。
信息III:经过大量数据分析,在同温同压下。气体C的体积和气体C的分子数成正比。在0℃和105Pa气压下,1mol任何气体的体积都近似等于22.4L。
信息IV:溶质D的物质的量的浓度,也称摩尔浓度,符号为c,单位是mol/L。可如下描述,在1L水溶液中,所包含溶质D的物质的量,就叫作溶质D的摩尔浓度。
(1)电解完全2mol的水可以得到氧气________ g。
(2)小明查阅资料得知,金属E的密度为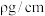 ,金属E晶体为立方体形,在棱长为
,金属E晶体为立方体形,在棱长为 的晶体空间内有E原子b个,则金属E的相对原子质量为
的晶体空间内有E原子b个,则金属E的相对原子质量为________ 。
信息I:“物质的量”是一个物理量,表示含有一定数目粒子的集体,符号为n,单位为摩尔
 。
。国际上规定,1mol微粒A所含有的该粒子A的数量为
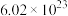 个。例如,
个。例如, 中含有
中含有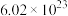 个H2O,含有
个H2O,含有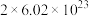 个H。
个H。信息II:1mol物质B所具有的总质量称为物质B的摩尔质量,符号为M,单位为g/mol。经研究,物质B的摩尔质量在数值上等于物质B的相对原子质量或相对分子质量。
 ,即
,即 的质量为44g。
的质量为44g。信息III:经过大量数据分析,在同温同压下。气体C的体积和气体C的分子数成正比。在0℃和105Pa气压下,1mol任何气体的体积都近似等于22.4L。
信息IV:溶质D的物质的量的浓度,也称摩尔浓度,符号为c,单位是mol/L。可如下描述,在1L水溶液中,所包含溶质D的物质的量,就叫作溶质D的摩尔浓度。
(1)电解完全2mol的水可以得到氧气
(2)小明查阅资料得知,金属E的密度为
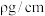 ,金属E晶体为立方体形,在棱长为
,金属E晶体为立方体形,在棱长为 的晶体空间内有E原子b个,则金属E的相对原子质量为
的晶体空间内有E原子b个,则金属E的相对原子质量为
您最近一年使用:0次



