2023高三·全国·专题练习
1 . K-O2电池结构如图所示,a和b为两个电极,其中之一为单质钾片。产生1Ah电量时,生成KO2的质量与消耗O2的质量比值约为___________ 。用此电池为铅酸蓄电池充电,消耗3.9g钾时,铅酸蓄电池消耗___________ g水。


您最近一年使用:0次
2023高三·全国·专题练习
解题方法
2 . 物质的量是高中化学常用的物理量,请完成以下有关计算(设 为阿伏加德罗常数的值):
为阿伏加德罗常数的值):
(1) 乙醇含有
乙醇含有_______ 个H原子,所含共价键的物质的量为_______ ,其中官能团羟基所含的电子数为_______ 。
(2)某条件下, 氧气所占的体积为
氧气所占的体积为 ,则在该条件下的气体摩尔体积为
,则在该条件下的气体摩尔体积为_______ 。
(3)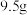 某二价金属的氯化物中含有
某二价金属的氯化物中含有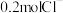 ,则此氯化物的摩尔质量为
,则此氯化物的摩尔质量为_______ 。
(4)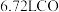 (标准状况)与一定量的
(标准状况)与一定量的 恰好完全反应(生成
恰好完全反应(生成 与
与 )后,生成
)后,生成 的质量为
的质量为_______ g,转移的电子数目为_______ 。
 为阿伏加德罗常数的值):
为阿伏加德罗常数的值):(1)
 乙醇含有
乙醇含有(2)某条件下,
 氧气所占的体积为
氧气所占的体积为 ,则在该条件下的气体摩尔体积为
,则在该条件下的气体摩尔体积为(3)
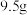 某二价金属的氯化物中含有
某二价金属的氯化物中含有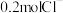 ,则此氯化物的摩尔质量为
,则此氯化物的摩尔质量为(4)
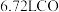 (标准状况)与一定量的
(标准状况)与一定量的 恰好完全反应(生成
恰好完全反应(生成 与
与 )后,生成
)后,生成 的质量为
的质量为
您最近一年使用:0次
解题方法
3 . 铝是中学化学学习阶段的唯一一种既能与酸(非氧化性酸)反应又能与强碱溶液反应放出 的金属,就铝的这一特殊性质,回答下列问题:
的金属,就铝的这一特殊性质,回答下列问题:
(1)等质量的两份铝分别与足量的盐酸、氢氧化钠溶液反应,所得 的体积之比是
的体积之比是___________ 。
(2)足量的两份铝分别投入到等体积、等物质的量浓度的盐酸和氢氧化钠溶液中,产生 的体积之比是
的体积之比是___________ 。
(3)足量的两份铝分别投入到等体积、一定物质的量浓度的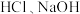 溶液中,二者产生的
溶液中,二者产生的 相等,则
相等,则 和
和 的物质的量浓度之比是
的物质的量浓度之比是___________ 。
(4)甲、乙两烧杯中各盛有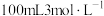 的盐酸和
的盐酸和 溶液,向两烧杯中分别加入等质量的铝粉,反应结束后,测得生成的气体体积比为
溶液,向两烧杯中分别加入等质量的铝粉,反应结束后,测得生成的气体体积比为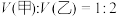 ,则加入铝粉的质量为___________(填字母)。
,则加入铝粉的质量为___________(填字母)。
 的金属,就铝的这一特殊性质,回答下列问题:
的金属,就铝的这一特殊性质,回答下列问题:(1)等质量的两份铝分别与足量的盐酸、氢氧化钠溶液反应,所得
 的体积之比是
的体积之比是(2)足量的两份铝分别投入到等体积、等物质的量浓度的盐酸和氢氧化钠溶液中,产生
 的体积之比是
的体积之比是(3)足量的两份铝分别投入到等体积、一定物质的量浓度的
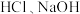 溶液中,二者产生的
溶液中,二者产生的 相等,则
相等,则 和
和 的物质的量浓度之比是
的物质的量浓度之比是(4)甲、乙两烧杯中各盛有
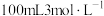 的盐酸和
的盐酸和 溶液,向两烧杯中分别加入等质量的铝粉,反应结束后,测得生成的气体体积比为
溶液,向两烧杯中分别加入等质量的铝粉,反应结束后,测得生成的气体体积比为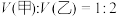 ,则加入铝粉的质量为___________(填字母)。
,则加入铝粉的质量为___________(填字母)。A.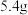 | B.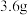 | C.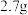 | D.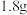 |
您最近一年使用:0次
2023-02-09更新
|
238次组卷
|
10卷引用:2019高考备考一轮复习精品资料 第三章 金属及其化合物 第2讲 镁、铝及其重要化合物【教学案】
(已下线)2019高考备考一轮复习精品资料 第三章 金属及其化合物 第2讲 镁、铝及其重要化合物【教学案】(已下线)专题3.2 铝及其重要化合物(讲)——2020年高考化学一轮复习讲练测(已下线)考点15 铝及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第08讲 金属材料(练)-2023年高考化学一轮复习讲练测(新教材新高考)第三章 金属及其化合物 第15讲 金属材料 金属冶炼(已下线)考点15 铝及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)2016-2017学年吉林长春外国语学校高一上期末理化学卷(已下线)3.2.2 物质的量在化学方程式计算中的应用(精练)-2020-2021学年上学期高一化学同步精品课堂(人教版必修第一册)黑龙江省虎林市高级中学2022-2023学年高三上学期第一次月考化学试题黑龙江省齐齐哈尔市三立高级中学2022-2023学年高三上学期期中考试化学试题
解题方法
4 . 已知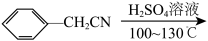
 ,用
,用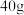 苯乙腈,最终得到
苯乙腈,最终得到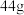 苯乙酸纯品,则苯乙酸的产率是
苯乙酸纯品,则苯乙酸的产率是___________ 。
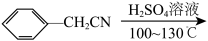
 ,用
,用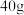 苯乙腈,最终得到
苯乙腈,最终得到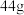 苯乙酸纯品,则苯乙酸的产率是
苯乙酸纯品,则苯乙酸的产率是
您最近一年使用:0次
5 . 准确称取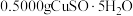 样品,加适量水溶解,转移至碘量瓶中,加过量
样品,加适量水溶解,转移至碘量瓶中,加过量 溶液并用稀
溶液并用稀 酸化,以淀粉溶液为指示剂,用
酸化,以淀粉溶液为指示剂,用 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 的溶液
的溶液 。测定过程中发生下列反应:
。测定过程中发生下列反应: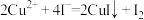 、
、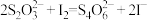 。计算
。计算 样品的纯度(写出计算过程):
样品的纯度(写出计算过程):_________ 。
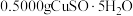 样品,加适量水溶解,转移至碘量瓶中,加过量
样品,加适量水溶解,转移至碘量瓶中,加过量 溶液并用稀
溶液并用稀 酸化,以淀粉溶液为指示剂,用
酸化,以淀粉溶液为指示剂,用 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 的溶液
的溶液 。测定过程中发生下列反应:
。测定过程中发生下列反应: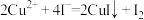 、
、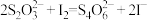 。计算
。计算 样品的纯度(写出计算过程):
样品的纯度(写出计算过程):
您最近一年使用:0次
6 . 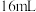 由
由 与
与 组成的混合气体在催化剂作用下于
组成的混合气体在催化剂作用下于 左右可发生反应:
左右可发生反应: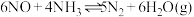 ,达到平衡时在相同条件下气体体积变为
,达到平衡时在相同条件下气体体积变为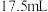 ,计算原混合气体中
,计算原混合气体中 与
与 的物质的量之比
的物质的量之比__________ 。
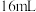 由
由 与
与 组成的混合气体在催化剂作用下于
组成的混合气体在催化剂作用下于 左右可发生反应:
左右可发生反应: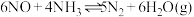 ,达到平衡时在相同条件下气体体积变为
,达到平衡时在相同条件下气体体积变为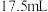 ,计算原混合气体中
,计算原混合气体中 与
与 的物质的量之比
的物质的量之比
您最近一年使用:0次
2023高三·全国·专题练习
7 . 将SO2通入用硫酸酸化的重铬酸钾溶液中,可制得硫酸铬钾KCr(SO4)2,反应的化学方程式为_______ ;如果溶液的酸碱性控制不当,可能会有Cr(OH)SO4杂质生成。现从得到的硫酸铬钾产品中取出3.160g样品加入足量盐酸和BaCl2溶液后,得到白色沉淀5.126g。若产品中杂质只有Cr(OH)SO4,则该产品中KCr(SO4)2的质量分数为_______ (用百分数表示,保留1位小数)。[摩尔质量/g·mol-1:KCr(SO4)2283;Cr(OH)SO4165]
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
8 . AlN用于电子仪器。AlN中常混有少量碳,将一定量含杂质碳的AlN样品置于密闭反应器中,通入4.032L(标准状况下的)O2,在高温下充分反应后测得气体的密度为1.34g/L(已折算成标准状况,AlN不跟O2反应),则所得气体的摩尔质量为_______ g/mol,该气体的成分是_______ (写化学式),该样品中含杂质碳_______ g。
您最近一年使用:0次
2023高三·全国·专题练习
9 . 将Pd(NH3)2Cl2在空气中550℃下焙烧(氧气不参与反应)可以直接得到海绵状的钯,海绵钯具有优良的储氢功能,其储氢原理为:2Pd(s)+xH2(g)=2PdHx(s)。假设海绵状金属钯密度为ρg·cm-3、摩尔质量为Mg·mol-1、其吸附的氢气是其体积的n倍(标准状况下),则此条件下海绵钯的储氢容量R=_______ mL·g-1,氢气的浓度r=_______ (储氢容量R即1g钯吸附氢气的体积;氢气的浓度r为1molPd吸附氢气的物质的量)。
您最近一年使用:0次
2023高三·全国·专题练习
10 . 某厂用m1kg的铬渣(含Cr2O340%)制备Cr(OH)SO4,最终得到产品m2kg,则产率为_______ 。
您最近一年使用:0次



