2023高三·全国·专题练习
解题方法
1 . 一定条件下Fe(OH)3与KClO在KOH溶液中反应可制得K2FeO4。生成0.1molK2FeO4转移的电子的物质的量_______ mol。
您最近一年使用:0次
2 . 对黄铵铁矾[化学式可表示为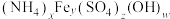 ,摩尔质量为
,摩尔质量为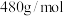 ]进行热分解实验,其分解过程如图所示。在
]进行热分解实验,其分解过程如图所示。在 前分解释放的物质为
前分解释放的物质为 ,
,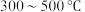 之间只有
之间只有 和
和 放出,此时残留固体中只含有
放出,此时残留固体中只含有 、O、S三种元素,
、O、S三种元素, 以上得到的是纯净的红棕色粉末。
以上得到的是纯净的红棕色粉末。

回答下列问题:
(1)黄铵铁矾的化学式为_______ 。
(2)在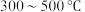 之间放出
之间放出 和
和 的物质的量之比是
的物质的量之比是_______ 。
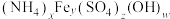 ,摩尔质量为
,摩尔质量为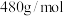 ]进行热分解实验,其分解过程如图所示。在
]进行热分解实验,其分解过程如图所示。在 前分解释放的物质为
前分解释放的物质为 ,
,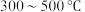 之间只有
之间只有 和
和 放出,此时残留固体中只含有
放出,此时残留固体中只含有 、O、S三种元素,
、O、S三种元素, 以上得到的是纯净的红棕色粉末。
以上得到的是纯净的红棕色粉末。
回答下列问题:
(1)黄铵铁矾的化学式为
(2)在
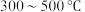 之间放出
之间放出 和
和 的物质的量之比是
的物质的量之比是
您最近一年使用:0次
3 . 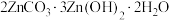 固体在加热升温过程中的质量变化如图所示。
固体在加热升温过程中的质量变化如图所示。

回答下列问题:
(1) 时,剩余固体中已不含碳元素,则剩余固体中含有
时,剩余固体中已不含碳元素,则剩余固体中含有_______ (填化学式)。
(2)整个过程的总反应方程式为_______ 。
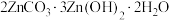 固体在加热升温过程中的质量变化如图所示。
固体在加热升温过程中的质量变化如图所示。
回答下列问题:
(1)
 时,剩余固体中已不含碳元素,则剩余固体中含有
时,剩余固体中已不含碳元素,则剩余固体中含有(2)整个过程的总反应方程式为
您最近一年使用:0次
解题方法
4 . 工业上是将氯气通入到 的
的 溶液中来制备
溶液中来制备 溶液,若
溶液,若 溶液中
溶液中 的质量分数为
的质量分数为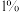 ,则生产
,则生产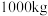 该溶液需消耗氯气的质量为
该溶液需消耗氯气的质量为_______  (保留整数)。
(保留整数)。
 的
的 溶液中来制备
溶液中来制备 溶液,若
溶液,若 溶液中
溶液中 的质量分数为
的质量分数为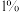 ,则生产
,则生产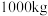 该溶液需消耗氯气的质量为
该溶液需消耗氯气的质量为 (保留整数)。
(保留整数)。
您最近一年使用:0次
解题方法
5 . 在搅拌下向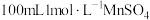 溶液中缓慢滴加
溶液中缓慢滴加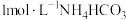 溶液,过滤、洗涤、干燥,得到
溶液,过滤、洗涤、干燥,得到 固体。需加入
固体。需加入 溶液的体积约为
溶液的体积约为_______ 。
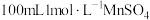 溶液中缓慢滴加
溶液中缓慢滴加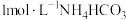 溶液,过滤、洗涤、干燥,得到
溶液,过滤、洗涤、干燥,得到 固体。需加入
固体。需加入 溶液的体积约为
溶液的体积约为
您最近一年使用:0次
解题方法
6 . 有同学提出用纯碱代替 溶液加入硫酸锌溶液中反应,在实际生产中得到的是一种碱式碳酸锌
溶液加入硫酸锌溶液中反应,在实际生产中得到的是一种碱式碳酸锌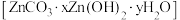 ,取该样品
,取该样品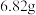 ,充分灼烧后测得残留物质量为
,充分灼烧后测得残留物质量为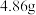 ,将所得气体通入足量澄清石灰水中,得到
,将所得气体通入足量澄清石灰水中,得到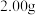 沉淀,则此碱式碳酸锌的化学式是
沉淀,则此碱式碳酸锌的化学式是______________________ 。
 溶液加入硫酸锌溶液中反应,在实际生产中得到的是一种碱式碳酸锌
溶液加入硫酸锌溶液中反应,在实际生产中得到的是一种碱式碳酸锌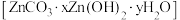 ,取该样品
,取该样品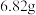 ,充分灼烧后测得残留物质量为
,充分灼烧后测得残留物质量为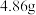 ,将所得气体通入足量澄清石灰水中,得到
,将所得气体通入足量澄清石灰水中,得到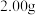 沉淀,则此碱式碳酸锌的化学式是
沉淀,则此碱式碳酸锌的化学式是
您最近一年使用:0次
22-23高一上·全国·课时练习
解题方法
7 . 有关物质的量浓度的计算
(1)计算的基本公式:c=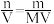 。
。
(2)计算的基本类型和方法:
①已知溶质的质量
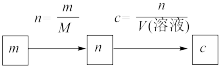
②已知溶液中某种粒子的数目
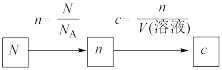
③标准状况下,气体溶质的物质的量浓度的计算
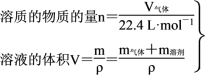 c=
c=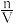
(3)注意:
①物质加入水中,注意溶质的判断。如SO3 H2SO4,Na2O或Na2O2
H2SO4,Na2O或Na2O2 NaOH,Na
NaOH,Na NaOH,NH3
NaOH,NH3 NH3·H2O等。
NH3·H2O等。
②溶液浓度与离子浓度的定量关系要注意电离程度与组成。
如0.1 mol·L-1的K2SO4溶液中c(K+)=0.2 mol·L-1。
(4)物质的量浓度与溶质的质量分数的换算
①换算公式:cB=_______ mol·L-1.M:溶质B的摩尔质量 ρ:溶液密度(g·mL-1)。
②推导方法:设溶液体积为1 L,则cB=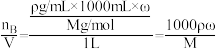 mol·L-1。
mol·L-1。
(5)溶液稀释和混合的计算
①溶液稀释的有关计算:稀释前后溶质的物质的量和质量都保持不变。_______ 。
②溶液混合的计算:混合前后溶质的物质的量或质量不变。_______ 。
注意:无特别指明时,V(混)≠V1+V2;V(混)= ,但溶液的质量守恒:m(混)=m1+m2。
,但溶液的质量守恒:m(混)=m1+m2。
(6)常见物理量之间的换算关系
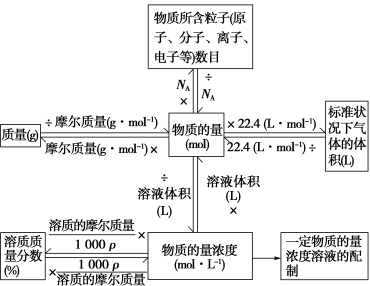
万能公式:n= =cBV
=cBV
(1)计算的基本公式:c=
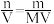 。
。(2)计算的基本类型和方法:
①已知溶质的质量

②已知溶液中某种粒子的数目
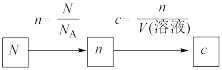
③标准状况下,气体溶质的物质的量浓度的计算
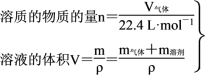 c=
c=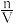
(3)注意:
①物质加入水中,注意溶质的判断。如SO3
 H2SO4,Na2O或Na2O2
H2SO4,Na2O或Na2O2 NaOH,Na
NaOH,Na NaOH,NH3
NaOH,NH3 NH3·H2O等。
NH3·H2O等。②溶液浓度与离子浓度的定量关系要注意电离程度与组成。
如0.1 mol·L-1的K2SO4溶液中c(K+)=0.2 mol·L-1。
(4)物质的量浓度与溶质的质量分数的换算
①换算公式:cB=
②推导方法:设溶液体积为1 L,则cB=
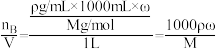 mol·L-1。
mol·L-1。(5)溶液稀释和混合的计算
①溶液稀释的有关计算:稀释前后溶质的物质的量和质量都保持不变。
②溶液混合的计算:混合前后溶质的物质的量或质量不变。
注意:无特别指明时,V(混)≠V1+V2;V(混)=
 ,但溶液的质量守恒:m(混)=m1+m2。
,但溶液的质量守恒:m(混)=m1+m2。(6)常见物理量之间的换算关系

万能公式:n=
 =cBV
=cBV
您最近一年使用:0次
2022高一·全国·专题练习
8 . 化学实验的微型化可有效地减少污染,实现化学实验绿色化的要求。某学生按下列操作做一个实验:在一块下衬白纸的玻璃片的不同位置分别滴加浓度为0.1 mol·L-1的KBr、KI(含淀粉溶液)、NaOH(含酚酞)、FeCl2(含KSCN)溶液各1滴,每种液滴彼此分开,围成半径小于表面皿的圆形(如图所示),在圆心处放置2粒芝麻粒大小的KMnO4晶体,向KMnO4晶体上滴加一滴浓盐酸,再立即用表面皿盖好。
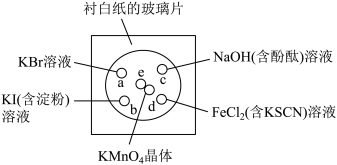
(1)e处反应的离子方程式为_______ 。该反应中发生反应的氧化剂和还原剂的物质的量之比为_______ 。
(2)b处的实验现象为_______ 。d处的实验现象为_______ 。
(3)c处反应的化学方程式为_______ 。标准状况下,当有0.224 L Cl2被NaOH溶液吸收后,转移电子的物质的量为_______ mol。
(4)通过该实验能否比较Cl2、FeCl3、KMnO4三种物质氧化性的强弱?_______ (填“能”或“不能”),若能,其氧化性由强到弱的顺序是_______ 。

(1)e处反应的离子方程式为
(2)b处的实验现象为
(3)c处反应的化学方程式为
(4)通过该实验能否比较Cl2、FeCl3、KMnO4三种物质氧化性的强弱?
您最近一年使用:0次
2022高一·全国·专题练习
9 . 常温常压下,用等质量的CH4、CO2、O2、SO2分别吹出四个气球,如图所示:
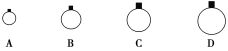
问题思考:
(1)等质量的CH4、CO2、O2、SO2的物质的量之比为_____
(2)同温同压下,等质量的CH4、CO2、O2、SO2的体积比为_____
(3)A、B、C、D四个气球中的气体分别是_____

问题思考:
(1)等质量的CH4、CO2、O2、SO2的物质的量之比为
(2)同温同压下,等质量的CH4、CO2、O2、SO2的体积比为
(3)A、B、C、D四个气球中的气体分别是
您最近一年使用:0次
2022高三·全国·专题练习
10 . 胆矾(CuSO4·5H2O)易溶于水,难溶于乙醇。某小组用工业废铜焙烧得到的CuO(杂质为氧化铁及泥沙)为原料与稀硫酸反应制备胆矾,并测定其结晶水的含量。回答下列问题:
结晶水测定:称量干燥坩埚的质量为m1,加入胆矾后总质量为m2,将坩埚加热至胆矾全部变为白色,置于干燥器中冷至室温后称量,重复上述操作,最终总质量恒定为m3.根据实验数据,胆矾分子中结晶水的个数为_______ (写表达式)。
结晶水测定:称量干燥坩埚的质量为m1,加入胆矾后总质量为m2,将坩埚加热至胆矾全部变为白色,置于干燥器中冷至室温后称量,重复上述操作,最终总质量恒定为m3.根据实验数据,胆矾分子中结晶水的个数为
您最近一年使用:0次



