1 . 设阿伏加德罗常数的值为 ,则下列说法正确的是
,则下列说法正确的是
 ,则下列说法正确的是
,则下列说法正确的是A.标准状况下, 个 个 分子占据空间的体积约为22.4 L 分子占据空间的体积约为22.4 L |
B.将含0.6 mol HCl溶质的浓盐酸与足量 共热,生成 共热,生成 的分子数为 的分子数为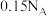 |
C.常温常压下,16 g 中含有的C-H共价键个数为 中含有的C-H共价键个数为 |
D.在0.1 mol/L  溶液中, 溶液中,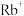 的数量为 的数量为 |
您最近一年使用:0次
名校
解题方法
2 . 用 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是
 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是A.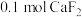 中含有的阳离子数目为 中含有的阳离子数目为 |
B.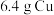 与足量 与足量 完全反应转移电子数目为 完全反应转移电子数目为 |
C.常温常压下,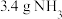 中含有的共价键数目为 中含有的共价键数目为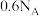 |
D. 由 由 和 和 组成的混合气体中含有的氧原子数目为 组成的混合气体中含有的氧原子数目为 |
您最近一年使用:0次
3 . 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
①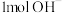 所含电子数为
所含电子数为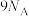
②任何气体的气体摩尔体积都约为
③常温常压下, 与
与 的混合气体所含原子数为
的混合气体所含原子数为
④同温同体积时,气体的物质的量越大,则压强越大
⑤两种物质的物质的量相同,则它们在标准状况下的体积也相同
⑥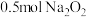 固体中含有阴离子的数目为
固体中含有阴离子的数目为
⑦足量的浓盐酸与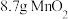 在加热条件下反应,被氧化的
在加热条件下反应,被氧化的 为
为
⑧ 的
的 溶液中,
溶液中, 离子的数目为
离子的数目为
⑨Na与水反应时,水表现出氧化性
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是①
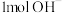 所含电子数为
所含电子数为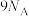
②任何气体的气体摩尔体积都约为

③常温常压下,
 与
与 的混合气体所含原子数为
的混合气体所含原子数为
④同温同体积时,气体的物质的量越大,则压强越大
⑤两种物质的物质的量相同,则它们在标准状况下的体积也相同
⑥
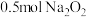 固体中含有阴离子的数目为
固体中含有阴离子的数目为
⑦足量的浓盐酸与
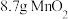 在加热条件下反应,被氧化的
在加热条件下反应,被氧化的 为
为
⑧
 的
的 溶液中,
溶液中, 离子的数目为
离子的数目为
⑨Na与水反应时,水表现出氧化性
| A.①②⑤⑦ | B.③④⑦⑨ | C.①④⑥⑨ | D.③④⑤⑧ |
您最近一年使用:0次
4 .  代表阿伏加德罗常数的值。下列说法正确的是
代表阿伏加德罗常数的值。下列说法正确的是
 代表阿伏加德罗常数的值。下列说法正确的是
代表阿伏加德罗常数的值。下列说法正确的是A.1mol蔗糖完全水解生成的葡萄糖分子数为 |
B.工业上,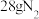 和4mol 和4mol 在高温高压催化剂作用下生成的 在高温高压催化剂作用下生成的 分子数为 分子数为 |
C.标准状况下,11.2L氯仿(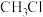 )中含有的极性键数目为 )中含有的极性键数目为 |
D.1molFe溶于过量稀硝酸溶液中,转移电子数为 |
您最近一年使用:0次
22-23高二上·浙江·期中
名校
5 . 将一定量的氯气通入60 mL浓度为10.00 mol·L-1的氢氧化钠浓溶液中,加热一段时间后恰好完全反应,溶液中形成NaCl、NaClO、 NaClO3共存体系。下列判断正确的是
| A.NaClO和NaC1O3是还原产物 |
| B.与NaOH反应的氯气的物质的量是0.6 mol |
| C.n(NaCl) : n(NaClO) : n(NaClO3)可能为10:7:1 |
| D.若反应中转移的电子为n mol,则0.3<n<0.5 |
您最近一年使用:0次
名校
6 . 设NA为阿伏加德罗常数的值。下列说法正确的是
| A.2.0 g H218O与D2O的混合物中所含中子数为NA |
| B.1 mol Na2O2固体中含离子总数为4NA |
| C.标准状况下,11.2 LH2O中含有分子的数目为0.5NA |
| D.1 mol Fe与1 mol Cl2充分反应,转移电子数为3NA |
您最近一年使用:0次
名校
7 . 设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.在常温常压下,11.2 L N2含有的分子数为0.5NA |
| B.分子总数为NA的N2、CO混合气体体积约为22.4 L,质量为28 g |
| C.常温常压下,1.6 g CH4含原子数为0.5NA |
| D.足量的CO2与39 g Na2O2发生反应,转移的电子数为NA |
您最近一年使用:0次
名校
8 . 下列叙述正确的是
A. 中含有的中子数为 中含有的中子数为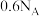 |
B.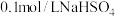 溶液中, 溶液中, 数目为 数目为 |
C.常温常压下,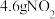 气体含有原子数为 气体含有原子数为 |
D.标准状况下,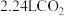 与足量 与足量 反应,转移的电子数 反应,转移的电子数 |
您最近一年使用:0次
2023-01-14更新
|
131次组卷
|
3卷引用:内蒙古赤峰二中2022-2023高一上学期期末考试化学试题
名校
9 . 工业上曾经通过反应“3Fe+4NaOH=Fe3O4+2H2↑+4Na↑”生产金属钠。下列有关说法正确的是
| A.用磁铁可以将Fe 与Fe3O4分离 |
| B.将生成的气体在空气中冷却可获得钠 |
| C.该反应中的氧化剂是NaOH |
| D.反应中若生成22.4 L H2(标准状况下),则转移的电子数约为2×6.02×1023 |
您最近一年使用:0次
10 . 用 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是
 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是A.活泼金属与盐酸反应生成  ,转移电子数为 ,转移电子数为 |
B.常温常压下,  中含分子数为 中含分子数为 |
C.80 g 中含氮原子数为 中含氮原子数为 |
D.  溶液中含 溶液中含 数为 数为 |
您最近一年使用:0次



