名校
1 . NA为阿伏加德罗常数的值。下列说法正确的是
| A.18gD2O和18gH2O中含有的质子数均为10NA |
| B.2L 0.5mol/L亚硫酸溶液中含有的氢离子数为2NA |
| C.密闭容器中2molNO与1molO2充分反应,产物的分子数为2NA |
| D.过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.2NA |
您最近一年使用:0次
名校
2 . 下列说法正确的是
| A.1molO2的体积为22.4L |
| B.28g丁烯所含碳原子数是28g乙烯所含碳原子数的2倍 |
| C.0.1mol/LAlCl3溶液中Cl-的物质的量为0.3mol |
| D.5.6gFe与足量C12反应,转移电子的物质的量为0.3mol |
您最近一年使用:0次
2021-09-07更新
|
59次组卷
|
2卷引用:甘肃省嘉峪关市第一中学2021届高三上学期一模考试化学试卷
名校
3 . 高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,其制备原理如下:2Fe(OH)3+3KClO+4KOH=2K2FeO4+3KCl+5H2O,下列说法正确的是
| A.0.1mol/LKClO溶液中含有的ClO-数目小于0.1NA |
| B.制备1molK2FeO4转移的电子数为3NA |
| C.18gH218O所含的质子数、电子数均为10NA |
| D.0.1mol高铁酸钾与水作用能生成0.1molFe(OH)3(胶体) |
您最近一年使用:0次
2021-08-26更新
|
613次组卷
|
6卷引用:新疆石河子第一中学2020-2021学年高三上学期8月月考(B卷)化学试题
新疆石河子第一中学2020-2021学年高三上学期8月月考(B卷)化学试题新疆石河子第一中学2021-2022学年高三上学期8月月考(A卷)化学试题黑龙江省大庆铁人中学2022届高三上学期开学考试化学试题(已下线)2021年秋季高三化学开学摸底考试卷03(山东专用)(已下线)专题02 NA及其应用—2022年高考化学二轮复习讲练测(全国版)-测试湖南省娄底涟源市第一中学2022届高三下学期第三次模考化学试题
名校
解题方法
4 . 若NA表示阿伏加德罗常数的数值,下列说法正确的是
| A.在标准状况下,11.2L氯气和氢气的混合物中所含的分子数为NA |
| B.5.6g铁与氯气完全反应,失去电子的数目为0.2NA |
| C.1molCl2发生化学反应,转移的电子数一定为2NA |
| D.在标准状况下,22.4L由N2、N2O组成的混合气体中所含有的N的物质的量为2mol |
您最近一年使用:0次
名校
5 . 阿伏加德罗常数的值为NA,下列说法正确的是
| A.标准状况下,2.24LN2和O2的混合气体中分子数为0.2NA |
| B.标准状况下,NA个苯分子所占体积为22.4L |
| C.标准状况下22.4LH2O中电子数为10NA |
| D.14gC2H4和C3H6混合气体中的氢原子数为2NA |
您最近一年使用:0次
名校
6 . 若 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是
 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是A.标准状况下,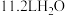 含有的分子数为 含有的分子数为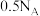 |
B. 过氧化钠与足量水反应,转移电子数为 过氧化钠与足量水反应,转移电子数为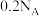 |
C.常温常压下, 含有的分子数为 含有的分子数为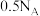 |
D.常温下,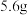 铁与硝酸反应,失去的电子数一定为 铁与硝酸反应,失去的电子数一定为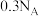 |
您最近一年使用:0次
2021-03-19更新
|
728次组卷
|
4卷引用:新疆乌鲁木齐市第八中学2018-2019学年高二下学期第三次月考化学试题
新疆乌鲁木齐市第八中学2018-2019学年高二下学期第三次月考化学试题(已下线)广东省深圳中学2020-2021学年高一下学期期中考试化学试题四川省南充市李渡中学2020-2021学年高一下学期第一次月考化学试题广东省汕头市澄海中学2020-2021学年高一下学期期中考试选择考化学试题
7 . 设NA表示阿伏加德罗常数的值。下列说法正确的是
| A.常温下,pH=13的NaOH溶液中含有的OH-数目为0.1NA |
| B.14 g聚乙烯中含C-H键总数目为2NA |
| C.100 mL 12 mol·L-1浓硝酸与过量Cu反应转移电子的数目为0.6NA |
| D.电解精炼铜时,若阳极质量减少64 g,则阴极得到电子的数目为2NA |
您最近一年使用:0次
8 . 工业上利用铁的氧化物在高温条件下循环裂解水制氢气的流程如图所示。

(1)反应I的化学方程式为:Fe3O4(s)+CO(g) 3FeO(s)+CO2(g),反应Ⅱ的化学方程式为
3FeO(s)+CO2(g),反应Ⅱ的化学方程式为_______ ,对比反应I、Ⅱ,铁的氧化物在循环裂解水制氢气过程中的作用是_______ 。
(2)反应III为:CO2(g)+C(s)⇌2CO(g) ∆H>0。为了提高达平衡后CO的产量,理论上可以采取的合理措施有_______ (任写一条措施)。
(3)流程图中碳的氧化物可用来制备碳酰肼[CO(NHNH2)2,其中碳元素为+4价]。加热条件下,碳酰肼能将锅炉内表面锈蚀后的氧化铁转化为结构紧密的四氧化三铁保护层,并生成氮气、水和二氧化碳。该反应的化学方程式为_______ 。
(4)①高铁酸盐是常用的水处理剂。高铁酸钠(Na2FeO4)可用如下反应制备:
2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑
若生成2mol Na2FeO4,则反应中电子转移的物质的量为_______ mol。
②高铁酸盐可将水体中的Mn2+氧化为MnO2进行除去,若氧化含Mn2+ 1mg的水体样本,需要1.2mg·L-1高铁酸钾_______ L。

(1)反应I的化学方程式为:Fe3O4(s)+CO(g)
 3FeO(s)+CO2(g),反应Ⅱ的化学方程式为
3FeO(s)+CO2(g),反应Ⅱ的化学方程式为(2)反应III为:CO2(g)+C(s)⇌2CO(g) ∆H>0。为了提高达平衡后CO的产量,理论上可以采取的合理措施有
(3)流程图中碳的氧化物可用来制备碳酰肼[CO(NHNH2)2,其中碳元素为+4价]。加热条件下,碳酰肼能将锅炉内表面锈蚀后的氧化铁转化为结构紧密的四氧化三铁保护层,并生成氮气、水和二氧化碳。该反应的化学方程式为
(4)①高铁酸盐是常用的水处理剂。高铁酸钠(Na2FeO4)可用如下反应制备:
2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑
若生成2mol Na2FeO4,则反应中电子转移的物质的量为
②高铁酸盐可将水体中的Mn2+氧化为MnO2进行除去,若氧化含Mn2+ 1mg的水体样本,需要1.2mg·L-1高铁酸钾
您最近一年使用:0次
9 . 设NA为阿伏加德罗常数的值。下列叙述正确的是
| A.0.1mol苯分子中含有双键数为NA |
| B.1L 1 mol∙L−1碳酸钠溶液中阴离子的数目大于NA |
| C.标准状况下,22.4L己烷中共含分子数为NA |
| D.50mL18.4 mol∙L−1浓硫酸与足量铜微热反应,转移的电子的数目为0.92NA |
您最近一年使用:0次
解题方法
10 . 设NA为阿伏加德罗常数。下列有关叙述正确的是
| A.常温常压下,22.4LHCl气体溶于水产生的H+数为NA |
| B.100ml0.01mol·L-1的甲醛水溶液含有的分子数为0.001NA |
| C.28gCO和N2混合气体含有的原子数为2NA |
| D.1mol的Cl2与足量H2氢气混合在点燃条件下充分反应转移的电子数为NA |
您最近一年使用:0次



