名校
1 . 碳循环(如图所示)的研究有利于实现我国的碳达峰及碳中和目标。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
| A.可通过加聚反应使葡萄糖转化为淀粉 |
B.电催化 转化为乙酸时,转移 转化为乙酸时,转移 个电子 个电子 |
C. 、 、 分子中碳原子均不存在孤对电子 分子中碳原子均不存在孤对电子 |
D.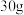 葡萄糖与乙酸的混合物中含有的氢原子数目为 葡萄糖与乙酸的混合物中含有的氢原子数目为 个 个 |
您最近一年使用:0次
2 .  可与
可与 反应生成白烟和无污染的
反应生成白烟和无污染的 ,根据该反应原理,管道工人可利用浓氨水检验氯气管道是否漏气。设
,根据该反应原理,管道工人可利用浓氨水检验氯气管道是否漏气。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 可与
可与 反应生成白烟和无污染的
反应生成白烟和无污染的 ,根据该反应原理,管道工人可利用浓氨水检验氯气管道是否漏气。设
,根据该反应原理,管道工人可利用浓氨水检验氯气管道是否漏气。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.11.2L  中含有孤对电子数为0.5 中含有孤对电子数为0.5 |
B.每消耗34g  ,转移电子总数为6 ,转移电子总数为6 |
C.0.1mol  充分反应,产物中的离子总数最多为0.4 充分反应,产物中的离子总数最多为0.4 |
D.每生成1mol  ,断裂的 ,断裂的 键数为11 键数为11 |
您最近一年使用:0次
名校
解题方法
3 . 监测 含量是否达到排放标准的反应原理是
含量是否达到排放标准的反应原理是 .
. 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是
 含量是否达到排放标准的反应原理是
含量是否达到排放标准的反应原理是 .
. 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是A.0.1mol 固体中所含离子总数为 固体中所含离子总数为 |
B.25℃时, 的HCl溶液中含有 的HCl溶液中含有 的数目为 的数目为 |
C.17g 中含有的原子数目为 中含有的原子数目为 |
D.2.24L 中含有的分子数目为 中含有的分子数目为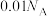 |
您最近一年使用:0次
名校
4 . 设 为阿伏加德罗常数的数值,下列说法正确的是
为阿伏加德罗常数的数值,下列说法正确的是
 为阿伏加德罗常数的数值,下列说法正确的是
为阿伏加德罗常数的数值,下列说法正确的是A. 由 由 与 与 组成的混合物中,原子数目为 组成的混合物中,原子数目为 |
B.常温下,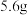 铁与足量浓硝酸反应转移的电子数为 铁与足量浓硝酸反应转移的电子数为 |
C.标准状况下, 中 中 的数目可能为 的数目可能为 |
D.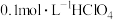 溶液中 溶液中 的数目为 的数目为 |
您最近一年使用:0次
2024-01-18更新
|
167次组卷
|
2卷引用:福建省龙岩市一级校联盟2023-2024学年高三上学期半期考联考化学试题
5 . 用NA 代表阿伏加德罗常数的值,下列说法正确的是
| A.等质量的N4与N2所含的原子个数比为2:1 |
| B.标准状况下,11.2LCCl4所含分子数为0.5NA |
C.1.8g的NH 中含有的电子数为NA 中含有的电子数为NA |
| D.0.1mol·L-1的MgCl2溶液中,所含Cl-的数目为0.2NA |
您最近一年使用:0次
名校
解题方法
6 . 设NA表示阿伏伽德罗常数的值,下列说法正确的是
| A.标准状况下,22.4L水中含σ键数目为2NA |
| B.1mol甲基(-CH3)中含10NA个电子 |
| C.28g氮气(N2)和1mol氢氰酸(HCN)中含有π键均为2NA |
| D.常温下,12g镁与足量稀硫酸反应,转移电子数为2NA |
您最近一年使用:0次
2023-09-16更新
|
227次组卷
|
2卷引用:福建省龙岩市连城县第一中学2022-2023学年高二下学期3月月考化学试题
名校
解题方法
7 . 下列说法中正确的是
| A.离子晶体固体AlF3中,一个Al3+与3个F-形成静电吸引作用 |
| B.基态O2-中有10种空间运动状态的电子 |
| C.1mol配离子[Cu(NH3)4]2+中,σ键数为13NA(NA为阿伏加德罗常数) |
| D.KNO3固体中,作用力有离子键、σ键、极性共价键 |
您最近一年使用:0次
名校
8 . 设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.标准状况下,2.24L 与 与 反应完全,形成 反应完全,形成 键的数目为 键的数目为 |
B.标准状况下,2.24L2-甲基戊烷中共价键数为 |
C.12g石墨中 键数为 键数为 |
D.60g乙酸与足量乙醇发生酯化反应,断裂的 键数为 键数为 |
您最近一年使用:0次
9 . 电催化 还原制氨是一种很有吸引力的替代方法,它可以在较温和的条件下实现氨的合成(反应表达式为:
还原制氨是一种很有吸引力的替代方法,它可以在较温和的条件下实现氨的合成(反应表达式为: )。设
)。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 还原制氨是一种很有吸引力的替代方法,它可以在较温和的条件下实现氨的合成(反应表达式为:
还原制氨是一种很有吸引力的替代方法,它可以在较温和的条件下实现氨的合成(反应表达式为: )。设
)。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是| A.电催化还原制氨实现化学能向电能转变 |
B.每产生34 g  , , 得到的电子数为 得到的电子数为 |
C.1 L 1 mol·L 氨水中, 氨水中, 分子数数为 分子数数为 |
D.消耗11.2 L  时,产生的 时,产生的 分子数为 分子数为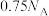 |
您最近一年使用:0次
解题方法
10 . 设NA为阿伏加德罗常数的值,下列说法正确的是
A.25.6gS8(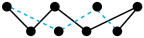 )分子中,所含共价键总数为0.1NA )分子中,所含共价键总数为0.1NA |
| B.0.1mol•L-1NaOH溶液中所含质子总数为2NA |
| C.4.2gC3H6分子中,所含σ键总数可能为0.9NA |
| D.1.1gK2S固体中,所含离子总数为0.3NA |
您最近一年使用:0次



