名校
1 . 回答下列问题
(1)标准状况下3.4gNH3与标准状况下_______ LH2S气体含有相同数目的氢原子数。
(2)19g某二价金属的氯化物RCl2中含有0.4mol的Cl-,则R的相对原子质量为_______ 。
(3)如图是某品牌饮用矿物质水的标签的部分内容。
请认真阅读标签内容,计算:
①镁离子的物质的量浓度的最大值是_______ 。
②一瓶合格的这种矿泉水中硫酸根离子的物质的量不能超过_______ mol。
(4)VLFe2(SO4)3溶液中含Fe3+mg,则溶液中SO 的物质的量浓度为
的物质的量浓度为_______ mol/L。
(5)在RO 中,共有x个核外电子,R原子的质量数为A,则R原子核内含有的中子数目是
中,共有x个核外电子,R原子的质量数为A,则R原子核内含有的中子数目是_______ 。
(1)标准状况下3.4gNH3与标准状况下
(2)19g某二价金属的氯化物RCl2中含有0.4mol的Cl-,则R的相对原子质量为
(3)如图是某品牌饮用矿物质水的标签的部分内容。
| 配料表:纯净水、硫酸镁、氯化钾 保质期:12个月 主要成分: 钾离子(K+):1.0~27.3mg/L 镁离子(Mg2+):0.1~4.8mg/L 氯离子(Cl-):10~27.3mg/L 硫酸根离子(SO  ):0.4~19.2mg/L ):0.4~19.2mg/L |
①镁离子的物质的量浓度的最大值是
②一瓶合格的这种矿泉水中硫酸根离子的物质的量不能超过
(4)VLFe2(SO4)3溶液中含Fe3+mg,则溶液中SO
 的物质的量浓度为
的物质的量浓度为(5)在RO
 中,共有x个核外电子,R原子的质量数为A,则R原子核内含有的中子数目是
中,共有x个核外电子,R原子的质量数为A,则R原子核内含有的中子数目是
您最近一年使用:0次
2023-08-26更新
|
186次组卷
|
2卷引用:辽宁省大连市第八中学2022-2023学年高一上学期12月月考化学试题
名校
解题方法
2 . 完成下列计算:
(1)若ag CO2含b个原子,则阿伏加德罗常数为___________ mol-1。
(2)含0.6molCl-的氯化镁的质量是___________ g。
(3)已知4.8g CO2和CO混合气体中含分子数为0.15NA,该混合气体的平均摩尔质量为___________ ,CO2和CO的物质的量之比是___________ 。
(1)若ag CO2含b个原子,则阿伏加德罗常数为
(2)含0.6molCl-的氯化镁的质量是
(3)已知4.8g CO2和CO混合气体中含分子数为0.15NA,该混合气体的平均摩尔质量为
您最近一年使用:0次
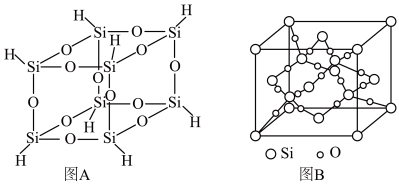
3 . 倍半硅氧烷在液晶显示、塑料阻燃、生物医用等领域具有重要应用,氢基倍半硅氧烷的分子结构如图A所示,其加热分解产物中SiO2的晶胞结构如图B所示。回答下列问题:
(1)基态Si原子的核外电子排布式为_______ ,其中每对成对电子之间的区别是_______ 。
(2)图A分子结构中,一个硅原子被3个_______ 元环共用,该分子的分子式为_______ 。
(3)图A分子结构中H元素的化合价为_______ ,O原子采用_______ 杂化,形成的极性共价键类型为(电子云重叠方式)_______ ;键的极性:Si-O键_______ Si-H键(填“>”“<”或“=”)。
(4)氢基倍半硅氧烷为_______ 晶体,SiO2为_______ 晶体。
(5)每个SiO2晶胞中含有O原子的个数为_______ ;已知SiO2晶体为面心立方结构,晶胞参数为anm,阿伏加德罗常数的值为NA,则SiO2晶体的密度为_______ g•cm-3。

(1)基态Si原子的核外电子排布式为
(2)图A分子结构中,一个硅原子被3个
(3)图A分子结构中H元素的化合价为
(4)氢基倍半硅氧烷为
(5)每个SiO2晶胞中含有O原子的个数为
您最近一年使用:0次



