名校
1 . 设 表示阿伏加德罗常数的值,下列叙述正确的是
表示阿伏加德罗常数的值,下列叙述正确的是
 表示阿伏加德罗常数的值,下列叙述正确的是
表示阿伏加德罗常数的值,下列叙述正确的是A. 熔融态时含有 熔融态时含有 个离子 个离子 |
B. 和 和 混合气体中氧原子总数为 混合气体中氧原子总数为 |
C.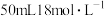 硫酸与足量铜共热,转移的电子数为 硫酸与足量铜共热,转移的电子数为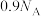 |
D. 的 的 水溶液中含有的氧原子数为 水溶液中含有的氧原子数为 |
您最近半年使用:0次
名校
2 . 将32g铜与140mL一定浓度的硝酸反应,铜完全溶解产生的NO和 混合气体在标准状况下的体积为11.2L。请回答:
混合气体在标准状况下的体积为11.2L。请回答:
(1)NO的体积为___________ L, 的体积为
的体积为___________ L。
(2)参加反应的硝酸的物质的量是___________ mol。
(3)待产生的气体全部释放后,向溶液加入V mL a mol/L的NaOH溶液,恰好使溶液中的 全部转化成沉淀,则原硝酸溶液的浓度为
全部转化成沉淀,则原硝酸溶液的浓度为___________ mol/L。(结果不需化简)
(4)欲使铜与硝酸反应生成的气体在NaOH溶液中全部转化为 ,至少需要30%的双氧水
,至少需要30%的双氧水_________ g。
 混合气体在标准状况下的体积为11.2L。请回答:
混合气体在标准状况下的体积为11.2L。请回答:(1)NO的体积为
 的体积为
的体积为(2)参加反应的硝酸的物质的量是
(3)待产生的气体全部释放后,向溶液加入V mL a mol/L的NaOH溶液,恰好使溶液中的
 全部转化成沉淀,则原硝酸溶液的浓度为
全部转化成沉淀,则原硝酸溶液的浓度为(4)欲使铜与硝酸反应生成的气体在NaOH溶液中全部转化为
 ,至少需要30%的双氧水
,至少需要30%的双氧水
您最近半年使用:0次
3 . 下列说法中,正确的是
A. 的质量是 的质量是 |
B. 中含有的分子数约为 中含有的分子数约为 |
C. 的体积一定是 的体积一定是 |
D. 溶液中含有 溶液中含有 |
您最近半年使用:0次
名校
4 . 下列说法是否正确(正确的打“√”,不正确的打“×”)若不正确请说明理由。
(1)元素周期表中每一横行称为一周期,每一纵列称为一个族。_________ ;
(2)FeCl3与Cu的反应为置换反应。_________ ;
(3)1 mol Na2O溶于水中形成1 L溶液,所得溶液的物质的量浓度为1 mol/L。_________ ;
(4)镧镍合金能大量吸收H2形成金属氢化物,可作储氢材料。_________
(1)元素周期表中每一横行称为一周期,每一纵列称为一个族。
(2)FeCl3与Cu的反应为置换反应。
(3)1 mol Na2O溶于水中形成1 L溶液,所得溶液的物质的量浓度为1 mol/L。
(4)镧镍合金能大量吸收H2形成金属氢化物,可作储氢材料。
您最近半年使用:0次
名校
解题方法
5 . 将100mL0.1mol/L的氯化钡溶液与50mL0.2mol/L的氯化钠溶液混合,不考虑溶液混合时体积的变化,则混合溶液中氯离子浓度是
| A.0.2mol/L | B.0.01mol/L | C.0.1mol/L | D.0.02mol/L |
您最近半年使用:0次
名校
6 . 回答下列问题。
Ⅰ.请回答:
(1)容量瓶是配制溶液所用的主要仪器。容量瓶上需标有___________ (填序号)。
①温度 ②浓度 ③容量 ④压强 ⑤刻度线 ⑥酸式或碱式
(2)下列关于容量瓶操作的说法中,正确的是___________(填序号)。
Ⅱ.实验室欲配制 的
的 溶液240mL:
溶液240mL:
(3)配制溶液时必须用到的仪器有托盘天平、药匙、玻璃棒、烧杯、量筒、胶头滴管和___________ 。
(4)若用 晶体来配制该溶液,应称量晶体的质量为
晶体来配制该溶液,应称量晶体的质量为___________ g。
(5)容量瓶使用前必须进行的操作是___________ 。
(6)在配制过程中,其他操作都正确,下列操作会引起所配溶液浓度偏高的是___________ (填序号)。
①没有洗涤烧杯和玻璃棒
②容量瓶未干燥,且瓶内有少量蒸馏水
③用托盘天平称量 晶体时,药品和砝码放反了
晶体时,药品和砝码放反了
④定容时俯视刻度线
⑤定容后塞上瓶塞反复摇匀,静置后,发现液面低于刻度线,再加水至刻度线
Ⅲ.某化学实验室需要 硫酸溶液480mL。根据溶液的配制情况回答下列问题:
硫酸溶液480mL。根据溶液的配制情况回答下列问题:
(7)现用质量分数为98%、密度为 的浓硫酸来配制所需的稀硫酸。计算所需浓硫酸的体积为
的浓硫酸来配制所需的稀硫酸。计算所需浓硫酸的体积为___________ mL(保留1位小数)。有①10mL、②25mL、③50mL、④100mL四种规格量筒,你选用量筒是___________ (填序号)。
(8)配制时,一般可分为几个步骤:①量取 ②计算 ③摇匀 ④稀释 ⑤冷却 ⑥洗涤 ⑦定容 ⑧转移,其正确的操作顺序为②→①→④→________→_________→_________→_________→③(填序号)。___________
Ⅰ.请回答:
(1)容量瓶是配制溶液所用的主要仪器。容量瓶上需标有
①温度 ②浓度 ③容量 ④压强 ⑤刻度线 ⑥酸式或碱式
(2)下列关于容量瓶操作的说法中,正确的是___________(填序号)。
| A.如果检漏时发现漏水,应当用滤纸吸干后再使用 |
| B.定容时,慢慢将蒸馏水倒至凹液面最低处与刻度线相平 |
| C.查漏时,应将活塞旋转180°再次检验是否漏水 |
| D.定容摇匀后,若发现液面变低,应补加蒸馏水至刻度线 |
Ⅱ.实验室欲配制
 的
的 溶液240mL:
溶液240mL:(3)配制溶液时必须用到的仪器有托盘天平、药匙、玻璃棒、烧杯、量筒、胶头滴管和
(4)若用
 晶体来配制该溶液,应称量晶体的质量为
晶体来配制该溶液,应称量晶体的质量为(5)容量瓶使用前必须进行的操作是
(6)在配制过程中,其他操作都正确,下列操作会引起所配溶液浓度偏高的是
①没有洗涤烧杯和玻璃棒
②容量瓶未干燥,且瓶内有少量蒸馏水
③用托盘天平称量
 晶体时,药品和砝码放反了
晶体时,药品和砝码放反了④定容时俯视刻度线
⑤定容后塞上瓶塞反复摇匀,静置后,发现液面低于刻度线,再加水至刻度线
Ⅲ.某化学实验室需要
 硫酸溶液480mL。根据溶液的配制情况回答下列问题:
硫酸溶液480mL。根据溶液的配制情况回答下列问题:(7)现用质量分数为98%、密度为
 的浓硫酸来配制所需的稀硫酸。计算所需浓硫酸的体积为
的浓硫酸来配制所需的稀硫酸。计算所需浓硫酸的体积为(8)配制时,一般可分为几个步骤:①量取 ②计算 ③摇匀 ④稀释 ⑤冷却 ⑥洗涤 ⑦定容 ⑧转移,其正确的操作顺序为②→①→④→________→_________→_________→_________→③(填序号)。
您最近半年使用:0次
名校
7 . 物质的量是高中化学常用的物理量,请完成以下有关计算:
(1)某气体氧化物的化学式为 ,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为
,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为___________ ,R的相对原子质量为___________ 。
(2)标准状况下有① ,②
,② 个
个 分子,③
分子,③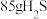 三种气体,对这三种气体的物质的量从大到小的顺序是
三种气体,对这三种气体的物质的量从大到小的顺序是___________ (填序号)。
(3)某混合盐溶液中含有离子: 、
、 、
、 、
、 ,测得
,测得 、
、 和
和 的物质的量浓度依次为:
的物质的量浓度依次为: 、
、 、
、 ,则
,则
___________  。
。
(4)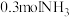 中含有质子数与
中含有质子数与___________ 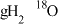 分子中所含质子数相等。
分子中所含质子数相等。
(5) 溶液中
溶液中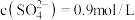 ,则
,则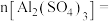
___________ 。
(1)某气体氧化物的化学式为
 ,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为
,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为(2)标准状况下有①
 ,②
,② 个
个 分子,③
分子,③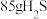 三种气体,对这三种气体的物质的量从大到小的顺序是
三种气体,对这三种气体的物质的量从大到小的顺序是(3)某混合盐溶液中含有离子:
 、
、 、
、 、
、 ,测得
,测得 、
、 和
和 的物质的量浓度依次为:
的物质的量浓度依次为: 、
、 、
、 ,则
,则
 。
。(4)
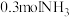 中含有质子数与
中含有质子数与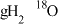 分子中所含质子数相等。
分子中所含质子数相等。(5)
 溶液中
溶液中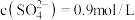 ,则
,则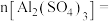
您最近半年使用:0次
名校
8 . 下列叙述正确的是
A. 水中溶解了 水中溶解了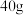  后,所得溶液浓度为 后,所得溶液浓度为 |
B. 的 的 溶液中 溶液中 的个数为 的个数为 |
C.将 (标准状况) (标准状况) 气体溶于水制成 气体溶于水制成 溶液,其物质的量浓度为 溶液,其物质的量浓度为 |
D.配制 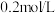 的 的 溶液,需用 溶液,需用 胆矾 胆矾 |
您最近半年使用:0次
名校
解题方法
9 . 用溶质质量分数为98%的浓硫酸(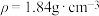 )配制
)配制 稀硫酸,下列操作正确的是
稀硫酸,下列操作正确的是
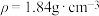 )配制
)配制 稀硫酸,下列操作正确的是
稀硫酸,下列操作正确的是| A.将蒸馏水缓慢注入盛有一定量浓硫酸的烧杯中,并不断搅拌至冷却 |
| B.必须的定量仪器有250mL容量瓶和托盘天平 |
| C.量取浓硫酸的体积为25.0mL |
| D.先在容量瓶中加入适量水,将量好的浓硫酸注入容量瓶,加水定容 |
您最近半年使用:0次
10 . 下列说法正确的是
| A.两种物质的物质的量相同,则它们在标况下的体积相同 |
B.0.5L1mol/L 溶液与0.2L1mol/LKCl溶液中的 溶液与0.2L1mol/LKCl溶液中的 的数目之比为15:2 的数目之比为15:2 |
| C.40gNaOH固体溶解在1L水中,所得溶液中溶质的物质的量浓度为1mol/L |
| D.标准状况下气体摩尔体积约为22.4L |
您最近半年使用:0次



