1 . CO与H2S反应可以制得COS,其化学方程式为 。NA为阿伏加德罗常数的值,下列有关说法正确的是
。NA为阿伏加德罗常数的值,下列有关说法正确的是
 。NA为阿伏加德罗常数的值,下列有关说法正确的是
。NA为阿伏加德罗常数的值,下列有关说法正确的是A.2.8g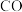 中含有的中子数为1.4NA 中含有的中子数为1.4NA |
B.pH=3的H2S溶液中 的数目为0.001NA 的数目为0.001NA |
C.0.1molCOS中 键数目为0.4NA 键数目为0.4NA |
| D.生成2.24LH2(标准状况),转移电子数目为0.4NA |
您最近一年使用:0次
解题方法
2 . 铅(Pb)元素的主要化合价有+2价和+4价,溶液中铅为+2价(Pb2+或 ,铅单质及其化合物在日常生活和工业生产中具有非常广泛的用途。
,铅单质及其化合物在日常生活和工业生产中具有非常广泛的用途。
(1)Pb3O4 俗名红丹,在涂料工业中用作防锈颜料,Pb3O4中+2价铅和+4价铅的原子个数之比为
(2)Pb、PbO2可用于制造铅蓄电池,铅蓄电池工作时的反应方程式为:Pb+PbO2+2H2SO4=2PbSO4+2H2O,该反应中还原产物为
(3)工业上利用铅渣(主要成分是PbO、Pb,以及少量不溶于硝酸的杂质)生产PbSO4的流程如图:
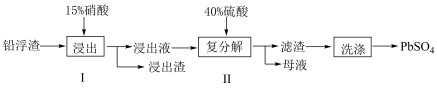
已知步骤1有NO产生,试写出Pb与硝酸反应的化学方程式
(4)血铅是指血液中铅元素的含量。血铅超标会引起机体的神经系统、血液系统、消化系统的一系列异常表现。某人血液中铅的浓度为0.4μg/mL,若转化为物质的量浓度为
您最近一年使用:0次
名校
解题方法
3 . 微观探析是认识物质的一种途径。设 为阿伏加德罗常数,下列有关说法正确的是
为阿伏加德罗常数,下列有关说法正确的是
 为阿伏加德罗常数,下列有关说法正确的是
为阿伏加德罗常数,下列有关说法正确的是A.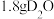 中含有的中子数目为 中含有的中子数目为 |
B.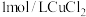 溶液中含有 溶液中含有 的数目小于 的数目小于 |
C. 与 与 的混合物中含有的分子数为 的混合物中含有的分子数为 |
D.25℃,101kPa, 与NaOH溶液完全反应,转移电子数目为 与NaOH溶液完全反应,转移电子数目为 |
您最近一年使用:0次
2024-03-06更新
|
855次组卷
|
4卷引用:2024届广东省汕头市高三下学期一模化学试题
4 . 设 表示阿伏加德罗常数的值,下列说法
表示阿伏加德罗常数的值,下列说法错误 的是
 表示阿伏加德罗常数的值,下列说法
表示阿伏加德罗常数的值,下列说法A.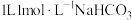 溶液中所含氧原子数目为 溶液中所含氧原子数目为 |
B.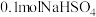 固体中,阴、阳离子的数目之和为 固体中,阴、阳离子的数目之和为 |
C. 单质 单质 与足量 与足量 反应,转移电子数为 反应,转移电子数为 |
D.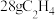 和 和 混合物中含有C原子数为 混合物中含有C原子数为 |
您最近一年使用:0次
名校
解题方法
5 . 下列溶液中溶质的物质的量浓度为 的是
的是
 的是
的是A.将 溶解于 溶解于 水中配成 水中配成 溶液 溶液 |
B.常温常压下,将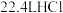 气体溶于水配成 气体溶于水配成 的盐酸 的盐酸 |
C.将 胆矾溶于水中配成 胆矾溶于水中配成 溶液 溶液 |
D.从 的 的 溶液中取出 溶液中取出 的溶液 的溶液 |
您最近一年使用:0次
名校
解题方法
6 . VLK2SO4溶液中,含有K+mg,则溶液中 的物质的量浓度为
的物质的量浓度为
 的物质的量浓度为
的物质的量浓度为A. mol/L mol/L | B.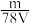 mol/L mol/L | C.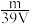 mol/L mol/L | D.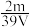 mol/L mol/L |
您最近一年使用:0次
名校
解题方法
7 . 一定物质的量浓度溶液的配制在生产与科学研究中有着广泛的应用。
(1)容量瓶是配制溶液所用的主要仪器。容量瓶上需标有___________ (填序号)。
①温度②浓度③容量④压强⑤刻度线⑥酸式或碱式
(2)“84消海液”是生活中常用的杀菌消毒剂。已知某“84消毒液”有效成分的浓度为 ,该“84消毒液”有效成分的物质的量浓度为
,该“84消毒液”有效成分的物质的量浓度为___________ 。写出其有效成分在水中的电离方程式:___________ 。现欲用 固体配制
固体配制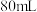 ,上述消毒溶液,除了烧杯、玻璃棒外,还必需的玻璃仪器有
,上述消毒溶液,除了烧杯、玻璃棒外,还必需的玻璃仪器有___________ 、___________ ,需要称量 固体
固体___________ g。
(3)下图是配制溶液的几个关键实验步骤的操作。
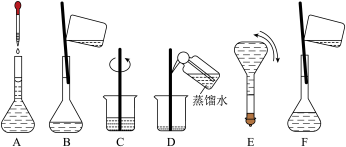
将上述实验步骤A~F按实验过程先后次序排列___________ 。C和F中玻璃棒的作用分别是___________ 和___________ 。
(4)若所配制的次氯酸钠溶液浓度偏低,原因可能是___________(填序号)。
(5)现用质量分数为 、密度为
、密度为 的浓硫酸来配制
的浓硫酸来配制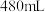 、
、 的稀硫酸。该浓硫酸的物质的量浓度为
的稀硫酸。该浓硫酸的物质的量浓度为___________  ,计算所需浓硫酸的体积为
,计算所需浓硫酸的体积为___________  。
。
(1)容量瓶是配制溶液所用的主要仪器。容量瓶上需标有
①温度②浓度③容量④压强⑤刻度线⑥酸式或碱式
(2)“84消海液”是生活中常用的杀菌消毒剂。已知某“84消毒液”有效成分的浓度为
 ,该“84消毒液”有效成分的物质的量浓度为
,该“84消毒液”有效成分的物质的量浓度为 固体配制
固体配制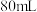 ,上述消毒溶液,除了烧杯、玻璃棒外,还必需的玻璃仪器有
,上述消毒溶液,除了烧杯、玻璃棒外,还必需的玻璃仪器有 固体
固体(3)下图是配制溶液的几个关键实验步骤的操作。

将上述实验步骤A~F按实验过程先后次序排列
(4)若所配制的次氯酸钠溶液浓度偏低,原因可能是___________(填序号)。
| A.配制前,容量瓶中有少量蒸馏水 |
| B.固体溶解后将溶液立即传移到容量瓶中 |
| C.定容时水多、超过刻度线,用胶头滴管吸出 |
| D.定容时,俯视溶液的凹液面 |
(5)现用质量分数为
 、密度为
、密度为 的浓硫酸来配制
的浓硫酸来配制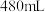 、
、 的稀硫酸。该浓硫酸的物质的量浓度为
的稀硫酸。该浓硫酸的物质的量浓度为 ,计算所需浓硫酸的体积为
,计算所需浓硫酸的体积为 。
。
您最近一年使用:0次
名校
8 . 已知盐酸受热易挥发,要使1L 1mol·L−1盐酸的物质的量浓度扩大一倍,下列方法中可行的是
| A.加热溶液,浓缩至0.5L |
| B.加入2L的1mol·L−1盐酸混合均匀 |
| C.先加入0.2L的10 mol·L−1盐酸,再稀释至1.5L |
| D.通入22.4L HCl气体(标况) |
您最近一年使用:0次
9 . “84消毒液”是一种以NaClO为主的高效消毒剂。某“84消毒液”瓶体部分标签如图1所示,该“84消毒液”通常稀释100倍(体积之比)后使用。请回答下列问题:

(1)配制100g24%84消毒液需要水多少______ g.需要的玻璃仪器有烧杯,玻璃棒______ (填名称)
(2)此“84消毒液”的物质的量浓度约为______ mol/L。(计算结果保留一位小数)
(3)某同学量取100mL此“84消毒液”,按说明要求稀释后用于消毒,则稀释后的溶液中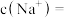
______ mol/L。
该同学参阅“84消毒液”的配方,欲用NaClO固体配制500mL含NaClO质量分数为24%的消毒液。
(4)如图2所示的仪器中配制溶液需要使用的是______ (填仪器序号),
(5)下列操作中,容量瓶不具备的功能是______ (填序号)。
a.配制一定体积准确浓度的标准溶液 b.贮存溶液
c.测量容量瓶规格以下的任意体积的溶液 d.准确稀释某一浓度的溶液
e.用来加热溶解固体溶质
(6)若实验遇下列情况,导致所配溶液的物质的量浓度偏高的是______。(填序号)。

(1)配制100g24%84消毒液需要水多少
(2)此“84消毒液”的物质的量浓度约为
(3)某同学量取100mL此“84消毒液”,按说明要求稀释后用于消毒,则稀释后的溶液中
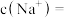
该同学参阅“84消毒液”的配方,欲用NaClO固体配制500mL含NaClO质量分数为24%的消毒液。
(4)如图2所示的仪器中配制溶液需要使用的是
(5)下列操作中,容量瓶不具备的功能是
a.配制一定体积准确浓度的标准溶液 b.贮存溶液
c.测量容量瓶规格以下的任意体积的溶液 d.准确稀释某一浓度的溶液
e.用来加热溶解固体溶质
(6)若实验遇下列情况,导致所配溶液的物质的量浓度偏高的是______。(填序号)。
| A.定容时俯视刻度线 | B.转移前,容量瓶内有蒸馏水 |
| C.未冷至室温就转移定容 | D.定容时水多用胶头滴管吸出 |
您最近一年使用:0次
名校
解题方法
10 . 现有下列物质:①Na2O2 ②NH4Cl ③HNO3 ④CO2 ⑤铜 ⑥FeCl3溶液 ⑦蔗糖
(1)上述状态的物质中,能导电有_______ (填序号)。
(2)③在水溶液中的电离方程式为_______ 。
(3)制作印刷电路板时⑥腐蚀铜的离子方程式为_______ ,反应中Fe3+被_______ (填“氧化”或“还原”)。
(4)标准状况下,由CO和CO2组成的混合气体33.6L,质量为56.4g,则该混合气体中,CO与CO2的物质的量之比为_______ 。
(5)⑤和③可发生反应:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,反应中若消耗8mol/L的硝酸 100 mL,则转移电子的数目为_______ 。
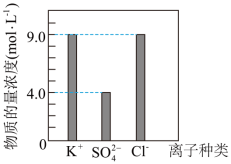
(6)某学习兴趣小组用KCl、K2SO4、NH4Cl固体配制了500mL无土栽培用的营养液。测得该营养液中部分离子的浓度柱状图如图所示,则该营养液中NH4Cl的物质的量为_______ 。
(1)上述状态的物质中,能导电有
(2)③在水溶液中的电离方程式为
(3)制作印刷电路板时⑥腐蚀铜的离子方程式为
(4)标准状况下,由CO和CO2组成的混合气体33.6L,质量为56.4g,则该混合气体中,CO与CO2的物质的量之比为
(5)⑤和③可发生反应:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,反应中若消耗8mol/L的硝酸 100 mL,则转移电子的数目为
(6)某学习兴趣小组用KCl、K2SO4、NH4Cl固体配制了500mL无土栽培用的营养液。测得该营养液中部分离子的浓度柱状图如图所示,则该营养液中NH4Cl的物质的量为

您最近一年使用:0次



