现有下列物质:①Na2O2 ②NH4Cl ③HNO3 ④CO2 ⑤铜 ⑥FeCl3溶液 ⑦蔗糖
(1)上述状态的物质中,能导电有_______ (填序号)。
(2)③在水溶液中的电离方程式为_______ 。
(3)制作印刷电路板时⑥腐蚀铜的离子方程式为_______ ,反应中Fe3+被_______ (填“氧化”或“还原”)。
(4)标准状况下,由CO和CO2组成的混合气体33.6L,质量为56.4g,则该混合气体中,CO与CO2的物质的量之比为_______ 。
(5)⑤和③可发生反应:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,反应中若消耗8mol/L的硝酸 100 mL,则转移电子的数目为_______ 。
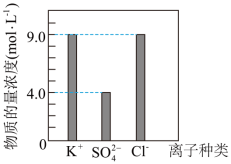
(6)某学习兴趣小组用KCl、K2SO4、NH4Cl固体配制了500mL无土栽培用的营养液。测得该营养液中部分离子的浓度柱状图如图所示,则该营养液中NH4Cl的物质的量为_______ 。
(1)上述状态的物质中,能导电有
(2)③在水溶液中的电离方程式为
(3)制作印刷电路板时⑥腐蚀铜的离子方程式为
(4)标准状况下,由CO和CO2组成的混合气体33.6L,质量为56.4g,则该混合气体中,CO与CO2的物质的量之比为
(5)⑤和③可发生反应:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,反应中若消耗8mol/L的硝酸 100 mL,则转移电子的数目为
(6)某学习兴趣小组用KCl、K2SO4、NH4Cl固体配制了500mL无土栽培用的营养液。测得该营养液中部分离子的浓度柱状图如图所示,则该营养液中NH4Cl的物质的量为

更新时间:2024-01-03 16:07:36
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】将一定质量的铜片加入到20 mL某浓度的浓硝酸中,充分反应后,铜片全部溶解,并收集到标准状况下的混合气体共896mL(假设气体中只有NO和NO2)。向反应后所得溶液中逐滴滴加1mol/L的NaOH溶液,产生沉淀质量与加入NaOH溶液体积(单位:mL)的关系如图所示。回答下列问题:
(1)B点所表示溶液中只含一种溶质,该物质是_______ (填化学式)。
(2)收集的气体中,NO2的物质的量为______ mol。
(3)铜片的质量为______ g。
(4)原浓硝酸的浓度为________________ mol/L。

(1)B点所表示溶液中只含一种溶质,该物质是
(2)收集的气体中,NO2的物质的量为
(3)铜片的质量为
(4)原浓硝酸的浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题
(1)某硫酸钠溶液50mL中含有1.15gNa+,取出10mL稀释至20mL后所得溶液中 的物质的量浓度是
的物质的量浓度是_______ 。
(2)12.4g Na2X中含有0.4mol Na+,则该物质的化学式为_______ 。
(3)室温下,某容积固定的密闭容器由可移动的活塞隔成A、B两室,分别向A、B两室充入H2、O2的混合气体和1mol空气,此时活塞的位置如图所示。

①A室混合气体所含分子总数约为_______ 。
②实验测得A室混合气体的质量为34g,则该混合气体的密度是同温同压下氦气密度的_______ 倍。
③若将A室H2、O2的混合气体点燃引爆,恢复原温度后,最终活塞停留的位置在_______ 刻度,容器内气体压强与反应前气体压强之比为_______ 。
(1)某硫酸钠溶液50mL中含有1.15gNa+,取出10mL稀释至20mL后所得溶液中
 的物质的量浓度是
的物质的量浓度是(2)12.4g Na2X中含有0.4mol Na+,则该物质的化学式为
(3)室温下,某容积固定的密闭容器由可移动的活塞隔成A、B两室,分别向A、B两室充入H2、O2的混合气体和1mol空气,此时活塞的位置如图所示。

①A室混合气体所含分子总数约为
②实验测得A室混合气体的质量为34g,则该混合气体的密度是同温同压下氦气密度的
③若将A室H2、O2的混合气体点燃引爆,恢复原温度后,最终活塞停留的位置在
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】完成下列问题
(1)实验室中将0.1 mol Na2O2加入水配制成溶液,写出相应的化学反应方程式___________ 。
(2)向(1)的溶液中加入一定量的NaHCO3固体,所得溶液中缓慢滴加一定浓度的盐酸,测得生成CO2的体积(已换算为标准状况下)与所加盐酸体积之间的关系如图所示。

①向(1)的溶液中加入的NaHCO3,固体质量为___________ g。
②滴加的盐酸物质的量浓度为___________ mol/L。
③图中:a=___________ 。
(1)实验室中将0.1 mol Na2O2加入水配制成溶液,写出相应的化学反应方程式
(2)向(1)的溶液中加入一定量的NaHCO3固体,所得溶液中缓慢滴加一定浓度的盐酸,测得生成CO2的体积(已换算为标准状况下)与所加盐酸体积之间的关系如图所示。

①向(1)的溶液中加入的NaHCO3,固体质量为
②滴加的盐酸物质的量浓度为
③图中:a=
您最近一年使用:0次
填空题
|
适中
(0.65)
真题
解题方法
【推荐1】铁是应用最广泛的金属,铁的卤化物、氧化物以及高价铁的含氧酸盐均为重要化合物。
(1)要确定铁的某氯化物FeClx的化学式,可用离子交换和滴定的方法。实验中称取0.54g的FeClx样品,溶解后先进行阳离子交换预处理,再通过含有饱和OH-的阴离子交换柱,使Cl-和OH-发生交换。交换完成后,流出溶液的OH-用0.40mol.L-1的盐酸滴定,滴至终点时消耗盐酸25.0mL。计算该样品中氯的物质的量,并求出FeClx中x值:_____________
(列出计算过程);
(2)现有一含有FeCl2和FeCl3的混合物样品,采用上述方法测得n(Fe):n(Cl)=1:2.1,则该样品中FeCl3的物质的量分数为________ 。在实验室中,FeCl2可用铁粉和________ 盐酸反应制备,FeCl3可用铁粉和________ 反应制备;
(3)FeCl3与氢碘酸反应时可生成棕色物质,该反应的离子方程式为______________________
(4)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3与KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式为__________________________
与MnO2-Zn电池类似,K2FeO4-Zn也可以组成碱性电池,K2FeO4在电池中作为正极材料,其电极反应式为_____________________________________ ,该电池总反应的离子方程式为_____________________________________________ 。
(1)要确定铁的某氯化物FeClx的化学式,可用离子交换和滴定的方法。实验中称取0.54g的FeClx样品,溶解后先进行阳离子交换预处理,再通过含有饱和OH-的阴离子交换柱,使Cl-和OH-发生交换。交换完成后,流出溶液的OH-用0.40mol.L-1的盐酸滴定,滴至终点时消耗盐酸25.0mL。计算该样品中氯的物质的量,并求出FeClx中x值:
(列出计算过程);
(2)现有一含有FeCl2和FeCl3的混合物样品,采用上述方法测得n(Fe):n(Cl)=1:2.1,则该样品中FeCl3的物质的量分数为
(3)FeCl3与氢碘酸反应时可生成棕色物质,该反应的离子方程式为
(4)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3与KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式为
与MnO2-Zn电池类似,K2FeO4-Zn也可以组成碱性电池,K2FeO4在电池中作为正极材料,其电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。某工程 师为了从使用过的腐蚀废液中回收铜,并重新获得FeCl3溶液,准备采用下列步骤:

(1)写出FeCl3溶液与Cu反应的离子方程式___________ ,若Fe和Cu及稀硫酸构成原电池,_______ 可做负极材料。可通过向滤液中加入________ (填化学式)溶液来检验Fe3+的存在,现象是__________ 。
(2)写出上图步骤③相关反应的化学方程式:③____________ 。C还可以用______ (填化学式),用这种物质反应后不引入新的杂质。
(3)请写出焊接钢轨时发生反应的化学方程式_______________ 。

(1)写出FeCl3溶液与Cu反应的离子方程式
(2)写出上图步骤③相关反应的化学方程式:③
(3)请写出焊接钢轨时发生反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】金属铁是应用广泛,铁的卤化物、氧化物以及高价铁的含氧酸盐均为重要化合物。
(1)要确定铁的某氯化物FeClx的化学式,可利用离子交换和滴定的方法。实验中称取3.25g的FeClx样品,溶解后先进行阳离子交换预处理,再通过含有饱和OH-的阴离子交换柱,使Cl-和OH-发生交换。交换完成后,流出溶液的OH-用1.0 mol·L-1的盐酸中和滴定,正好中和时消耗盐酸60.0mL。计算该样品中氯的物质的量,并求出FeClx中x的值:__________________ (列出计算过程)。
(2)现有一含有FeCl2和FeCl3的混合物样品,采用上述方法测得n(Fe)∶n(Cl) = 1∶2.8,则该样品中FeCl3的物质的量分数为___________________________________________ 。
(3)把SO2气体通入FeCl3溶液中,发生反应的离子方程式为_______________________ 。
(4)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3和KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式为_____________________________________ ;与MnO2—Zn电池类似,K2FeO4—Zn也可以组成碱性电池,其中Zn极的电极反应式为________________________ ,K2FeO4的电极反应式为________________________________________ 。
(1)要确定铁的某氯化物FeClx的化学式,可利用离子交换和滴定的方法。实验中称取3.25g的FeClx样品,溶解后先进行阳离子交换预处理,再通过含有饱和OH-的阴离子交换柱,使Cl-和OH-发生交换。交换完成后,流出溶液的OH-用1.0 mol·L-1的盐酸中和滴定,正好中和时消耗盐酸60.0mL。计算该样品中氯的物质的量,并求出FeClx中x的值:
(2)现有一含有FeCl2和FeCl3的混合物样品,采用上述方法测得n(Fe)∶n(Cl) = 1∶2.8,则该样品中FeCl3的物质的量分数为
(3)把SO2气体通入FeCl3溶液中,发生反应的离子方程式为
(4)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3和KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】铁及其化合物是重要的化学物质,如天然磁石中含有较多的Fe3O4、三水合草酸合铁(Ⅲ)酸钾{K3[Fe(C2O4)3]·3H2O,呈绿色,可溶于水,难溶于乙醇,见光易分解}常用于化学光量计、绿矾(FeSO4·7H2O)是常用的还原剂。回答下列问题:
(1)电子工业中,常用氯化铁溶液腐蚀铜制造印刷电路板,该原理的离子方程式为_____ 。
(2)根据化合价及元素的性质,Na2S5可以改写为Na2S·4S、Fe3O4可以改写为FeO·Fe2O3,则Fe3Cl8可以改写为_____ 、Fe3I8可以改写为_____ 。
(3)可通过下列两个步骤制备三水合草酸合铁(Ⅲ)酸钾晶体。
步骤i:向盛有3.00g黄色晶体FeC2O4·2H2O的烧杯中,加入10.00mLK2C2O4溶液,加热至40℃左右,缓慢滴入过量的H2O2,一段时间后,出现红褐色沉淀。
步骤ii:加热至沸腾,分两次缓慢加入8.00~9.00mLH2C2O4溶液,至沉淀溶解,得到绿色溶液。加热浓缩、加入无水乙醇、结晶,抽滤干燥得7.860g三水合草酸合铁(III)酸钾晶体。
①步骤ⅰ中,生成三草酸合铁酸钾与另一种铁的化合物,该化合物为_____ (填化学式)。
②步骤ⅱ加入无水乙醇的目的是_____ 。
③实验小组完成实验后发现产率偏低,其主要原因可能是_____ 。
(4)8.34gFeSO4·7H2O(Mr=278)样品隔绝空气受热分解生成多种化合物过程的热重曲线(残留样品质量随温度变化的曲线)如图所示。
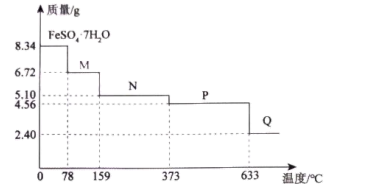
①温度为100℃时,固体物质M的化学式为_____ 。
②在隔绝空气的条件下,由P得到Q的化学方程式为_____ 。
(1)电子工业中,常用氯化铁溶液腐蚀铜制造印刷电路板,该原理的离子方程式为
(2)根据化合价及元素的性质,Na2S5可以改写为Na2S·4S、Fe3O4可以改写为FeO·Fe2O3,则Fe3Cl8可以改写为
(3)可通过下列两个步骤制备三水合草酸合铁(Ⅲ)酸钾晶体。
步骤i:向盛有3.00g黄色晶体FeC2O4·2H2O的烧杯中,加入10.00mLK2C2O4溶液,加热至40℃左右,缓慢滴入过量的H2O2,一段时间后,出现红褐色沉淀。
步骤ii:加热至沸腾,分两次缓慢加入8.00~9.00mLH2C2O4溶液,至沉淀溶解,得到绿色溶液。加热浓缩、加入无水乙醇、结晶,抽滤干燥得7.860g三水合草酸合铁(III)酸钾晶体。
①步骤ⅰ中,生成三草酸合铁酸钾与另一种铁的化合物,该化合物为
②步骤ⅱ加入无水乙醇的目的是
③实验小组完成实验后发现产率偏低,其主要原因可能是
(4)8.34gFeSO4·7H2O(Mr=278)样品隔绝空气受热分解生成多种化合物过程的热重曲线(残留样品质量随温度变化的曲线)如图所示。

①温度为100℃时,固体物质M的化学式为
②在隔绝空气的条件下,由P得到Q的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】下列离子方程式正确的是________ 。
A.稀硫酸与铁丝制取氢气: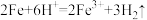
B.Cu片投入到FeCl3溶液中:Cu+2Fe3+=Cu2++2Fe2+
C.将少量Na放入水中:Na+H2O=Na++OH-+H2↑
D.氢氧化钡溶液与硫酸反应:OH-+H+=H2O
E.向澄清石灰水中通入少量二氧化碳:Ca2++2OH-+CO2=CaCO3↓+H2O
F.碳酸氢钠溶液与足量盐酸反应:2H++CO =H2O+CO2↑
=H2O+CO2↑
G.氧化钠与水反应:Na2O+H2O=2OH-+2Na+
H.将氧化钡与稀硫酸混合: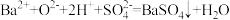
I.碳酸钙与稀盐酸制备二氧化碳:
J.CuSO4溶液中滴加Ba(OH)2溶液:Cu2++2OH-=Cu(OH)2↓
K.将铝片插入硝酸银溶液中: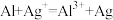
L.铁投入稀硫酸中:2Fe+6H+=2Fe3++3H2↑
A.稀硫酸与铁丝制取氢气:
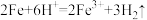
B.Cu片投入到FeCl3溶液中:Cu+2Fe3+=Cu2++2Fe2+
C.将少量Na放入水中:Na+H2O=Na++OH-+H2↑
D.氢氧化钡溶液与硫酸反应:OH-+H+=H2O
E.向澄清石灰水中通入少量二氧化碳:Ca2++2OH-+CO2=CaCO3↓+H2O
F.碳酸氢钠溶液与足量盐酸反应:2H++CO
 =H2O+CO2↑
=H2O+CO2↑G.氧化钠与水反应:Na2O+H2O=2OH-+2Na+
H.将氧化钡与稀硫酸混合:
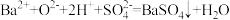
I.碳酸钙与稀盐酸制备二氧化碳:

J.CuSO4溶液中滴加Ba(OH)2溶液:Cu2++2OH-=Cu(OH)2↓
K.将铝片插入硝酸银溶液中:
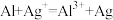
L.铁投入稀硫酸中:2Fe+6H+=2Fe3++3H2↑
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】化学与我们的生活、生产、环境、资源利用等息息相关。回答下列问题:
(1)大气中下列气体含量的升高会对环境产生一定的影响,用物质的序号填空,过量会导致温室效应加剧的主要物质是_______ ,会造成酸雨的物质是_______ ,会导致光化学烟雾的物质是_______ 。
①二氧化碳 ②二氧化硫 ③氮氧化物NOx
(2)电子工业常用质量分数为30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。写出FeCl3溶液与铜反应的离子方程式_______ 。
(3)饮用水消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一,漂白粉是常用的消 毒剂,其有效成分是_______ (填化学式)。Cl2是传统的自来水消毒剂,而ClO2是新型的自来水消毒剂,这两种消毒剂消毒完成后,氯元素均以Cl—形式存在。现要消毒1.00 m3生活污水,分别用Cl2和ClO2来消毒处理,所耗Cl2与ClO2的质量比值为 _______ (保留小数点后2位)。
(1)大气中下列气体含量的升高会对环境产生一定的影响,用物质的序号填空,过量会导致温室效应加剧的主要物质是
①二氧化碳 ②二氧化硫 ③氮氧化物NOx
(2)电子工业常用质量分数为30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。写出FeCl3溶液与铜反应的离子方程式
(3)饮用水消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一,漂白粉是常用的消 毒剂,其有效成分是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)Na2SiO3的水溶液俗称______________ ,是制备硅胶和木材防火剂的原料。
(2)许多人喜欢佩戴玉石饰品。玉石的主要成分基本属于硅酸盐,例如和田玉(Ca2Mg5H2Si8O24)可表示为氧化物形式2CaO·5MgO·8SiO2·H2O,则南阳玉(CaAl2Si2O8)表示为氧化物形式是________________ 。
(3)光导纤维在强碱性条件下容易发生“断路”,试用离子方程式解释其原因_____________________________________________ 。
(4)蔗糖与浓硫酸反应生成的黑色(单质)物质会继续与浓硫酸作用产生两种气体,当转移2mol电子时,生成标准状况下的气体共_______ L。
(2)许多人喜欢佩戴玉石饰品。玉石的主要成分基本属于硅酸盐,例如和田玉(Ca2Mg5H2Si8O24)可表示为氧化物形式2CaO·5MgO·8SiO2·H2O,则南阳玉(CaAl2Si2O8)表示为氧化物形式是
(3)光导纤维在强碱性条件下容易发生“断路”,试用离子方程式解释其原因
(4)蔗糖与浓硫酸反应生成的黑色(单质)物质会继续与浓硫酸作用产生两种气体,当转移2mol电子时,生成标准状况下的气体共
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】物质的量是高中化学常用的物理量,请完成以下有关计算:
(1)2.3 g乙醇含有的氢原子的物质的量为____________ ,含有的共价键的物质的量为_________ ,其中所含羟基的电子的物质的量为_________ 。
(2)某条件下,8 g氧气所占的体积为6 L,则在该条件下的气体摩尔体积为____________ 。
(3)100 mL硫酸铝溶液中c(Al3+) =0.20mol/L(不考虑水解因素),则其中n(SO )=
)=____________ 。
(4)9.5 g某二价金属的氯化物中含有0.2 mol C1-,此氯化物的摩尔质量为_____________ 。
(5)6.72 LCO(标准状况)与一定量的Fe2O3恰好完全反应(生成Fe与CO2)后,生成Fe的质量为__________ 。转移的电子的物质的量是_____________ 。
(1)2.3 g乙醇含有的氢原子的物质的量为
(2)某条件下,8 g氧气所占的体积为6 L,则在该条件下的气体摩尔体积为
(3)100 mL硫酸铝溶液中c(Al3+) =0.20mol/L(不考虑水解因素),则其中n(SO
 )=
)=(4)9.5 g某二价金属的氯化物中含有0.2 mol C1-,此氯化物的摩尔质量为
(5)6.72 LCO(标准状况)与一定量的Fe2O3恰好完全反应(生成Fe与CO2)后,生成Fe的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】 MnO2是一种重要的化工原料,由MnO2制备系列物质的过程如图所示:

回答下列问题:
(1)上述反应中MnO2作氧化剂的是 (填序号,下同),作催化剂的是 。
(2)写出上述反应中属于离子反应的离子方程式: 。
(3)相同条件下生成等体积的O2,反应③和④转移的电子数之比为 。
(4)反应⑤中氧化剂与还原剂的物质的量之比为 。
(5)反应②的化学方程式为3Cl2+2HgO Hg+HgCl2+2Cl2O,若生成8.7gCl2O,则转移的电子的物质的量为 mol
Hg+HgCl2+2Cl2O,若生成8.7gCl2O,则转移的电子的物质的量为 mol

回答下列问题:
(1)上述反应中MnO2作氧化剂的是 (填序号,下同),作催化剂的是 。
(2)写出上述反应中属于离子反应的离子方程式: 。
(3)相同条件下生成等体积的O2,反应③和④转移的电子数之比为 。
(4)反应⑤中氧化剂与还原剂的物质的量之比为 。
(5)反应②的化学方程式为3Cl2+2HgO
 Hg+HgCl2+2Cl2O,若生成8.7gCl2O,则转移的电子的物质的量为 mol
Hg+HgCl2+2Cl2O,若生成8.7gCl2O,则转移的电子的物质的量为 mol
您最近一年使用:0次



