1 .  为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
A.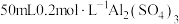 溶液中 溶液中 数目为 数目为 |
B.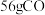 与 与 的混合气体中原子数目为 的混合气体中原子数目为 |
C.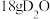 中共价键数目为 中共价键数目为 |
D.常温常压下,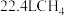 中电子数目为 中电子数目为 |
您最近半年使用:0次
2 . 请按要求填空:
(1)12.4g Na2X含有0.4mol Na+,Na2X的摩尔质量为___________ 。
(2)相同状况下,一定体积的气态氢化物H2X的质量是等体积NH3的2倍。则X的相对原子质量为___________ 。
(3)气态化合物A的化学式可以表示为OxFy,已知同温同压下10mL A受热完全分解生成15mL O2和10mL F2,则A的化学式为___________ 。
(4)0.5L 0.5mol/L FeCl3溶液中的Cl-的物质的量浓度为___________ 。
(5)质量分数为98%,密度为1.84g·cm-3的某浓硫酸,溶质的物质的量浓度为___________ 。
(6)a个X原子的总质量为b g,则X的相对原子质量可表示为___________ 。
(1)12.4g Na2X含有0.4mol Na+,Na2X的摩尔质量为
(2)相同状况下,一定体积的气态氢化物H2X的质量是等体积NH3的2倍。则X的相对原子质量为
(3)气态化合物A的化学式可以表示为OxFy,已知同温同压下10mL A受热完全分解生成15mL O2和10mL F2,则A的化学式为
(4)0.5L 0.5mol/L FeCl3溶液中的Cl-的物质的量浓度为
(5)质量分数为98%,密度为1.84g·cm-3的某浓硫酸,溶质的物质的量浓度为
(6)a个X原子的总质量为b g,则X的相对原子质量可表示为
您最近半年使用:0次
3 . 设NA为阿伏伽德罗常数的值,下列说法正确的是
| A.标准状况下,22.4L氯气与56g铁粉点燃充分反应,转移的电子数为3NA |
| B.0.5mol/L的MgCl2溶液中Cl-个数与78g过氧化钠中所含的阴离子数目相等 |
| C.常温常压下,将17gNH3溶于1L水中可得1mol/L的氨水溶液 |
| D.标准状况下,2.24L的CO2和N2O混合物中所含有的原子数目为0.3NA |
您最近半年使用:0次
名校
解题方法
4 . 利用课学上学到的知识来解决生活中的问题是我们学习的重要目的。
(1)某化学实验兴趣小组自行购置了鸡蛋、食醋等生活用品,进行了如下探究。
①将鸡蛋壳(主要成分为 )泡进食醋中,发现有气泡产生,请写出该反应的离子方程式:
)泡进食醋中,发现有气泡产生,请写出该反应的离子方程式:________ 。
②同学测出从超市购买的食醋中醋酸( )含量为
)含量为 ,则食醋中醋酸含量为
,则食醋中醋酸含量为_____ 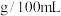 。
。
(2)如图是化学实验室浓盐酸试剂标签上的部分内容。丙同学计划用该浓盐酸配制 的稀盐酸,现实验仅需要稀盐酸
的稀盐酸,现实验仅需要稀盐酸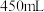 ,可供选用的仪器有:①胶头滴管:②烧瓶;③烧杯:④药匙;⑤玻璃棒。请回答下列问题:
,可供选用的仪器有:①胶头滴管:②烧瓶;③烧杯:④药匙;⑤玻璃棒。请回答下列问题:
①配制稀盐酸时,还缺少的仪器有____ 。
②经计算,配制 的稀盐酸需要量取上述浓盐酸的体积为
的稀盐酸需要量取上述浓盐酸的体积为____  (结果保留1位小数)。
(结果保留1位小数)。
③测定所配制的稀盐酸,发现其浓度大于 ,引起误差的原因可能是
,引起误差的原因可能是____ 。
A.将量取的浓盐酸倒入烧杯后,洗涤量筒,洗涤液也注入烧杯
B.定容时俯视容量瓶刻度线
C.转移溶液后,未洗涤烧杯和玻璃棒
D.定容摇匀后发现液面低于容量瓶的刻度线,再加水至刻度线
(3)某同学利用鸡蛋壳和配制好的稀盐酸溶液制备 ,查询相关书籍后,设计了如下装置测定
,查询相关书籍后,设计了如下装置测定 的相对分子质量。
的相对分子质量。
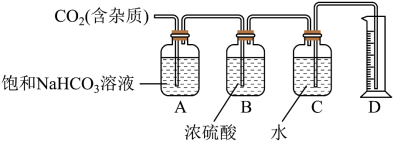
① 装置中的饱和
装置中的饱和 溶液可以吸收
溶液可以吸收__________ 。
②实验前测得 装置(含水)重量为
装置(含水)重量为 ,实验完毕后
,实验完毕后 装置(含水)重量为
装置(含水)重量为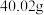 ,
, 中量筒读数为
中量筒读数为 ,已知相同条件下
,已知相同条件下 密度为
密度为 ,计算实验条件下,气体摩尔体积为
,计算实验条件下,气体摩尔体积为____ 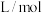 ,(保留2位小数),请根据以上数据用相对密度法计算
,(保留2位小数),请根据以上数据用相对密度法计算 的相对分子质量为
的相对分子质量为_______ (保留2位小数)。
(1)某化学实验兴趣小组自行购置了鸡蛋、食醋等生活用品,进行了如下探究。
①将鸡蛋壳(主要成分为
 )泡进食醋中,发现有气泡产生,请写出该反应的离子方程式:
)泡进食醋中,发现有气泡产生,请写出该反应的离子方程式:②同学测出从超市购买的食醋中醋酸(
 )含量为
)含量为 ,则食醋中醋酸含量为
,则食醋中醋酸含量为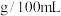 。
。(2)如图是化学实验室浓盐酸试剂标签上的部分内容。丙同学计划用该浓盐酸配制
 的稀盐酸,现实验仅需要稀盐酸
的稀盐酸,现实验仅需要稀盐酸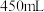 ,可供选用的仪器有:①胶头滴管:②烧瓶;③烧杯:④药匙;⑤玻璃棒。请回答下列问题:
,可供选用的仪器有:①胶头滴管:②烧瓶;③烧杯:④药匙;⑤玻璃棒。请回答下列问题:盐酸 化学纯( )( )( ) )品名:盐酸 化学式:  相对分子质量:  密度: 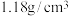 质量分数:  |
②经计算,配制
 的稀盐酸需要量取上述浓盐酸的体积为
的稀盐酸需要量取上述浓盐酸的体积为 (结果保留1位小数)。
(结果保留1位小数)。③测定所配制的稀盐酸,发现其浓度大于
 ,引起误差的原因可能是
,引起误差的原因可能是A.将量取的浓盐酸倒入烧杯后,洗涤量筒,洗涤液也注入烧杯
B.定容时俯视容量瓶刻度线
C.转移溶液后,未洗涤烧杯和玻璃棒
D.定容摇匀后发现液面低于容量瓶的刻度线,再加水至刻度线
(3)某同学利用鸡蛋壳和配制好的稀盐酸溶液制备
 ,查询相关书籍后,设计了如下装置测定
,查询相关书籍后,设计了如下装置测定 的相对分子质量。
的相对分子质量。
①
 装置中的饱和
装置中的饱和 溶液可以吸收
溶液可以吸收②实验前测得
 装置(含水)重量为
装置(含水)重量为 ,实验完毕后
,实验完毕后 装置(含水)重量为
装置(含水)重量为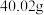 ,
, 中量筒读数为
中量筒读数为 ,已知相同条件下
,已知相同条件下 密度为
密度为 ,计算实验条件下,气体摩尔体积为
,计算实验条件下,气体摩尔体积为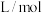 ,(保留2位小数),请根据以上数据用相对密度法计算
,(保留2位小数),请根据以上数据用相对密度法计算 的相对分子质量为
的相对分子质量为
您最近半年使用:0次
5 .  为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.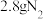 中含有质子数目为 中含有质子数目为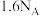 |
B.标准状况下,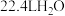 中含有共价键数目为 中含有共价键数目为 |
C.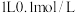 氢氧化钠溶液中含有钠离子数目为 氢氧化钠溶液中含有钠离子数目为 |
D. 与足量水充分反应,转移电子数目为 与足量水充分反应,转移电子数目为 |
您最近半年使用:0次
6 . 某兴趣小组通过下列实验探究 与
与 的氧化性强弱,并对实验原理所涉及的反应进行定性、定量研究。
的氧化性强弱,并对实验原理所涉及的反应进行定性、定量研究。
(1)探究 与
与 的氧化性强弱
的氧化性强弱
【实验 】将
】将 溶液和
溶液和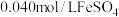 溶液(
溶液( )等体积混合,产生灰黑色沉淀,溶液呈黄色。该条件下,根据实验现象可以判断出氧化性:
)等体积混合,产生灰黑色沉淀,溶液呈黄色。该条件下,根据实验现象可以判断出氧化性:
_____  (填“>”“<”)。
(填“>”“<”)。
(2)验证反应 是可逆反应
是可逆反应
【实验Ⅱ】
①取实验 反应后的上层清液或沉淀进行实验,将表格补充完整。
反应后的上层清液或沉淀进行实验,将表格补充完整。
②根据实验数据,证明该反应为可逆反应,不需要完成表格中编号_____ 的实验。
(3)测定反应 的平衡常数
的平衡常数
测定方案:通过氧化还原滴定法可测定平衡时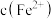 ,再根据实验
,再根据实验 反应物浓度数据计算得出
反应物浓度数据计算得出 和
和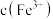 ,进而求算出平衡常数
,进而求算出平衡常数 。
。
【实验Ⅲ】室温下,待实验Ⅰ中反应达到平衡状态时,取 上层清液,用
上层清液,用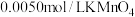 标准溶液滴定
标准溶液滴定 ,达到滴定终点记录消耗
,达到滴定终点记录消耗 标准溶液的体积。重复实验3次,平均消耗
标准溶液的体积。重复实验3次,平均消耗 标准溶液的体积为
标准溶液的体积为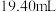 。
。
①用于盛装 标准溶液进行滴定的玻璃仪器名称为
标准溶液进行滴定的玻璃仪器名称为_____ 。
②平衡时
_____  ,平衡常数
,平衡常数
_____ 。
③若取实验 反应后的含
反应后的含 浊液进行实验Ⅱ,会使测得的平衡常数
浊液进行实验Ⅱ,会使测得的平衡常数 值
值_____ 。
A.偏大 B.偏小 C.无影响 D.无法判断
 与
与 的氧化性强弱,并对实验原理所涉及的反应进行定性、定量研究。
的氧化性强弱,并对实验原理所涉及的反应进行定性、定量研究。(1)探究
 与
与 的氧化性强弱
的氧化性强弱【实验
 】将
】将 溶液和
溶液和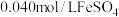 溶液(
溶液( )等体积混合,产生灰黑色沉淀,溶液呈黄色。该条件下,根据实验现象可以判断出氧化性:
)等体积混合,产生灰黑色沉淀,溶液呈黄色。该条件下,根据实验现象可以判断出氧化性:
 (填“>”“<”)。
(填“>”“<”)。(2)验证反应
 是可逆反应
是可逆反应【实验Ⅱ】
①取实验
 反应后的上层清液或沉淀进行实验,将表格补充完整。
反应后的上层清液或沉淀进行实验,将表格补充完整。| 实验编号 | 操作及现象 | 结论 |
| 1 | 取上层黄色清液,滴加 | 存在 |
| 2 | 取少量灰黑色沉淀,滴加浓硝酸,沉淀溶解,出现红棕色气体 | 存在 |
| 3 | 操作及现象是: | 存在 |
| 4 | 取上层清液,滴加 溶液,产生蓝色沉淀 溶液,产生蓝色沉淀 |
(3)测定反应
 的平衡常数
的平衡常数测定方案:通过氧化还原滴定法可测定平衡时
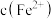 ,再根据实验
,再根据实验 反应物浓度数据计算得出
反应物浓度数据计算得出 和
和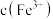 ,进而求算出平衡常数
,进而求算出平衡常数 。
。【实验Ⅲ】室温下,待实验Ⅰ中反应达到平衡状态时,取
 上层清液,用
上层清液,用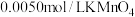 标准溶液滴定
标准溶液滴定 ,达到滴定终点记录消耗
,达到滴定终点记录消耗 标准溶液的体积。重复实验3次,平均消耗
标准溶液的体积。重复实验3次,平均消耗 标准溶液的体积为
标准溶液的体积为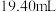 。
。①用于盛装
 标准溶液进行滴定的玻璃仪器名称为
标准溶液进行滴定的玻璃仪器名称为②平衡时

 ,平衡常数
,平衡常数
③若取实验
 反应后的含
反应后的含 浊液进行实验Ⅱ,会使测得的平衡常数
浊液进行实验Ⅱ,会使测得的平衡常数 值
值A.偏大 B.偏小 C.无影响 D.无法判断
您最近半年使用:0次
7 . 用 表示阿伏加德罗常数的值,下列叙述正确的是
表示阿伏加德罗常数的值,下列叙述正确的是
 表示阿伏加德罗常数的值,下列叙述正确的是
表示阿伏加德罗常数的值,下列叙述正确的是A. 溶解在1L水中,所得溶液中溶质的物质的量浓度为 溶解在1L水中,所得溶液中溶质的物质的量浓度为 |
B.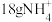 所含电子数为 所含电子数为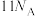 |
C. 在标准状况下的体积约为44.8L 在标准状况下的体积约为44.8L |
D.标准状况下,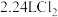 与足量铁粉反应转移的电子数为 与足量铁粉反应转移的电子数为 |
您最近半年使用:0次
名校
解题方法
8 . 用1.6mol/L某金属阳离子Rn+的盐溶液5mL,恰好将20mL0.4mol/L的硫酸盐中的硫酸根完全沉淀,则n值为
| A.1 | B.2 | C.3 | D.4 |
您最近半年使用:0次
9 . 设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A. 所含电子的数目为 所含电子的数目为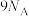 |
B. 溶液中所含 溶液中所含 的数目为 的数目为 |
C.甲醛和乙酸的混合物60g中所含碳原子的数目为 |
D. 与 与 反应生成 反应生成 时,转移电子的数目为 时,转移电子的数目为 |
您最近半年使用:0次
名校
10 . 设NA为阿伏加德罗常数的值,下列说法正确的是
| A.常温下11.2LCl2溶于水,溶液中Cl-、ClO-和HClO的微粒数之和为NA |
| B.0.1mol/L CH3COONa溶液中,含CH3COO-的数目小于0.1NA |
| C.0.1mol氯气与足量铁完全反应时转移的电子数为0.2NA |
| D.常温下,1L pH=11的Ba(OH)2溶液中含OH-的数目为0.002NA |
您最近半年使用:0次



