1 . 一种电化学还原制氨气的反应为: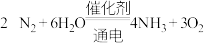 ,设
,设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
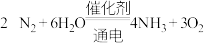 ,设
,设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.标准状况下,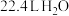 含有的分子数为 含有的分子数为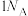 |
B.标准状况下,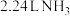 含有质子的数目为 含有质子的数目为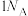 |
C. 氨水中,含有的 氨水中,含有的 分子数等于 分子数等于 |
D.每消耗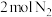 ,理论上电子转移的数目为 ,理论上电子转移的数目为 |
您最近半年使用:0次
2 . 下列叙述不正确的是
| A.将40gNaOH配成1L溶液,所得溶液的物质的量浓度为1mol/L |
| B.同温同压下,相同质量的二氧化碳和二氧化硫的体积比是16∶11 |
C.从 的NaCl溶液中取出0.5L,取出的溶液中 的NaCl溶液中取出0.5L,取出的溶液中 的物质的量浓度为 的物质的量浓度为 |
D.2.24LCO和 混合气体中含有的碳原子数目为 混合气体中含有的碳原子数目为 |
您最近半年使用:0次
3 . 物质的量是学习中重要的物理量,下列说法正确的是
A.1个 分子的质量是 分子的质量是 |
B. 的质量大于 的质量大于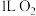 的质量 的质量 |
C.若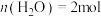 , , 中含有的电子的物质的量是 中含有的电子的物质的量是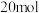 |
D.标准状况下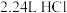 溶于 溶于 水中,溶液的物质的量浓度是 水中,溶液的物质的量浓度是 |
您最近半年使用:0次
名校
4 . NA表示阿伏加德罗常数的值。下列说法错误的是
| A.标况下,3.36L氮气所含共用电子对的数目为0.45NA |
B.0.2mol 与水恰好完全反应转移0.4mol电子 与水恰好完全反应转移0.4mol电子 |
C.1.8g的NH 中含有的电子数为1NA 中含有的电子数为1NA |
D.1 L 0.1 mol/L的 溶液中, 溶液中, 的物质的量为 的物质的量为 |
您最近半年使用:0次
5 . 下列溶液中 物质的量浓度最大的是
物质的量浓度最大的是
 物质的量浓度最大的是
物质的量浓度最大的是A. | B.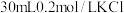 |
C. | D. |
您最近半年使用:0次
名校
6 . 如图是某硫酸试剂瓶上的部分内容。下列说法正确的是


A.该硫酸的物质的量浓度为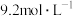 |
B.实验室需要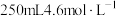 的稀硫酸,配制时应量取该硫酸 的稀硫酸,配制时应量取该硫酸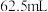 |
| C.硫酸的摩尔质量为98 |
| D.定容时仰视刻度线,会造成所配溶液浓度偏高 |
您最近半年使用:0次
名校
7 . 某无色透明溶液中可能大量存在Ag+、Ca2+、Cu2+、Fe3+、Na+中的几种。请填写下列空白。
(1)不做任何实验就可以肯定原溶液中不存在的离子是___________ 。
(2)取少量原溶液,加入过量稀盐酸、有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是___________ 。
(3)取(2)中的滤液,加入过量的碳酸钠溶液,出现白色沉淀,说明原溶液中肯定有___________ ,该过程产生白色沉淀的离子方程式为___________ 。
(4)原溶液可能大量共存的阴离子是___________(选填字母编号)。
(5)写出NaHSO4在水溶液中的电离方程式___________ 。12gNaHSO4中含有___________ 个O原子,将其溶于水配成500mL溶液,则溶液的物质的量浓度为___________ mol/L,从中取出l00mL可以消耗1mol/L的NaOH溶液___________ mL。
(1)不做任何实验就可以肯定原溶液中不存在的离子是
(2)取少量原溶液,加入过量稀盐酸、有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是
(3)取(2)中的滤液,加入过量的碳酸钠溶液,出现白色沉淀,说明原溶液中肯定有
(4)原溶液可能大量共存的阴离子是___________(选填字母编号)。
| A.OH- | B. | C. | D.Cl- |
您最近半年使用:0次
名校
解题方法
8 . NA为阿伏加德罗常数,下列叙述错误的是
| A.常温常压下,l6gO3所含的氧原子数为NA |
| B.标准状况下22.4LH2O的原子总数为3NA |
| C.1L0.5mol/LMgCl2溶液含自的Cl-数为NA |
| D.1molNa与足量O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子 |
您最近半年使用:0次
2024-01-12更新
|
81次组卷
|
2卷引用:广西柳州铁一中学2023-2024学年高一上学期段考化学试卷
名校
9 . 回答下列问题。
(1)标况下,0.1mol 所占的体积约为
所占的体积约为_______ L,所含的电子总数约为________ 个。
(2)从400mL2.0mol/L的 溶液中取出20mL,将这20mL加水稀释到100mL,所得的溶液中
溶液中取出20mL,将这20mL加水稀释到100mL,所得的溶液中 的物质的量浓度为
的物质的量浓度为___________ mol/L。
(3) 和
和 组成的固体混合物40.0g加热至质量不再变化,冷却干燥后称得残余固体质量为33.8g,则原固体混合物中
组成的固体混合物40.0g加热至质量不再变化,冷却干燥后称得残余固体质量为33.8g,则原固体混合物中 的质量分数为
的质量分数为___________ %[保留小数点后1位]。
(4)常温常压下,某钢性瓶充满 气体时质量为273.90g,改充满
气体时质量为273.90g,改充满 则质量为275.50g。若充满
则质量为275.50g。若充满 则质量是
则质量是___________ g[保留小数点后2位]。
(5)往100mL4.0mol/L的NaOH溶液中缓缓地通入2.24L 气体(标况),若忽略溶液体积的变化,所得溶液的溶质及其物质的量浓度分别为
气体(标况),若忽略溶液体积的变化,所得溶液的溶质及其物质的量浓度分别为___________ 。
(1)标况下,0.1mol
 所占的体积约为
所占的体积约为(2)从400mL2.0mol/L的
 溶液中取出20mL,将这20mL加水稀释到100mL,所得的溶液中
溶液中取出20mL,将这20mL加水稀释到100mL,所得的溶液中 的物质的量浓度为
的物质的量浓度为(3)
 和
和 组成的固体混合物40.0g加热至质量不再变化,冷却干燥后称得残余固体质量为33.8g,则原固体混合物中
组成的固体混合物40.0g加热至质量不再变化,冷却干燥后称得残余固体质量为33.8g,则原固体混合物中 的质量分数为
的质量分数为(4)常温常压下,某钢性瓶充满
 气体时质量为273.90g,改充满
气体时质量为273.90g,改充满 则质量为275.50g。若充满
则质量为275.50g。若充满 则质量是
则质量是(5)往100mL4.0mol/L的NaOH溶液中缓缓地通入2.24L
 气体(标况),若忽略溶液体积的变化,所得溶液的溶质及其物质的量浓度分别为
气体(标况),若忽略溶液体积的变化,所得溶液的溶质及其物质的量浓度分别为
您最近半年使用:0次
名校
解题方法
10 . 如图是硫酸的试剂标签上的部分内容。某次学生实验需要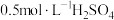 溶液480mL,若由你来配制所需溶液,请根据实验室已有的仪器和药品情况回答下列问题:
溶液480mL,若由你来配制所需溶液,请根据实验室已有的仪器和药品情况回答下列问题:
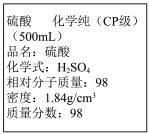
(1)该配制实验中所需98%浓硫酸的体积为__________ mL(保留一位小数)
(2)实验中除量筒、烧杯、玻璃棒外还需要的玻璃仪器___________
(3)下列操作会引起所配溶液浓度偏大的是______(填字母)。
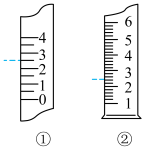
(4)温度计、量筒的一部分如图所示,下述读数(虚线所指刻度)及说法正确的是_____(填字母)。
(5)把VmL含有 和
和 的混合溶液分成两等份,一份加入含足量NaOH的溶液并加热,铵根离子完全反应生成
的混合溶液分成两等份,一份加入含足量NaOH的溶液并加热,铵根离子完全反应生成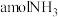 (已知
(已知 );另一份加入含
);另一份加入含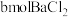 的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中
的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中 的浓度为
的浓度为__________ mol/L。
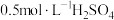 溶液480mL,若由你来配制所需溶液,请根据实验室已有的仪器和药品情况回答下列问题:
溶液480mL,若由你来配制所需溶液,请根据实验室已有的仪器和药品情况回答下列问题:
(1)该配制实验中所需98%浓硫酸的体积为
(2)实验中除量筒、烧杯、玻璃棒外还需要的玻璃仪器
(3)下列操作会引起所配溶液浓度偏大的是______(填字母)。
| A.用量筒量取浓硫酸时,仰视量筒的刻度 |
| B.向容量瓶中转移时,有少量液体溅出 |
| C.定容时仰视刻度线 |
| D.定容后倒置摇匀后再正立时,发现液面低于刻度线 |
(4)温度计、量筒的一部分如图所示,下述读数(虚线所指刻度)及说法正确的是_____(填字母)。

| A.①是量筒,读数为2.5mL | B.②是量筒,读数为2.5mL |
| C.可用②量取2.26mL的液体 | D.①是温度计,读数为2.5℃ |
(5)把VmL含有
 和
和 的混合溶液分成两等份,一份加入含足量NaOH的溶液并加热,铵根离子完全反应生成
的混合溶液分成两等份,一份加入含足量NaOH的溶液并加热,铵根离子完全反应生成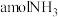 (已知
(已知 );另一份加入含
);另一份加入含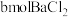 的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中
的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中 的浓度为
的浓度为
您最近半年使用:0次



