名校
解题方法
1 . 下列用于解释事实的化学用语中,不正确的是
A.Na2S溶液显碱性:S2-+2H2O H2S+2OH- H2S+2OH- |
B.K2Cr2O7溶液中含有CrO :Cr2O :Cr2O +H2O +H2O 2CrO 2CrO +2H+ +2H+ |
C.盛放NaOH溶液的试剂瓶不能用玻璃塞:2OH-+SiO2=SiO +H2O +H2O |
D.红热木炭遇浓硫酸产生刺激性气味气体:2H2SO4(浓)+C CO2↑+2SO2↑+2H2O CO2↑+2SO2↑+2H2O |
您最近一年使用:0次
2022-07-26更新
|
1379次组卷
|
8卷引用:江西省宜春市丰城市第九中学2022-2023学年高二下学期开学质量检测化学试题
名校
解题方法
2 . 下列反应的离子方程式正确的是
| A.往澄清的石灰水中通入过量CO2:Ca2++2OH-+CO2=CaCO3↓+H2O |
B.氢氧化钡溶液与稀H2SO4反应:Ba2++SO +H++OH-=BaSO4↓+H2O +H++OH-=BaSO4↓+H2O |
| C.将氯气溶于水制备次氯酸:Cl2+ H2O=2H++ Cl-+ ClO- |
D.用酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO + 6H++ 5H2O2=2Mn2++ 5O2↑ + 8H2O + 6H++ 5H2O2=2Mn2++ 5O2↑ + 8H2O |
您最近一年使用:0次
2021-03-04更新
|
77次组卷
|
2卷引用:江西省抚州市金溪县第一中学2020-2021学年高二上学期入学考试化学试题
名校
解题方法
3 . 下列事实对应的离子方程式或电极反应式书写正确的是
A.用石墨作电极电解CuSO4溶液2Cu2++2H2O 2Cu+O2↑+4H+ 2Cu+O2↑+4H+ |
B.碳酸钠溶液显碱性:CO +2H2O +2H2O H2CO3+2OH- H2CO3+2OH- |
| C.钢铁发生吸氧腐蚀时,铁作负极被氧化:Fe-3e-=Fe3+ |
D.在强碱溶液中Fe(OH)3与NaClO反应生成Na2FeO4:3ClO-+2 Fe(OH)3=2FeO +3Cl-+H2O+4H+ +3Cl-+H2O+4H+ |
您最近一年使用:0次
2021-03-04更新
|
74次组卷
|
5卷引用:江西省南昌市第二中学2017-2018学年高二上学期期末考试化学试题
名校
解题方法
4 . 下列反应的离子方程式不正确的是
A.铁与稀盐酸反应: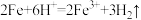 |
B.氢氧化钠溶液与盐酸反应: |
C.锌与硫酸铜溶液反应: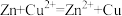 |
D.氯化钡溶液与稀硫酸反应: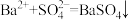 |
您最近一年使用:0次
2020-12-20更新
|
1440次组卷
|
73卷引用:【全国县级联考】江西省上饶县高中2017-2018学年高一下学期期末考试化学试题
【全国县级联考】江西省上饶县高中2017-2018学年高一下学期期末考试化学试题江西省井冈山市宁冈中学2021-2022学年高三下学期开学考试化学试题(已下线)2011-2012学年广东省梅州市曾宪梓中学高一中段考试化学试卷(已下线)2011-2012学年广东省佛山一中高二下学期期中考试文科化学试卷(已下线)2011-2012学年广东省揭阳一中高一下学期期中考试(文)化学试卷 (已下线)2011-2012学年广东汕头市达濠中学高二下学期期中考试文科化学试卷(已下线)2012-2013学年广东省深圳科学高中高一第一学期期末考试化学试卷B(已下线)2014-2015学年广东省肇庆第四中学高二上学期第一次月考文科化学卷2014-2015广东省汕头市金山中学高二上学期月考化学(文)试卷2014-2015广东省揭阳市第一中学高二上学期期末考试化学文试卷2015届广东省普通高中高三6月学业水平考试化学试卷2015-2016学年甘肃省会宁一中高二上期中(文)化学试卷2015-2016学年广东省实验中学高二上学期期末文化学试卷2015-2016学年广东省仲元中学高一下期末文科化学试卷广东省仲元中学2016-2017学年高二下学期期中考试(文)化学试题广东省普通高中2016-2017学年高二6月学业水平考试化学试题广东省普通高中2016-2017学年高二1月学业水平考试化学试题云南省玉溪市第一中学2016-2017学年高一下学期期末考试化学试题广东省韶关市新丰一中2016-2017学年高一下学期期末学业水平考试化学试题河北省唐山市滦县二中2017-2018学年高二期中考试化学(文)试卷广东省肇庆市实验中学2017-2018学年高二上学期期中考试(文)化学试题云南省峨山彝族自治县第一中学2017-2018学年高二12月月考(文)化学试题广东省深圳市高级中学2016-2017学年高一下学期期中考试+化学(学业水平)广东省深圳市高级中学2016-2017学年高二下学期期中考试(学业水平)化学试题广东省汕头市金山中学2017-2018学年高二上学期期末考试(学业水平测试)化学试题广东省佛山一中2017-2018学年高二上学期期末考试 化学(文)试题广东省汕头市达濠华侨中学2017-2018学年高二下学期阶段联考(一)化学试题广东省汕头市金山中学2017-2018学年高二下学期期中考试化学试题【全国百强校】广东省佛山市第一中学2017-2018学年高二下学期期中考试(文)化学试题2018年6月广东省普通高中学业水平考试化学试卷(A卷)【全国百强校】广东仲元中学2017-2018学年高二下学期期中考试化学(文)试题【全国百强校】贵州省遵义航天高级中学2018-2019学年高二(文)上学期第一次月考化学试题【全国百强校】黑龙江省牡丹江市第一高级中学2018-2019学年高二(文)上学期10月月考化学试题广东省湛江市第一中学2017-2018学年高一下学期第一次大考化学试题【全国百强校】广西壮族自治区桂林市第十八中学2018-2019学年高二上学期期中考试化学试题内蒙古自治区正镶白旗察汗淖中学2018-2019学年高一上学期期中考试化学试题广东省揭阳市惠来县第一中学2018-2019学年高一上学期期中考试化学试题【校级联考】广东省汕头市达濠华侨中学、东厦中学2018-2019学年高二(文)上学期阶段测试(二)化学试题广东省江门市第二中学2018-2019学年高二5月月考(文)化学试题2019年6月广东省普通高中学业水平考试化学试题2019年6月广东普通高中学业水平考试B卷化学试题广东省广州市番禺区2017-2018学年高二上学期期中考试化学(文)试题甘肃省天水市天水一中2019-2020学年高二(普通班)上学期第一次月考化学(文)试题2019-2020学年新新教材同步人教版高中化学必修第一册 (模块)质量检测贵州省凯里市第一中学2019-2020学年高二上学期期中考试化学(文)试题广东省韶关市新丰县第一中学2019-2020学年高二上学期期中考试化学(合格考)试题甘肃省张掖市第二中学2019-2020学年高二上学期期中考试化学(文)试题广西壮族自治区钦州市第三中学2017-2018学年高二上学期期中考试理综(文科)化学试题广东省揭阳普宁市2019-2020学年高一上学期期末考试化学试题夯基提能2020届高三化学选择题对题专练——离子反应方程式书写广东省湛江市第二十一中学2019-2020学年高一下学期复学考试(线上测试)化学试题广东省湛江市第二十一中学2019-2020学年高二上学期期中考试(学考)化学试题广东省江门市第二中学2019-2020学年高二上学期第二次考试(期中)化学(合格考)试题人教版(2019)高一必修第一册 第一章 物质及其变化 第二节 离子反应广东省肇庆市实验中学2020-2021学年高一上学期期中考试化学试题湖北省沙市中学2020-2021学年高一上学期期中考试化学(学考)试题江苏省南通西藏民族中学2020-2021学年高一上学期期中考试化学试题湖南平江县第一中学2021届高三上学期第二次月考化学试题2018年广东省普通高中学业水平合格性考试化学试卷湖南省武冈二中2019-2020学年高二下学期期末考试化学(学考)试题2016-2017学年广东省仲元中学高二上学期期末考试(文)化学试卷广东省江门市新会陈经纶中学2020-2021学年高二上学期期中考试化学(合格考)试题2021年1月广东省普通高中学业水平合格性考试化学试题贵州省凯里市第一中学2021-2022学年高二上学期期中考试化学(文科)试题云南省玉溪市第二中学2021-2022学年高二上学期期中考试化学试题云南省玉溪市江川区第二中学2021-2022学年高二上学期期中考试化学试题天津市滨海新区田家炳中学2022-2023学年高一上学期期中考试化学试题2023年广东省普通高中学业水平合格性考试化学科模拟测试卷(二)2023年广东省普通高中学业水平合格性考试化学科模拟仿真卷(一)广东省兴宁市东红中学2020-2021学年高一下学期期中考试化学试题湖南省2023年普通高中学业水平考试合格性考试(专家B卷)化学试题2023年黑龙江省高一下学期普通高中学业水平合格性考试化学模拟试题黑龙江省佳木斯市三校联考2023-2024学年高一下学期4月期中考试化学试题
名校
解题方法
5 . 已知①相同温度下:Ksp[Zn(OH)2]>Ksp(ZnS),Ksp(MgCO3)>Ksp[Mg(OH)2];②电离出S2-的能力:FeS>H2S>CuS,则下列离子方程式错误的是
| A.将FeS加入稀盐酸中:FeS+2H+=Fe2++H2S↑ |
| B.向CuSO4溶液中通H2S气体:Cu2++H2S=CuS↓+2H+ |
| C.将ZnCl2溶液和Na2S溶液混合:Zn2++S2-+2H2O=Zn(OH)2↓+H2S↑ |
D.向少量Mg(HCO3)2溶液中加入足量NaOH溶液:Mg2++2 +4OH-=Mg(OH)2↓+2 +4OH-=Mg(OH)2↓+2 +2H2O +2H2O |
您最近一年使用:0次
2020-12-11更新
|
814次组卷
|
13卷引用:江西省宜春市丰城市第九中学2022-2023学年高二下学期开学质量检测化学试题
江西省宜春市丰城市第九中学2022-2023学年高二下学期开学质量检测化学试题黑吉两省十校2020-2021学年高二上学期期中联考(其他8校用)化学试题(已下线)3.4.1 难溶电解质的沉淀溶解平衡(练习)-2020-2021学年上学期高二化学同步精品课堂(新教材人教版选择性必修1)2020年全国卷Ⅱ化学真题变式题福建省莆田第二十四中学2021-2022学年高二下学期开学摸底考试化学(2卷)试题课时1 沉淀溶解平衡及其应用山东省潍坊第一中学2022-2023学年高二上学期期末考试化学试题山东省青岛第六十八中学2023-2024学年高二上学期期中考试化学试卷黑龙江省海伦市第一中学2022-2023学年高二上学期11月期中考试化学试题(已下线)专题08 沉淀溶解平衡-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(人教版2019)(已下线)选择题1-5山东省青岛第十七中学2023-2024学年高二下学期期初考试化学试卷 2024届安徽省六安第一中学高三下学期质量检测(三 )化学试题
名校
解题方法
6 . 下列离子方程式中正确的是
A.澄清石灰水与稀盐酸反应 |
B.氢氧化钡与硫酸反应  |
C.铜片插入硝酸银溶液中 |
D.氯化镁溶液与氢氧化钠溶液反应 |
您最近一年使用:0次
2020-11-28更新
|
325次组卷
|
24卷引用:江西省宜春九中(外国语学校)2019-2020学年高二上学期入学考试化学试题
江西省宜春九中(外国语学校)2019-2020学年高二上学期入学考试化学试题江西省宜春中学2020-2021学年高一上学期期中考试化学试题(已下线)2012-2013学年辽宁盘锦第二高中高一第二次阶段考试化学试卷2017届陕西省安康市石泉中学高三上学期第一次月考化学试卷2016-2017学年甘肃静宁一中高一上月考二化学试卷河南省周口中英文学校2017-2018学年高一上学期期中考试化学试题高中化学人教版 必修1 第二章 化学物质及其变化 2.离子反应 离子反应及其发生的条件甘肃省白银市靖远县第四中学2018-2019学年高一上学期期中考试化学试题广东省韶关市新丰县第一中学2018-2019学年高一上学期期中考试化学试题山东省聊城第二中学2019-2020学年高一上学期第二次考试(9月)化学试题甘肃省靖远县第四中学2019-2020学年高一10月月考化学试题吉林省吉林地区普通高中友好学校联合体第三十一届2019-2020学年高一上学期期中考试化学试题吉林省白城市第十四中学2019—2020学年高一上学期期中考试化学试题福建省建瓯市芝华中学2019-2020学年高一上学期期中考试化学试题河南省周口中英文学校2019-2020学年高一上学期期中考试化学试题吉林省公主岭市范家屯镇第一中学2019-2020学年高一上学期第二次月考化学试题甘肃省兰州大学附属中学(33中)2019-2020学年高一上学期期中考试化学试题甘肃省庄浪县第一中学2020-2021学年高一上学期第一学段考试化学试题 内蒙古北京八中乌兰察布分校2020-2021学年高一上学期期中(学科素养评估二)考试化学试题重庆市渝西中学2020-2021学年高一上学期第一次月考化学试题浙江省苍南县金乡卫城中学2020-2021学年高一上学期第二次月考化学试题重庆市巫山县官渡中学2020-2021学年高一下学期第二次月考化学试题陕西省西安高新第一中学2022-2023学年高一上学期第一次月考 化学试题河南省许昌市鄢陵县职业教育中心2021—2022学年高一上学期升学班第一次月考化学试题
名校
解题方法
7 . 下列离子方程式正确的是
A.稀硫酸与Ba (OH)2溶液混合:Ba2++2OH-+2H++ SO =BaSO4↓+2H2O =BaSO4↓+2H2O |
B.小苏打溶液与氢氧化钠溶液混合:HCO +OH-=CO2↑+H2O +OH-=CO2↑+H2O |
| C.氯气通入澄清石灰水制漂白粉:2Ca(OH)2+2Cl2=Ca2++2Cl-+2ClO-+2H2O |
| D.Cl2溶于水:Cl2+H2O=2H++Cl-+ClO- |
您最近一年使用:0次
2020-11-25更新
|
99次组卷
|
2卷引用:江西省宜春市宜丰中学2023-2024学年高一上学期开学考试化学试题
名校
解题方法
8 . 下列表示对应化学反应的离子方程式正确的是
A.NaOH溶液与足量NaHCO3溶液反应:OH- + HCO = CO = CO + H2O + H2O |
B.Fe2(SO4)3溶液中加入足量Ba(OH)2溶液:Fe3+ + SO + Ba2+ + 3OH-=Fe(OH)3↓ + BaSO4↓ + Ba2+ + 3OH-=Fe(OH)3↓ + BaSO4↓ |
| C.碳酸钡中加入稀硫酸:BaCO3 + 2H+= Ba2+ + H2O + CO2↑ |
| D.氯化铝溶液与过量氨水反应 Al3+ + 3OH-=Al(OH)3↓ |
您最近一年使用:0次
2020-09-11更新
|
643次组卷
|
3卷引用:江西省丰城市第九中学2022-2023学年高三上学期入学考化学试题
名校
解题方法
9 . 能正确表示下列反应的离子方程式是( )
A.用过量氨水吸收工业尾气中的SO2:2NH3·H2O+SO2=2 + + +H2O +H2O |
B.氯化钠与浓硫酸混合加热:H2SO4+2Cl- SO2↑+Cl2↑+H2O SO2↑+Cl2↑+H2O |
C.磁性氧化铁溶于稀硝酸:3Fe2++4H++ ═3Fe3++NO↑+2H2O ═3Fe3++NO↑+2H2O |
D.明矾溶液中滴入Ba(OH)2溶液使 恰好完全沉淀:2Ba2++3OH-+Al3++2 恰好完全沉淀:2Ba2++3OH-+Al3++2 ═2BaSO4↓+Al(OH)3↓ ═2BaSO4↓+Al(OH)3↓ |
您最近一年使用:0次
名校
解题方法
10 . 硫酸亚铁的用途广泛,可以制备下图所示物质,下列说法错误的是
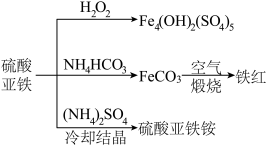

| A.Fe4(OH)2(SO4)5属于碱式盐,可用作净水剂 |
B.与足量NH4HCO3反应的离子方程式为:2 +Fe2+═FeCO3↓+CO2↑+H2O +Fe2+═FeCO3↓+CO2↑+H2O |
| C.可用稀硫酸和K3[Fe(CN)6]溶液检验铁红中是否含有FeCO3 |
| D.“冷却结晶”后的操作是过滤,“煅烧”操作的主要仪器有酒精灯、蒸发皿、玻璃棒 |
您最近一年使用:0次
2020-08-24更新
|
357次组卷
|
6卷引用:江西省丰城市第九中学2022-2023学年高三上学期入学考化学试题



