20. 实验室需要0.1mol·L
-1NaOH溶液450mL和0.5mol·L
-1硫酸溶液500mL。根据这两种溶液的配制情况回答下列问题:
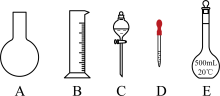
(1)如图所示的仪器中配制溶液肯定不需要的是
__________(填序号),配制上述溶液还需用到的玻璃仪器是
__________(填仪器名称)。
(2)配制0.1mol·L
-1NaOH溶液操作步骤如下:
①把称量好的NaOH`固体放入小烧杯中,加适量蒸馏水溶解;
②把①所得溶液冷却至室温,再小心转入一定容积的容量瓶中;
③继续向容量瓶中加蒸馏水至液面距刻度线1~2cm处,改用胶头滴管小心滴加蒸馏水至溶液凹液面与刻度线相切;
④用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心转入容量瓶,并轻轻摇匀;
⑤将容量瓶瓶塞塞紧,充分摇匀。
操作步骤的正确顺序为
__________(填序号)。
(3)根据计算用托盘天平称取NaOH的质量为
__________g。在实验中其他操作均正确,若容量瓶用蒸馏水洗涤后未干燥,则所得溶液浓度
______________0.10mol·L
-1(填“大于”“等于”或“小于”,下同)。若还未等溶液冷却就定容了,则所得溶液浓度
__________0.10mol·L
-1。
(4)根据计算得知,所需质量分数为98%、密度为1.84g·cm
-3的浓硫酸的体积为
__________mL(计算结果保留一位小数)。如果实验室有10mL、15mL、20mL、50mL的量筒,应选用
__________mL的量筒最好。