名校
解题方法
1 . 回答下列问题:
(1)某溶液中含有下列离子中的某些离子: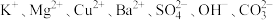 和
和 ,为确定其成分,取3份溶液分别进行如下实验:
,为确定其成分,取3份溶液分别进行如下实验:
Ⅰ.加入铝粉,有气泡产生
Ⅱ.滴入 溶液,无白色沉淀产生
溶液,无白色沉淀产生
Ⅲ.先滴加足量稀硝酸,再滴加 溶液,产生白色沉淀
溶液,产生白色沉淀
①根据以上现象判断,原溶液中肯定不存在的离子是_______ ,不能确定的离子是_______ ,若各离子浓度相等,可进一步得到的结论是_______ 。
②写出步骤Ⅲ中发生的离子反应方程式_______ 。
(2)某兴趣小组在两份相同的 溶液中,分别滴入相同浓度的
溶液中,分别滴入相同浓度的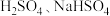 溶液,其导电能力随滴入溶液体积变化的曲线如下图所示:
溶液,其导电能力随滴入溶液体积变化的曲线如下图所示:

①图中表示 溶液中滴加
溶液中滴加 ,溶液的是曲线
,溶液的是曲线_______ (填“1”或“2”)。
② 在水溶液中的电离方程式为
在水溶液中的电离方程式为_______ 。
③下列说法错误的是_______ 。
A.曲线1中a点前导电能力不断减弱,说明生成的 不是电解质
不是电解质
B.曲线1中a点后导电能力不断增强,说明溶液中离子浓度在逐渐增大
C.曲线2中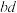 段发生的离子反应是
段发生的离子反应是
D.曲线2中d点对应的溶液显酸性
(1)某溶液中含有下列离子中的某些离子:
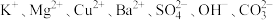 和
和 ,为确定其成分,取3份溶液分别进行如下实验:
,为确定其成分,取3份溶液分别进行如下实验:Ⅰ.加入铝粉,有气泡产生
Ⅱ.滴入
 溶液,无白色沉淀产生
溶液,无白色沉淀产生Ⅲ.先滴加足量稀硝酸,再滴加
 溶液,产生白色沉淀
溶液,产生白色沉淀①根据以上现象判断,原溶液中肯定不存在的离子是
②写出步骤Ⅲ中发生的离子反应方程式
(2)某兴趣小组在两份相同的
 溶液中,分别滴入相同浓度的
溶液中,分别滴入相同浓度的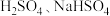 溶液,其导电能力随滴入溶液体积变化的曲线如下图所示:
溶液,其导电能力随滴入溶液体积变化的曲线如下图所示:
①图中表示
 溶液中滴加
溶液中滴加 ,溶液的是曲线
,溶液的是曲线②
 在水溶液中的电离方程式为
在水溶液中的电离方程式为③下列说法错误的是
A.曲线1中a点前导电能力不断减弱,说明生成的
 不是电解质
不是电解质B.曲线1中a点后导电能力不断增强,说明溶液中离子浓度在逐渐增大
C.曲线2中
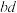 段发生的离子反应是
段发生的离子反应是
D.曲线2中d点对应的溶液显酸性
您最近一年使用:0次
2022-02-28更新
|
449次组卷
|
2卷引用:重庆第二外国语学校2021-2022学年高一上学期期末考试化学试题
2 . 根据酸碱的质子理论,“凡是能给出质子( )的分子或离子都是酸;凡是能结合质子的分子或离子都是碱。”按这个理论,下列微粒中:①
)的分子或离子都是酸;凡是能结合质子的分子或离子都是碱。”按这个理论,下列微粒中:① ,②
,② ,③
,③ ,④
,④ ,⑤
,⑤ ,⑥HClO,⑦
,⑥HClO,⑦ ,⑧
,⑧ 。
。
(1)只属于酸的微粒是:_______ ;属于两性的微粒是:_______ 。(填标号)。
(2)写出⑤和⑥反应的离子方程式_______ 。
(3)经检测某工业废水显酸性,且废水中含有大量 、
、 和上述③、⑦、⑧离子。
和上述③、⑦、⑧离子。
a.下列离子中不可能大量存在该废水的是_______ (填标号)。
A. B.
B. C.
C. D.
D.
b.将该废水调节至碱性;废水中存在的离子产生的现象是_______ 。
(4)用流程图表示除去粗盐水中 、
、 、
、 离子的方案设计。
离子的方案设计。
(可选用试剂有:稀盐酸、稀硫酸、 溶液、
溶液、 溶液、NaOH溶液。)
溶液、NaOH溶液。)
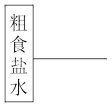
_______ 。
 )的分子或离子都是酸;凡是能结合质子的分子或离子都是碱。”按这个理论,下列微粒中:①
)的分子或离子都是酸;凡是能结合质子的分子或离子都是碱。”按这个理论,下列微粒中:① ,②
,② ,③
,③ ,④
,④ ,⑤
,⑤ ,⑥HClO,⑦
,⑥HClO,⑦ ,⑧
,⑧ 。
。(1)只属于酸的微粒是:
(2)写出⑤和⑥反应的离子方程式
(3)经检测某工业废水显酸性,且废水中含有大量
 、
、 和上述③、⑦、⑧离子。
和上述③、⑦、⑧离子。a.下列离子中不可能大量存在该废水的是
A.
 B.
B. C.
C. D.
D.
b.将该废水调节至碱性;废水中存在的离子产生的现象是
(4)用流程图表示除去粗盐水中
 、
、 、
、 离子的方案设计。
离子的方案设计。(可选用试剂有:稀盐酸、稀硫酸、
 溶液、
溶液、 溶液、NaOH溶液。)
溶液、NaOH溶液。)
您最近一年使用:0次
2023-02-17更新
|
282次组卷
|
2卷引用:山东省枣庄市2022-2023学年高一上学期期末考试化学试题
名校
3 . 按要求回答下列问题
(1)在无色透明的强酸性溶液中能大量共存的离子组是_______ 。
①.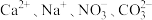
②.
③.
④.
⑤.Fe3+、K+、Cl-、S2-
⑥.Ag+、Na+、 、
、
⑦.Na+、Al3+、 、Cl-
、Cl-
⑧.Ba2+、 、C1-、CH3COO-
、C1-、CH3COO-
(2)①用单线桥表示反应电子转移的方向和数目: ,被氧化和被还原元素的物质的个数比
,被氧化和被还原元素的物质的个数比_______ 。
②用双线桥表示反应电子转移的方向和数目_______ 。
2Na2O2+2H2O=4NaOH+O2↑
反应每生成1个O2转移的电子数目为_______ 。
(3)有下列6种物质:K2SO4、K2SO3、I2、H2SO4、KIO3、H2O组成一个氧化还原反应,已知在反应中K2SO3失去电子。请回答下列问题:将这6种物质分别填入下面对应的横线上,组成一个配平 的化学方程式:_______ 。
_______+_______+H2SO4→_______+_______+_______(填化学式)
(1)在无色透明的强酸性溶液中能大量共存的离子组是
①.
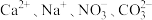
②.

③.

④.

⑤.Fe3+、K+、Cl-、S2-
⑥.Ag+、Na+、
 、
、
⑦.Na+、Al3+、
 、Cl-
、Cl-⑧.Ba2+、
 、C1-、CH3COO-
、C1-、CH3COO-(2)①用单线桥表示反应电子转移的方向和数目:
 ,被氧化和被还原元素的物质的个数比
,被氧化和被还原元素的物质的个数比②用双线桥表示反应电子转移的方向和数目
2Na2O2+2H2O=4NaOH+O2↑
反应每生成1个O2转移的电子数目为
(3)有下列6种物质:K2SO4、K2SO3、I2、H2SO4、KIO3、H2O组成一个氧化还原反应,已知在反应中K2SO3失去电子。请回答下列问题:将这6种物质分别填入下面对应的横线上,组成一个
_______+_______+H2SO4→_______+_______+_______(填化学式)
您最近一年使用:0次
解题方法
4 . 回答下列问题
(1)用自来水配制硝酸银溶液会产生浑浊现象,说明自来水中有__________ (微粒符号表示)。
(2)某反应后的溶液中有 。已知
。已知 在反应中得到电子,该反应的离子方程式
在反应中得到电子,该反应的离子方程式_____________ (不用配平)。
(3)某工业废水经检测显酸性,且废水中含有较多的 ,则于该废水中的不可能大量存在是(选
,则于该废水中的不可能大量存在是(选 )
)____________ ;若将该废水调节至碱性,原废水中__________ 的离子会减少。
(1)用自来水配制硝酸银溶液会产生浑浊现象,说明自来水中有
(2)某反应后的溶液中有
 。已知
。已知 在反应中得到电子,该反应的离子方程式
在反应中得到电子,该反应的离子方程式(3)某工业废水经检测显酸性,且废水中含有较多的
 ,则于该废水中的不可能大量存在是(选
,则于该废水中的不可能大量存在是(选 )
)
您最近一年使用:0次
解题方法
5 . 运用氮及其化合物的相关知识,完成下列各题。
(1)下列说法中,不正确 的是_______
(2)关于收集一氧化氮和二氧化氮两种气体的方法,下列叙述中正确的是_______
(3)下列气体中,既能用浓硫酸又能用碱石灰干燥的是_______
(4)将铁屑溶于过量盐酸后,再加入下列物质,会有 生成的是_______
生成的是_______
(5)下列各组离子在溶液中能大量共存的是_______
(1)下列说法中,
| A.豆科植物通过根瘤菌吸收空气中的氮气的过程是化学变化 |
| B.汽车尾气中排放的氮氧化物是由游离态氮转化来的 |
| C.化石燃料燃烧时通常不释放出氮氧化物 |
| D.植物秸秆燃烧时释放出氮氧化物,参与了氮的循环 |
| A.都可用排水法 |
| B.一氧化氮用排水法,二氧化氮用向上排空气法 |
| C.都可用向上排空气法 |
| D.一氧化氮用向上排空气法,二氧化氮用排水法 |
A. | B. | C.NO | D. |
 生成的是_______
生成的是_______| A.硫酸 | B.氯水 | C.硝酸锌 | D.氯化铜 |
A. 、 、 、 、 、 、 | B. 、 、 、 、 、 、 |
C. 、 、 、 、 、 、 | D. 、 、 、 、 、 、 |
您最近一年使用:0次
6 . 金属材料对于促进生产发展、改善人类生活发挥了巨大作用。请回答下列关于金属及其化合物的问题:
(1)若加入铝粉能放出氢气的溶液中分别加入下列各组离子,可能共存的是_______。
(2)实验室里保存 溶液时,常在溶液中加入
溶液时,常在溶液中加入_______ ,其目的为_______ 。
(3)实验室配制 溶液时,为了防止
溶液时,为了防止 水解,需要将
水解,需要将 溶于稀硫酸中,再加水稀释。现需配制
溶于稀硫酸中,再加水稀释。现需配制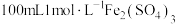 溶液,需要用托盘天平称量
溶液,需要用托盘天平称量_______ g 晶体,配制该溶液所需玻璃仪器除了烧杯、玻璃棒、量筒外,还需要
晶体,配制该溶液所需玻璃仪器除了烧杯、玻璃棒、量筒外,还需要_______ ;如果配制时俯视定容,那么所配溶液的浓度_______ (填“偏大”、“小”或“无影响”)。
(4)除杂:(括号内为杂质)
①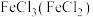 除杂试剂为
除杂试剂为_______ (填化学式),离子方程式为_______ ;
②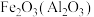 除杂试剂为
除杂试剂为_______ (填化学式),离子方程式为_______ 。
(1)若加入铝粉能放出氢气的溶液中分别加入下列各组离子,可能共存的是_______。
A.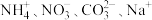 | B.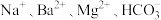 |
C.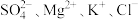 | D.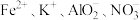 |
 溶液时,常在溶液中加入
溶液时,常在溶液中加入(3)实验室配制
 溶液时,为了防止
溶液时,为了防止 水解,需要将
水解,需要将 溶于稀硫酸中,再加水稀释。现需配制
溶于稀硫酸中,再加水稀释。现需配制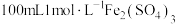 溶液,需要用托盘天平称量
溶液,需要用托盘天平称量 晶体,配制该溶液所需玻璃仪器除了烧杯、玻璃棒、量筒外,还需要
晶体,配制该溶液所需玻璃仪器除了烧杯、玻璃棒、量筒外,还需要(4)除杂:(括号内为杂质)
①
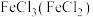 除杂试剂为
除杂试剂为②
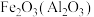 除杂试剂为
除杂试剂为
您最近一年使用:0次
7 . 回答下列问题:
(1)已知反应: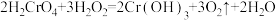 ,该反应中
,该反应中 只发生如下变化过程:
只发生如下变化过程:
① 中Cr元素的化合价是
中Cr元素的化合价是___________ ,该反应中的还原剂是___________ (填化学式)。
②该反应中,生成1mol 转移电子的数目是
转移电子的数目是___________ 。
(2)某无色溶液中可能含有 、
、 、
、 、
、 、
、 、
、 中的一种或几种离子。为确定其成分,进行以下实验:
中的一种或几种离子。为确定其成分,进行以下实验:
甲:向此溶液中滴加足量稀盐酸无明显现象。
乙:向甲的溶液并加入足量的 溶液,有23.3g白色沉淀产生。
溶液,有23.3g白色沉淀产生。
丙:向乙的溶液中加入足量的NaOH溶液,有5.8g白色沉淀产生。
根据实验结果判断:
①原溶液中不能确定是否含有的离子是___________ 。
②实验乙中反应的离子方程式为___________ 。
③由题中数据计算 的物质的量,下列选项一定正确的是
的物质的量,下列选项一定正确的是___________ 。
A. 等于0.4mol B.
等于0.4mol B. 大于或等于0.4mol C.
大于或等于0.4mol C. 等0.2mol
等0.2mol
(1)已知反应:
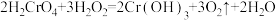 ,该反应中
,该反应中 只发生如下变化过程:
只发生如下变化过程:
①
 中Cr元素的化合价是
中Cr元素的化合价是②该反应中,生成1mol
 转移电子的数目是
转移电子的数目是(2)某无色溶液中可能含有
 、
、 、
、 、
、 、
、 、
、 中的一种或几种离子。为确定其成分,进行以下实验:
中的一种或几种离子。为确定其成分,进行以下实验:甲:向此溶液中滴加足量稀盐酸无明显现象。
乙:向甲的溶液并加入足量的
 溶液,有23.3g白色沉淀产生。
溶液,有23.3g白色沉淀产生。丙:向乙的溶液中加入足量的NaOH溶液,有5.8g白色沉淀产生。
根据实验结果判断:
①原溶液中不能确定是否含有的离子是
②实验乙中反应的离子方程式为
③由题中数据计算
 的物质的量,下列选项一定正确的是
的物质的量,下列选项一定正确的是A.
 等于0.4mol B.
等于0.4mol B. 大于或等于0.4mol C.
大于或等于0.4mol C. 等0.2mol
等0.2mol
您最近一年使用:0次
2023-08-21更新
|
134次组卷
|
2卷引用:广西河池市罗城仫佬族自治县高级中学等2校2022-2023学年高一上学期12月月考化学试题
解题方法
8 . 在酸性条件下,NO 与I-、Fe2+、SO
与I-、Fe2+、SO 等离子均不能大量共存。(_____)
等离子均不能大量共存。(_____)
 与I-、Fe2+、SO
与I-、Fe2+、SO 等离子均不能大量共存。(_____)
等离子均不能大量共存。(_____)
您最近一年使用:0次
2023高三上·全国·专题练习
解题方法
9 . NO (H+)不能和
(H+)不能和_______ 大量共存。
 (H+)不能和
(H+)不能和
您最近一年使用:0次
名校
10 . Ⅰ.完成下列问题
(1)医院里医生给“病人”做心电图时,在仪器与皮肤接触部位擦的一种电解质溶液是_______
(2)把0.05molBa(OH)2固体加入100mL下列液体中,溶液的导电能力明显减弱的是_______
(3)有关溶液中所含离子的检验,下列判断正确的是_______
(4)下列关于强电解质与弱电解质的说法正确的是_______
(5)能用离子方程式2H++CO =CO2↑+H2O表示的是
=CO2↑+H2O表示的是
(6)下列离子方程式中正确的是_______
(7)在酸性溶液中能大量共存且溶液为无色透明的离子组是_______
Ⅱ.有9种物质:①液态氯化氢②乙醇③熔融的KNO3④Cu⑤Na2O固体⑥氨水⑦NaHCO3溶液⑧无水醋酸⑨NaOH溶液。
(8)属于电解质的是___________ ;属于非电解质的有___________ 。
(9)写出⑧在水溶液中的电离方程式___________ 。
(10)写出⑨在水溶液中的电离方程式___________ 。
(11)已知亚磷酸H3PO3是二元弱酸,其与足量⑨反应后的产物为水和___________ 。
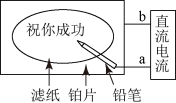
(12)以氯化钠为原料设计了“黑笔写红字”的趣味实验。滤纸先用氯化钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上,b端与铂片连接,a端与铅笔笔芯连接。接通电源后,用铅笔在滤纸上写字,会出现红色字迹。下列叙述正确的是________
(1)医院里医生给“病人”做心电图时,在仪器与皮肤接触部位擦的一种电解质溶液是_______
| A.氯化钠 | B.医用酒精 | C.葡萄糖 | D.碘酒 |
(2)把0.05molBa(OH)2固体加入100mL下列液体中,溶液的导电能力明显减弱的是_______
| A.水 | B.1mol·L-1MgCl2溶液 |
| C.1mol·L-1醋酸溶液 | D.0.5mol·L-1 H2SO4溶液 |
(3)有关溶液中所含离子的检验,下列判断正确的是_______
A.滴加BaCl2溶液,有白色沉淀生成,则原溶液中一定含有SO |
B.滴加盐酸,生成能使澄清石灰水变浑浊的气体,则原溶液中一定含有CO |
| C.滴加碳酸钠溶液产生白色沉淀,再加盐酸沉淀消失,则原溶液中一定含有Ba2+ |
| D.用某溶液做焰色反应时火焰为黄色,则该溶液中一定有钠元素,可能还有钾元素 |
(4)下列关于强电解质与弱电解质的说法正确的是_______
| A.强电解质溶液中不存在溶质分子,弱电解质溶液中只存在溶质分子 |
| B.强电解质在水中的溶解度大于弱电解质在水中的溶解度 |
| C.强电解质溶液的导电能力比弱电解质溶液强 |
| D.强电解质在水中全部电离,弱电解质在水中部分电离 |
(5)能用离子方程式2H++CO
 =CO2↑+H2O表示的是
=CO2↑+H2O表示的是| A.H2SO4和Na2CO3 | B.HCl和BaCO3 |
| C.CH3COOH和Na2CO3 | D.HI和NaHCO3 |
(6)下列离子方程式中正确的是_______
| A.Fe与稀硫酸的反应:2Fe+6H+=Fe3++3H2↑ |
B.硫酸钠与氯化钡浴液混合:SO +Ba2+=BaSO4↓ +Ba2+=BaSO4↓ |
| C.硝酸滴在石灰石上:CaCO3+2H+=Ca2++H2CO3 |
D.氧化铜与硫酸混合:Cu2++SO =CuSO4 =CuSO4 |
(7)在酸性溶液中能大量共存且溶液为无色透明的离子组是_______
A.K+、MnO 、Na+、Cl- 、Na+、Cl- | B.K+、Na+、NO 、SO 、SO |
C.Ba2+、Na+、NO 、SO 、SO | D.Mg2+、Na+、Cl-、SO |
Ⅱ.有9种物质:①液态氯化氢②乙醇③熔融的KNO3④Cu⑤Na2O固体⑥氨水⑦NaHCO3溶液⑧无水醋酸⑨NaOH溶液。
(8)属于电解质的是
(9)写出⑧在水溶液中的电离方程式
(10)写出⑨在水溶液中的电离方程式
(11)已知亚磷酸H3PO3是二元弱酸,其与足量⑨反应后的产物为水和
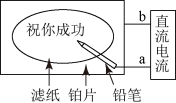
(12)以氯化钠为原料设计了“黑笔写红字”的趣味实验。滤纸先用氯化钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上,b端与铂片连接,a端与铅笔笔芯连接。接通电源后,用铅笔在滤纸上写字,会出现红色字迹。下列叙述正确的是________
| A.b极发生还原反应 |
| B.铂片端作阴极 |
| C.铅笔端有少量的氯气产生 |
| D.a处是负极 |
您最近一年使用:0次



