解题方法
1 . 向100mL 和
和 的混合溶液中逐渐加入铁粉,充分反应后溶液中固体剩余物的质量与加入铁粉的质量关系如图所示。忽略反应过程中溶液体积的变化,下列说法正确的是
的混合溶液中逐渐加入铁粉,充分反应后溶液中固体剩余物的质量与加入铁粉的质量关系如图所示。忽略反应过程中溶液体积的变化,下列说法正确的是

 和
和 的混合溶液中逐渐加入铁粉,充分反应后溶液中固体剩余物的质量与加入铁粉的质量关系如图所示。忽略反应过程中溶液体积的变化,下列说法正确的是
的混合溶液中逐渐加入铁粉,充分反应后溶液中固体剩余物的质量与加入铁粉的质量关系如图所示。忽略反应过程中溶液体积的变化,下列说法正确的是
A.a点时溶液中发生的反应为 |
B.b点时溶液中的阳离子有 、 、 和 和 |
C.c点时溶液中 的物质的量浓度为 的物质的量浓度为 |
| D.由c点到d点的过程中,溶液的质量一直减小 |
您最近一年使用:0次
名校
解题方法
2 . 下列不能 达到“实验目的”的“实验操作及现象”是
| 选项 | 实验目的 | 实验操作及现象 |
| A | 证明浓硫酸有吸水性 | 向蔗糖中滴加浓硫酸,蔗糖变黑 |
| B | 证明SO2具有漂白性 | 向品红溶液中通入SO2,溶液褪色 |
| C | 证明氧化性:Br2>I2 | 向KI和淀粉的混合溶液中滴加溴水,溶液变蓝 |
| D | 检验NH4Cl溶液中的NH | 向NH4Cl溶液中加入浓NaOH溶液,加热,产生的气体能使湿润的红色石蕊试纸变蓝 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-01-17更新
|
305次组卷
|
2卷引用:北京市2022-2023学年高二上学期第二次合格考化学试题
名校
解题方法
3 . 反应 可用于制备金属钼(Mo)。下列关于该反应的说法不正确的是
可用于制备金属钼(Mo)。下列关于该反应的说法不正确的是
 可用于制备金属钼(Mo)。下列关于该反应的说法不正确的是
可用于制备金属钼(Mo)。下列关于该反应的说法不正确的是| A.Al的还原性比Mo强 | B.Mo为还原产物 |
| C.Al得到电子 | D. 发生还原反应 发生还原反应 |
您最近一年使用:0次
2022-12-27更新
|
479次组卷
|
5卷引用:江苏省2022-2023学年高二上学期学业水平合格性模拟预测(一)化学试题
江苏省2022-2023学年高二上学期学业水平合格性模拟预测(一)化学试题江苏省涟水县第一中学2022-2023学年高二上学期学业水平合格性考试化学试题(已下线)专题七 氧化还原反应(已下线)合格考汇编3氧化还原反应广东省湛江市第二十一中学2023-2024学年高一下学期第一次月考化学(学考)试题
解题方法
4 . 下列关于钠的叙述中,不正确 的是
| A.钠具有很强的还原性 | B.钠燃烧时发出黄色的火焰 |
| C.钠原子的最外层只有1个电子 | D.钠离子具有很强的氧化性 |
您最近一年使用:0次
解题方法
5 . 某化学课外小组用海带为原料制取少量单质,实验流程如下:

请回答下列问题:
(1)①实验步骤Ⅰ会用到下列仪器中的_______ (填字母);
a.酒精灯 b.漏斗 c.坩埚 d.泥三角
②步骤Ⅲ所采用的分离方法是_______ (填“过滤”或“蒸馏”);
③步骤Ⅳ说明氧化性:Cl2_______ (填“>”或“<”)I2。
(2)一定条件下,工业上可利用H2和I2反应生成HI,反应的化学方程式为H2(g)+I2(g) 2HI(g)。将1mol I2(g)和1mol H2置于1L的密闭容器中,10min后测得I2(g)为0.3 mol。则:
2HI(g)。将1mol I2(g)和1mol H2置于1L的密闭容器中,10min后测得I2(g)为0.3 mol。则:
①用I2(g)表示该反应的速率为_______ mol·L-1·min-1;
②其他条件不变时,再通入1mol H2,该反应的速率将_______ (填“增大”“不变”或“减小”)。

请回答下列问题:
(1)①实验步骤Ⅰ会用到下列仪器中的
a.酒精灯 b.漏斗 c.坩埚 d.泥三角
②步骤Ⅲ所采用的分离方法是
③步骤Ⅳ说明氧化性:Cl2
(2)一定条件下,工业上可利用H2和I2反应生成HI,反应的化学方程式为H2(g)+I2(g)
 2HI(g)。将1mol I2(g)和1mol H2置于1L的密闭容器中,10min后测得I2(g)为0.3 mol。则:
2HI(g)。将1mol I2(g)和1mol H2置于1L的密闭容器中,10min后测得I2(g)为0.3 mol。则:①用I2(g)表示该反应的速率为
②其他条件不变时,再通入1mol H2,该反应的速率将
您最近一年使用:0次
6 . 在45~ 50°C时,臭氧(O3)可以将碘氧化为碘酸碘[I(IO3)3]。反应的化学方程式如下:9O3+2I2=I(IO3)3+ 9O2。下列说法正确的是
| A.O3既不是氧化剂也不是还原剂 |
| B.I(IO3)3中碘元素的化合价均为+5 |
| C.氧化性:I(IO3)3>I2 |
| D.氧化性:I2> I(IO3)3 |
您最近一年使用:0次
7 . 某实验小组欲通过加热蒸发KNO3溶液的方法获得KNO3固体。已知KNO3固体在一定温度下能够发生反应:2KNO3 2KNO2 + O2↑。为了探究加热蒸发所得固体X中是否含有KNO2,小组同学分别设计并完成了以下实验。
2KNO2 + O2↑。为了探究加热蒸发所得固体X中是否含有KNO2,小组同学分别设计并完成了以下实验。
【查阅资料】
ⅰ.AgNO2是微溶于水的白色(略带黄色)固体
ⅱ.KNO2能在酸性条件下与KI反应,生成I2
【实验过程】
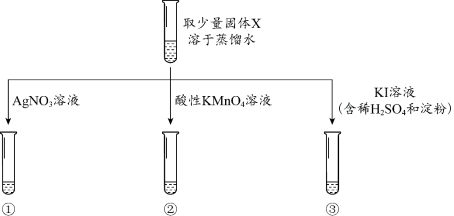
【分析解释】
(1)实验①中,观察到有少量白色沉淀生成,该白色沉淀是_______ 。
(2)实验②中,观察到酸性KMnO4溶液紫红色褪去,利用对比实验排除了稀释对溶液颜色变化的影响。补全该反应的离子方程式:2MnO + 5NO
+ 5NO + 6H+ = 2Mn2+ +
+ 6H+ = 2Mn2+ +_______ + 3H2O
(3)实验③中,观察到溶液变为蓝色。实验③中选择KI溶液的依据是_______ (填字母)。
a.KNO2具有氧化性,KI具有还原性
b.KNO2具有还原性,KI具有氧化性
【反思评价】
(4)综合上述实验,甲同学认为,实验①、②、③均可以证明固体X中含有KNO2;乙同学认为,通过实验③不能证明固体X中含有KNO2。乙同学的理由是_______ 。
 2KNO2 + O2↑。为了探究加热蒸发所得固体X中是否含有KNO2,小组同学分别设计并完成了以下实验。
2KNO2 + O2↑。为了探究加热蒸发所得固体X中是否含有KNO2,小组同学分别设计并完成了以下实验。【查阅资料】
ⅰ.AgNO2是微溶于水的白色(略带黄色)固体
ⅱ.KNO2能在酸性条件下与KI反应,生成I2
【实验过程】

【分析解释】
(1)实验①中,观察到有少量白色沉淀生成,该白色沉淀是
(2)实验②中,观察到酸性KMnO4溶液紫红色褪去,利用对比实验排除了稀释对溶液颜色变化的影响。补全该反应的离子方程式:2MnO
 + 5NO
+ 5NO + 6H+ = 2Mn2+ +
+ 6H+ = 2Mn2+ +(3)实验③中,观察到溶液变为蓝色。实验③中选择KI溶液的依据是
a.KNO2具有氧化性,KI具有还原性
b.KNO2具有还原性,KI具有氧化性
【反思评价】
(4)综合上述实验,甲同学认为,实验①、②、③均可以证明固体X中含有KNO2;乙同学认为,通过实验③不能证明固体X中含有KNO2。乙同学的理由是
您最近一年使用:0次
2022-04-15更新
|
283次组卷
|
2卷引用:北京市2021-2022学年高三年级下学期合格考(第一次)化学试题
解题方法
8 . 下列有关实验操作、现象及结论都正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 两支试管各盛4 mL 0.1 mol/L酸性高锰酸钾溶液,分别加入2 mL 0.1 mol/L的 草酸溶液和2 mL 0.2 mol/L草酸溶液 | 加入0.2 mol/L草酸溶液的试管中,高锰酸钾溶液完全褪色时间更短 | 反应物浓度越大,反应速率越快 |
| B | 室温下,向 溶液中滴加少量KI溶液,再滴加几滴淀粉溶液 溶液中滴加少量KI溶液,再滴加几滴淀粉溶液 | 溶液变蓝色 |  的氧化性比 的氧化性比 的强 的强 |
| C | 将淀粉和稀硫酸混合加热一段时间后,再加入新制的 悬浊液,加热 悬浊液,加热 | 产生砖红色沉淀 | 淀粉在稀硫酸、加热条件下水 解为葡萄糖 |
| D | 取一支试管装入2 mL 2 mol/L NaOH溶液,先滴加1 mL 1 mol/L  溶液,再滴加几滴1 mol/L 溶液,再滴加几滴1 mol/L 溶液 溶液 | 先生成白色沉淀,后沉淀变为蓝色 | 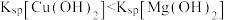 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-01-11更新
|
348次组卷
|
2卷引用:河南省濮阳市2021-2022学年高二下学期学业质量监测考试化学试题
13-14高一下·北京西城·期末
名校
9 . 为探究H2O2、SO2、Br2氧化性强弱,某小组同学设计如下实验(夹持及尾气处理装置已略去,气密性已检验)。
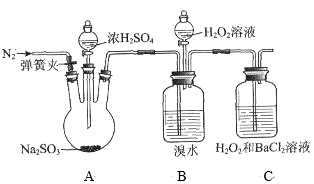
(1)A中发生反应的化学方程式是____ 。
(2)甲同学通过C中产生白色沉淀,得出结论,氧化性:H2O2>SO2。
①乙同学认为不能得出此结论,认为在滴加浓硫酸之前应增加一步操作,该操作是____ 。
②丙同学认为还应该在B和C之间增加洗气瓶D,D中盛放的试剂是___ 。
③将乙和丙同学改进后的方案进行实验,C中产生白色沉淀,得出结论:氧化性H2O2>SO2。
(3)ⅲ中滴入少量H2O2没有明显变化。提出假设:
观点1:H2O2的量少不能氧化Br―
观点2:B中有未反应的H2SO3
为验证观点2,应进行的实验操作及现象是________ 。
(4)通过上述全部实验,得出结论:H2O2、SO2、Br2氧化性由强到弱的顺序是____ 。

| 实验操作 | 实验现象 |
| ⅰ.打开A中分液漏斗活塞,滴加浓硫酸 | A中有气泡产生,B中红棕色溴水褪色,C中有白色沉淀 |
| ⅱ.取C中沉淀加入盐酸 | C中白色沉淀不溶解 |
| ⅲ.打开B中分液漏斗活塞,逐滴滴加H2O2 | 开始时颜色无明显变化;继续滴加H2O2溶液,一段时间后,混合液逐渐变成红棕色 |
(2)甲同学通过C中产生白色沉淀,得出结论,氧化性:H2O2>SO2。
①乙同学认为不能得出此结论,认为在滴加浓硫酸之前应增加一步操作,该操作是
②丙同学认为还应该在B和C之间增加洗气瓶D,D中盛放的试剂是
③将乙和丙同学改进后的方案进行实验,C中产生白色沉淀,得出结论:氧化性H2O2>SO2。
(3)ⅲ中滴入少量H2O2没有明显变化。提出假设:
观点1:H2O2的量少不能氧化Br―
观点2:B中有未反应的H2SO3
为验证观点2,应进行的实验操作及现象是
(4)通过上述全部实验,得出结论:H2O2、SO2、Br2氧化性由强到弱的顺序是
您最近一年使用:0次
2016-12-09更新
|
1151次组卷
|
9卷引用:北京市朝阳区2021-2022学年高一年级下学期合格考模拟检测化学试题
北京市朝阳区2021-2022学年高一年级下学期合格考模拟检测化学试题北京市2019年普通高中学业水平合格性考试模拟化学试题江西省省重点校联盟2022-2023学年高二上学期入学联考化学试题(已下线)2013-2014北京市西城区下学期高一年级期末考试化学试卷(已下线)2015届河南省洛阳市高三上学期期中考试化学试卷2014-2015学年湖北省部分重点高中高二下期末考试化学试卷(已下线)北京市第四中学2016-2017学年高一下学期期中考试化学试题四川省眉山市彭山区第一中学2019-2020学年高二上学期开学考试化学试题(人教版2019)必修第二册 模块学业水平合格性测评



