1 . 将 和空气的混合气体通入
和空气的混合气体通入 、
、 和
和 的混合溶液中回收S,其转化如图所示(CuS不溶于水)。下列说法正确的是
的混合溶液中回收S,其转化如图所示(CuS不溶于水)。下列说法正确的是
 和空气的混合气体通入
和空气的混合气体通入 、
、 和
和 的混合溶液中回收S,其转化如图所示(CuS不溶于水)。下列说法正确的是
的混合溶液中回收S,其转化如图所示(CuS不溶于水)。下列说法正确的是
A.基态Cu原子的电子排布式为 |
B.过程①的离子方程式为: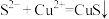 |
C.氧化性: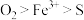 |
D.相同条件下, 和空气的比例不影响处理效果 和空气的比例不影响处理效果 |
您最近一年使用:0次
名校
解题方法
2 . 以下是一系列非金属元素间的置换反应,其中不能说明反应前的非金属单质的氧化性强于产物中非金属单质的氧化性的是
A. | B.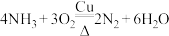 |
C. | D. |
您最近一年使用:0次
3 . 细菌可以促使铁、氮两种元素进行氧化还原反应,并耦合两种元素的循环。耦合循环中的部分转化如下图所示。_______ (填字母序号)。
a.N2转化为氨态氮 b.硝化过程 c.反硝化过程
(2)氮肥是水体中氨态氮的主要来源之一,氨气是生产氮肥的主要原料,工业合成氨的化学方程式为_______ 。
(3)硝化过程中,含氮物质发生_______ (填“氧化”或“还原”)反应。
(4)氨态氮与亚硝态氮可以在氨氧化细菌的作用下转化为氮气。该反应中,当产生0.02 mol 氮气时,转移的电子的物质的量为_______ mol。
(5)NO是大气污染气体,测定某气体样品中NO含量操作如下:将2L气样通入适量酸化的H2O2溶液中,使NO完全被氧化为 。向上述反应后溶液中加入30 mL0.1 mol·L−1FeSO4溶液(过量),充分反应后,多余Fe2+与3.5 mL、0.1 mol·L−1K2Cr2O7恰好反应。NO被H2O2氧化为
。向上述反应后溶液中加入30 mL0.1 mol·L−1FeSO4溶液(过量),充分反应后,多余Fe2+与3.5 mL、0.1 mol·L−1K2Cr2O7恰好反应。NO被H2O2氧化为 的离子方程式是
的离子方程式是______ 。上述过程中发生下列反应:3Fe2++ +4H+=NO↑+3Fe3++2H2O;
+4H+=NO↑+3Fe3++2H2O; + 6Fe2+ +14H+ =2Cr3+ +6Fe3++7H2O。则气样中NO的含量为
+ 6Fe2+ +14H+ =2Cr3+ +6Fe3++7H2O。则气样中NO的含量为_______ mg /L。(保留计算过程)
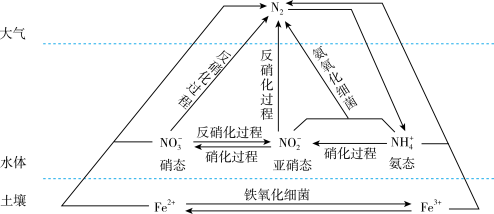
a.N2转化为氨态氮 b.硝化过程 c.反硝化过程
(2)氮肥是水体中氨态氮的主要来源之一,氨气是生产氮肥的主要原料,工业合成氨的化学方程式为
(3)硝化过程中,含氮物质发生
(4)氨态氮与亚硝态氮可以在氨氧化细菌的作用下转化为氮气。该反应中,当产生0.02 mol 氮气时,转移的电子的物质的量为
(5)NO是大气污染气体,测定某气体样品中NO含量操作如下:将2L气样通入适量酸化的H2O2溶液中,使NO完全被氧化为
 。向上述反应后溶液中加入30 mL0.1 mol·L−1FeSO4溶液(过量),充分反应后,多余Fe2+与3.5 mL、0.1 mol·L−1K2Cr2O7恰好反应。NO被H2O2氧化为
。向上述反应后溶液中加入30 mL0.1 mol·L−1FeSO4溶液(过量),充分反应后,多余Fe2+与3.5 mL、0.1 mol·L−1K2Cr2O7恰好反应。NO被H2O2氧化为 的离子方程式是
的离子方程式是 +4H+=NO↑+3Fe3++2H2O;
+4H+=NO↑+3Fe3++2H2O; + 6Fe2+ +14H+ =2Cr3+ +6Fe3++7H2O。则气样中NO的含量为
+ 6Fe2+ +14H+ =2Cr3+ +6Fe3++7H2O。则气样中NO的含量为
您最近一年使用:0次
4 . 研究和采取措施去除氮氧化物尾气和水中硝酸盐造成的氮污染备受关注。
Ⅰ氧化吸收法 酸性条件下,NaClO溶液氧化 、NO和
、NO和 等生成
等生成 和
和 。
。
(1)其他条件一定, 转化为
转化为 的转化率随水体溶液初始pH的变化如图1所示。
的转化率随水体溶液初始pH的变化如图1所示。 、NO和
、NO和 三种气体中,相同条件下最易被NaClO氧化的是
三种气体中,相同条件下最易被NaClO氧化的是________ 。
②在酸性水体中,加入NaClO溶液吸收 的离子方程式为
的离子方程式为________ 。
③水体溶液初始pH越小, 转化率越高。其原因是
转化率越高。其原因是________ 。
(2)NaClO吸收液还可以同时脱除烟气中NO和 。研究发现NaClO吸收液在不同初始pH条件下,对流动烟气的脱硫效率都接近100%,而对NO的脱除率如图2所示:
。研究发现NaClO吸收液在不同初始pH条件下,对流动烟气的脱硫效率都接近100%,而对NO的脱除率如图2所示:
①酸性条件下, 的脱除率高于NO,其原因除
的脱除率高于NO,其原因除 的还原性比NO强外,还可能是
的还原性比NO强外,还可能是________ 。
②若用盐酸调节NaClO吸收液pH,不仅不利于NO的吸收,还会在反应过程中生成一种有毒气体,其化学式为________ 。
Ⅱ催化还原法
(3)在 的催化条件下,使用
的催化条件下,使用 作为还原剂,可将水中的
作为还原剂,可将水中的 转化为
转化为 。该反应机理分为三步,如题17图3所示:第一步:
。该反应机理分为三步,如题17图3所示:第一步:________ (补充完整该步反应机理);第二步: 从Cu表面迁移至W的表面;第三步:
从Cu表面迁移至W的表面;第三步: 在W表面吸附并解离为活性氢原子(W-H),W-H将
在W表面吸附并解离为活性氢原子(W-H),W-H将 还原为
还原为 ,同时W-H将CuO还原为Cu,自身转化为W,实现Cu和W的催化循环。
,同时W-H将CuO还原为Cu,自身转化为W,实现Cu和W的催化循环。 作为还原硝酸盐过程的催化剂,其催化机理与
作为还原硝酸盐过程的催化剂,其催化机理与 相似。但还原过程中检测到三种含氮化合物微粒,其浓度变化如图4所示,在1.5小时以后,
相似。但还原过程中检测到三种含氮化合物微粒,其浓度变化如图4所示,在1.5小时以后, 的百分含量不断减少,
的百分含量不断减少, 的百分含量不断增多的可能原因是
的百分含量不断增多的可能原因是________ 。
Ⅰ氧化吸收法 酸性条件下,NaClO溶液氧化
 、NO和
、NO和 等生成
等生成 和
和 。
。(1)其他条件一定,
 转化为
转化为 的转化率随水体溶液初始pH的变化如图1所示。
的转化率随水体溶液初始pH的变化如图1所示。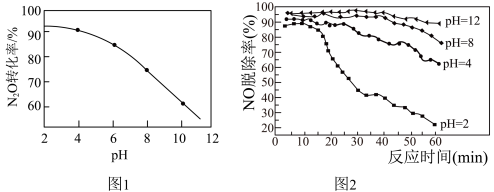
 、NO和
、NO和 三种气体中,相同条件下最易被NaClO氧化的是
三种气体中,相同条件下最易被NaClO氧化的是②在酸性水体中,加入NaClO溶液吸收
 的离子方程式为
的离子方程式为③水体溶液初始pH越小,
 转化率越高。其原因是
转化率越高。其原因是(2)NaClO吸收液还可以同时脱除烟气中NO和
 。研究发现NaClO吸收液在不同初始pH条件下,对流动烟气的脱硫效率都接近100%,而对NO的脱除率如图2所示:
。研究发现NaClO吸收液在不同初始pH条件下,对流动烟气的脱硫效率都接近100%,而对NO的脱除率如图2所示:①酸性条件下,
 的脱除率高于NO,其原因除
的脱除率高于NO,其原因除 的还原性比NO强外,还可能是
的还原性比NO强外,还可能是②若用盐酸调节NaClO吸收液pH,不仅不利于NO的吸收,还会在反应过程中生成一种有毒气体,其化学式为
Ⅱ催化还原法
(3)在
 的催化条件下,使用
的催化条件下,使用 作为还原剂,可将水中的
作为还原剂,可将水中的 转化为
转化为 。该反应机理分为三步,如题17图3所示:第一步:
。该反应机理分为三步,如题17图3所示:第一步: 从Cu表面迁移至W的表面;第三步:
从Cu表面迁移至W的表面;第三步: 在W表面吸附并解离为活性氢原子(W-H),W-H将
在W表面吸附并解离为活性氢原子(W-H),W-H将 还原为
还原为 ,同时W-H将CuO还原为Cu,自身转化为W,实现Cu和W的催化循环。
,同时W-H将CuO还原为Cu,自身转化为W,实现Cu和W的催化循环。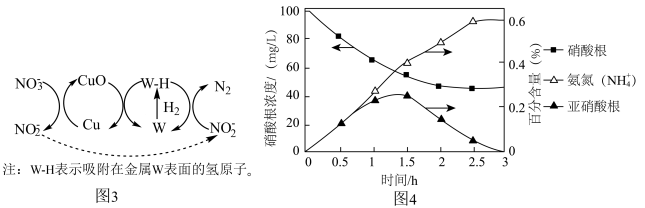
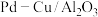 作为还原硝酸盐过程的催化剂,其催化机理与
作为还原硝酸盐过程的催化剂,其催化机理与 相似。但还原过程中检测到三种含氮化合物微粒,其浓度变化如图4所示,在1.5小时以后,
相似。但还原过程中检测到三种含氮化合物微粒,其浓度变化如图4所示,在1.5小时以后, 的百分含量不断减少,
的百分含量不断减少, 的百分含量不断增多的可能原因是
的百分含量不断增多的可能原因是
您最近一年使用:0次
解题方法
5 . 新型冠状病毒肺炎爆发以来,各类杀菌消毒剂逐渐被人们所认识和使用。下列是我们常见的几种消毒剂:①“84”消毒液;②H2O2(在水中一部分可以电离出阴、阳离子);③ClO2;④O3;⑤碘酒;⑥75%酒精;⑦高铁酸钠(Na2FeO4)。回答下列问题:
(1)上述杀菌消毒剂属于电解质的是___________ (填序号),“84”消毒液中有效成分的电离方程式为___________ ,双氧水的电子式为___________ 。
(2)各类杀菌消毒剂使用时,必须严格按照使用说明。
①巴西奥运会期间,由于工作人员将“84”消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是NaClO与H2O2反应产生O2促进藻类快速生长。该反应说明氧化性:NaClO___________ H2O2(填“>”或“<”),若1 mol NaClO参加反应,转移电子数___________ (阿伏加德罗常数为NA)。
②若混合使用“洁厕灵”(主要成分为盐酸)与“84”消毒液会产生氯气。原因是(用离子方程式表示)___________ 。
(3)ClO2在杀菌消毒过程中会产生亚氯酸盐(ClO ),需将其转化为Cl− 除去,下列试剂可将ClO
),需将其转化为Cl− 除去,下列试剂可将ClO 转化为Cl− 的是
转化为Cl− 的是___________ (填标号)。
a.FeSO4 b.O3 c.KMnO4 d.Na2CO3
(1)上述杀菌消毒剂属于电解质的是
(2)各类杀菌消毒剂使用时,必须严格按照使用说明。
①巴西奥运会期间,由于工作人员将“84”消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是NaClO与H2O2反应产生O2促进藻类快速生长。该反应说明氧化性:NaClO
②若混合使用“洁厕灵”(主要成分为盐酸)与“84”消毒液会产生氯气。原因是(用离子方程式表示)
(3)ClO2在杀菌消毒过程中会产生亚氯酸盐(ClO
 ),需将其转化为Cl− 除去,下列试剂可将ClO
),需将其转化为Cl− 除去,下列试剂可将ClO 转化为Cl− 的是
转化为Cl− 的是a.FeSO4 b.O3 c.KMnO4 d.Na2CO3
您最近一年使用:0次
名校
6 . 氨是一种重要的化工原料,广泛用于硝酸、纯碱、制药、化肥等工业。合成氨反应为 ,
, 在催化剂作用下发生一系列转化的示意图如下:
在催化剂作用下发生一系列转化的示意图如下:
 ,
, 在催化剂作用下发生一系列转化的示意图如下:
在催化剂作用下发生一系列转化的示意图如下: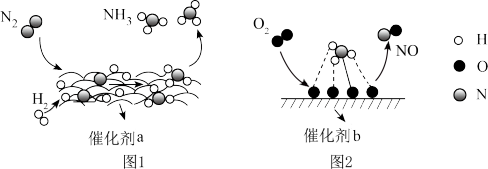
A.催化剂b表面发生的反应利用了 的氧化性 的氧化性 |
| B.催化剂a、b表面发生的反应过程中均发生了非极性共价键的断裂 |
C.合成氨反应的热效应为 (E表示键能) (E表示键能) |
D.22.4L 在催化剂a表面充分反应,转移电子数一定为 在催化剂a表面充分反应,转移电子数一定为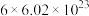 |
您最近一年使用:0次
7 . “价类”二维图体现了元素的分类观、转化观,下图是 元素及其化合物的“价类”二维图。下列说法正确的是
元素及其化合物的“价类”二维图。下列说法正确的是
 元素及其化合物的“价类”二维图。下列说法正确的是
元素及其化合物的“价类”二维图。下列说法正确的是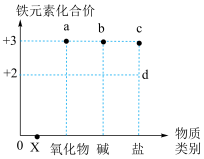
| A.a到b可以一步实现 | B.实验室保存d的溶液可以加入少量铜粉 |
| C.b为红褐色固体 | D.d转化为c需要加入还原剂 |
您最近一年使用:0次
名校
8 . 工厂烟气(主要污染物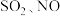 )直接排放会造成空气污染,需处理后才能排放。
)直接排放会造成空气污染,需处理后才能排放。
(1)“纳米零价铁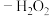 ”体系可将烟气中难溶的NO氧化为可溶的
”体系可将烟气中难溶的NO氧化为可溶的 。在一定温度下,将
。在一定温度下,将 溶液和HCl溶液雾化后与烟气按一定比例混合,以一定流速通过装有纳米零价铁的反应装置,可将烟气中的NO氧化。
溶液和HCl溶液雾化后与烟气按一定比例混合,以一定流速通过装有纳米零价铁的反应装置,可将烟气中的NO氧化。
① 催化
催化 分解产生HO·,HO·将NO氧化为
分解产生HO·,HO·将NO氧化为 的机理如下图所示,Y的化学式为
的机理如下图所示,Y的化学式为___________ 。 反应生成HNO3的化学方程式为
反应生成HNO3的化学方程式为___________ 。
③纳米零价铁的作用是___________ 。
④NO脱除率随温度的变化如下图所示。温度高于120℃时,NO脱除率随温度升高呈现下降趋势的主要原因是___________ 。 、
、 ,下列措施能提高尾气中NO和
,下列措施能提高尾气中NO和 去除率的有
去除率的有___________ (填字母)。
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量NaOH溶液
(3) 脱硝技术已成为使用广泛和成熟的烟气净化技术,脱硝效率高达
脱硝技术已成为使用广泛和成熟的烟气净化技术,脱硝效率高达 %以上。反应机理如下图所示,写出该反应发生的化学方程式
%以上。反应机理如下图所示,写出该反应发生的化学方程式___________ 。 溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO转化为
溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO转化为 的转化率随
的转化率随 溶液初始pH(用稀盐酸调节)的变化如图所示:
溶液初始pH(用稀盐酸调节)的变化如图所示: 溶液中,
溶液中, 氧化NO生成Cl-和
氧化NO生成Cl-和 ,其离子方程式为
,其离子方程式为___________ 。
②NaClO溶液的初始pH越小,NO转化率越高。其原因是___________ 。
(5)目前, 溶液广泛地应用于脱硫脱硝。某课外小组同学设计了如图喷淋吸收塔装置
溶液广泛地应用于脱硫脱硝。某课外小组同学设计了如图喷淋吸收塔装置 如图
如图 。设计该装置的优点是
。设计该装置的优点是___________ 。脱硝反应中,每吸收标准状况下448mL的NO,转移的电子数为___________ mol。
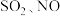 )直接排放会造成空气污染,需处理后才能排放。
)直接排放会造成空气污染,需处理后才能排放。(1)“纳米零价铁
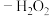 ”体系可将烟气中难溶的NO氧化为可溶的
”体系可将烟气中难溶的NO氧化为可溶的 。在一定温度下,将
。在一定温度下,将 溶液和HCl溶液雾化后与烟气按一定比例混合,以一定流速通过装有纳米零价铁的反应装置,可将烟气中的NO氧化。
溶液和HCl溶液雾化后与烟气按一定比例混合,以一定流速通过装有纳米零价铁的反应装置,可将烟气中的NO氧化。①
 催化
催化 分解产生HO·,HO·将NO氧化为
分解产生HO·,HO·将NO氧化为 的机理如下图所示,Y的化学式为
的机理如下图所示,Y的化学式为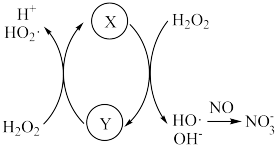
 反应生成HNO3的化学方程式为
反应生成HNO3的化学方程式为③纳米零价铁的作用是
④NO脱除率随温度的变化如下图所示。温度高于120℃时,NO脱除率随温度升高呈现下降趋势的主要原因是

 、
、 ,下列措施能提高尾气中NO和
,下列措施能提高尾气中NO和 去除率的有
去除率的有A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量NaOH溶液
(3)
 脱硝技术已成为使用广泛和成熟的烟气净化技术,脱硝效率高达
脱硝技术已成为使用广泛和成熟的烟气净化技术,脱硝效率高达 %以上。反应机理如下图所示,写出该反应发生的化学方程式
%以上。反应机理如下图所示,写出该反应发生的化学方程式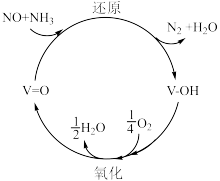
 溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO转化为
溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO转化为 的转化率随
的转化率随 溶液初始pH(用稀盐酸调节)的变化如图所示:
溶液初始pH(用稀盐酸调节)的变化如图所示: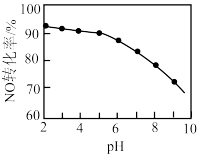
 溶液中,
溶液中, 氧化NO生成Cl-和
氧化NO生成Cl-和 ,其离子方程式为
,其离子方程式为②NaClO溶液的初始pH越小,NO转化率越高。其原因是
(5)目前,
 溶液广泛地应用于脱硫脱硝。某课外小组同学设计了如图喷淋吸收塔装置
溶液广泛地应用于脱硫脱硝。某课外小组同学设计了如图喷淋吸收塔装置 如图
如图 。设计该装置的优点是
。设计该装置的优点是
您最近一年使用:0次
9 .  是一种新型多功能绿色消毒剂。
是一种新型多功能绿色消毒剂。
I.某兴趣小组利用废铁屑(含少量 )制备高铁酸钠的工艺流程如图所示:
)制备高铁酸钠的工艺流程如图所示: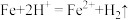 ;
; ;
;_______ 。
(2)“操作”中通入空气的目的是_______ 。
(3)“氧化”时发生反应的化学方程式为_______ 。
(4)称取一定质量碘化钾于碘量瓶中,加入 溶液和一定质量氟化钠固体,待溶解完毕;准确称取
溶液和一定质量氟化钠固体,待溶解完毕;准确称取 样品于碘量瓶中,待样品充分溶解后,加硫酸酸化至反应完全;淀粉作指示剂,用
样品于碘量瓶中,待样品充分溶解后,加硫酸酸化至反应完全;淀粉作指示剂,用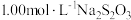 标准溶液进行滴定,消耗标准液体积为
标准溶液进行滴定,消耗标准液体积为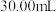 。已知
。已知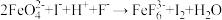 (未配平);
(未配平); 计算样品中
计算样品中 的质量分数
的质量分数_____ (写出计算过程)。
II. 主要用于废水处理。
主要用于废水处理。
(5) 净水原理如图所示。
净水原理如图所示。 是一种多功能水处理剂的原因为
是一种多功能水处理剂的原因为_______ 。 处理高氯废水中的有机物时,需在一定条件下使用。
处理高氯废水中的有机物时,需在一定条件下使用。
① 时,
时,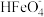 分解放出
分解放出 并产生
并产生 沉淀,该反应的离子方程式为
沉淀,该反应的离子方程式为_______ 。
②酸性溶液中 的氧化性大于
的氧化性大于 的氧化性。
的氧化性。 处理高氯废水中的有机物需在碱性条件下进行,其原因是
处理高氯废水中的有机物需在碱性条件下进行,其原因是_______ 。
 是一种新型多功能绿色消毒剂。
是一种新型多功能绿色消毒剂。I.某兴趣小组利用废铁屑(含少量
 )制备高铁酸钠的工艺流程如图所示:
)制备高铁酸钠的工艺流程如图所示:
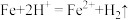 ;
; ;
;(2)“操作”中通入空气的目的是
(3)“氧化”时发生反应的化学方程式为
(4)称取一定质量碘化钾于碘量瓶中,加入
 溶液和一定质量氟化钠固体,待溶解完毕;准确称取
溶液和一定质量氟化钠固体,待溶解完毕;准确称取 样品于碘量瓶中,待样品充分溶解后,加硫酸酸化至反应完全;淀粉作指示剂,用
样品于碘量瓶中,待样品充分溶解后,加硫酸酸化至反应完全;淀粉作指示剂,用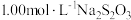 标准溶液进行滴定,消耗标准液体积为
标准溶液进行滴定,消耗标准液体积为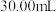 。已知
。已知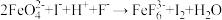 (未配平);
(未配平); 计算样品中
计算样品中 的质量分数
的质量分数II.
 主要用于废水处理。
主要用于废水处理。(5)
 净水原理如图所示。
净水原理如图所示。 是一种多功能水处理剂的原因为
是一种多功能水处理剂的原因为
 处理高氯废水中的有机物时,需在一定条件下使用。
处理高氯废水中的有机物时,需在一定条件下使用。①
 时,
时,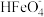 分解放出
分解放出 并产生
并产生 沉淀,该反应的离子方程式为
沉淀,该反应的离子方程式为②酸性溶液中
 的氧化性大于
的氧化性大于 的氧化性。
的氧化性。 处理高氯废水中的有机物需在碱性条件下进行,其原因是
处理高氯废水中的有机物需在碱性条件下进行,其原因是
您最近一年使用:0次
名校
解题方法
10 . 《新修本草》中描述“青矾”为“本来绿色,新出窟未见风者,正如琉璃。烧之赤色”。青矾加热时的反应为2FeSO4·7H2O Fe2O3+SO2↑+H2SO4+13H2O。下列说法正确的是
Fe2O3+SO2↑+H2SO4+13H2O。下列说法正确的是
 Fe2O3+SO2↑+H2SO4+13H2O。下列说法正确的是
Fe2O3+SO2↑+H2SO4+13H2O。下列说法正确的是| A.产物中含有3种非金属氧化物 | B.反应为分解反应 |
| C.SO2是氧化产物 | D.铁元素发生还原反应 |
您最近一年使用:0次



