名校
解题方法
1 . 利用物质类别及核心元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的常见化合价与部分物质类别的对应关系。回答下列问题:

(1)质量相同的a和b,物质的量之比为_______ 。将H2S与a混合,发生反应的氧化剂与还原剂的物质的量之比为_______ 。
(2)c的浓溶液能与S反应产生一种气体,该气体的化学式为_______ 。
(3)将足量的a通入BaCl2溶液中,下列说法正确的是_______(填标号)。
(4)宋代著名法医学家宋慈的《洗冤集录》中有“银针验毒”的记载,“银针验毒”的原理:4Ag+2H2S+O2=2Ag2S+2H2O。H2S在该反应中_______(填标号)。
(5)若e为正盐,且能被酸性K2Cr2O7氧化为Na2SO4,Cr2O 被还原为Cr3+,写出此反应的离子方程式:
被还原为Cr3+,写出此反应的离子方程式:_______ 。
(6)若e为酸式盐,将0.1mole的溶液中加入适量H2O2氧化后,稀释成10L溶液进行环保回收,此时稀释后溶液的pH为_______ 。

(1)质量相同的a和b,物质的量之比为
(2)c的浓溶液能与S反应产生一种气体,该气体的化学式为
(3)将足量的a通入BaCl2溶液中,下列说法正确的是_______(填标号)。
| A.溶液中出现白色沉淀 |
| B.溶液没有明显变化 |
| C.若再通入Cl2或NH3,则溶液中均会出现白色沉淀 |
| D.将溶液蒸干后仍然能得到BaCl2 |
| A.是氧化剂 | B.是还原剂 |
| C.既是氧化剂也是还原剂 | D.既不是氧化剂也不是还原剂 |
 被还原为Cr3+,写出此反应的离子方程式:
被还原为Cr3+,写出此反应的离子方程式:(6)若e为酸式盐,将0.1mole的溶液中加入适量H2O2氧化后,稀释成10L溶液进行环保回收,此时稀释后溶液的pH为
您最近一年使用:0次
2022-05-18更新
|
127次组卷
|
2卷引用: 重庆市万州第二高级中学2022-2023学年高三下学期2月月考化学试题
名校
2 . 钠及其化合物在生活和生产中有重要用途。
(1) 因外观和食盐相似,有咸味,容易使人误食中毒。已知
因外观和食盐相似,有咸味,容易使人误食中毒。已知 能发生如下反应:
能发生如下反应: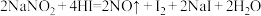 。请回答:
。请回答:
①上述反应中,氧化产物是___________ (填化学式),其中HI在反应中体现出的性质为___________ (填字母)。
A.酸性 B.氧化性 C.碱性 D.还原性
②某厂废液中含有3%~6%的 ,直接排放会造成污染,下列试剂能使
,直接排放会造成污染,下列试剂能使 转化为不引起二次污染的
转化为不引起二次污染的 的是
的是___________ (填字母)。
A.NaClO B. C.
C. D.
D.
(2) 是实验室常用的试剂,也常作呼吸面具和潜水艇里的供氧剂。
是实验室常用的试剂,也常作呼吸面具和潜水艇里的供氧剂。
①写出 与
与 反应的化学方程式
反应的化学方程式___________ 。
②将二氧化碳和水蒸气组成的混合气体8.0g通过足量的 粉末,完全吸收后固体质量增重3.2g,则该混合气体中水蒸气的质量为
粉末,完全吸收后固体质量增重3.2g,则该混合气体中水蒸气的质量为___________ 。
③将一定量的 固体投入到含有下列离子的溶液中:
固体投入到含有下列离子的溶液中: 、
、 、
、 、
、 ,完全反应后,溶液中上述离子数目几乎不变的是
,完全反应后,溶液中上述离子数目几乎不变的是___________ (填离子符号)。
(3) 是实验室中常用的物质。侯德榜“联合制碱法”将制碱技术发展到一个新的水平。该工艺以氯化钠为原料制取纯碱,主要流程如图所示(部分物质已略去)。
是实验室中常用的物质。侯德榜“联合制碱法”将制碱技术发展到一个新的水平。该工艺以氯化钠为原料制取纯碱,主要流程如图所示(部分物质已略去)。
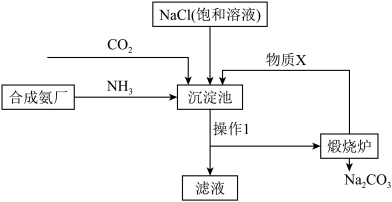
①上述流程中,物质X是___________ (填化学式)。
②写出沉淀池的化学反应方程式___________ 。
③下列关于侯德榜“联合制碱法”说法错误的是___________ (填字母)。
A.上述流程中滤液中可分离得到一种氮肥
B.上述流程应在饱和NaCl溶液中先通 ,再通
,再通
C.沉淀池中析出晶体利用了相同条件下物质溶解度的差异
D.该工艺的碳原子利用率理论上为100%
(1)
 因外观和食盐相似,有咸味,容易使人误食中毒。已知
因外观和食盐相似,有咸味,容易使人误食中毒。已知 能发生如下反应:
能发生如下反应: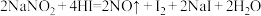 。请回答:
。请回答:①上述反应中,氧化产物是
A.酸性 B.氧化性 C.碱性 D.还原性
②某厂废液中含有3%~6%的
 ,直接排放会造成污染,下列试剂能使
,直接排放会造成污染,下列试剂能使 转化为不引起二次污染的
转化为不引起二次污染的 的是
的是A.NaClO B.
 C.
C. D.
D.
(2)
 是实验室常用的试剂,也常作呼吸面具和潜水艇里的供氧剂。
是实验室常用的试剂,也常作呼吸面具和潜水艇里的供氧剂。①写出
 与
与 反应的化学方程式
反应的化学方程式②将二氧化碳和水蒸气组成的混合气体8.0g通过足量的
 粉末,完全吸收后固体质量增重3.2g,则该混合气体中水蒸气的质量为
粉末,完全吸收后固体质量增重3.2g,则该混合气体中水蒸气的质量为③将一定量的
 固体投入到含有下列离子的溶液中:
固体投入到含有下列离子的溶液中: 、
、 、
、 、
、 ,完全反应后,溶液中上述离子数目几乎不变的是
,完全反应后,溶液中上述离子数目几乎不变的是(3)
 是实验室中常用的物质。侯德榜“联合制碱法”将制碱技术发展到一个新的水平。该工艺以氯化钠为原料制取纯碱,主要流程如图所示(部分物质已略去)。
是实验室中常用的物质。侯德榜“联合制碱法”将制碱技术发展到一个新的水平。该工艺以氯化钠为原料制取纯碱,主要流程如图所示(部分物质已略去)。
①上述流程中,物质X是
②写出沉淀池的化学反应方程式
③下列关于侯德榜“联合制碱法”说法错误的是
A.上述流程中滤液中可分离得到一种氮肥
B.上述流程应在饱和NaCl溶液中先通
 ,再通
,再通
C.沉淀池中析出晶体利用了相同条件下物质溶解度的差异
D.该工艺的碳原子利用率理论上为100%
您最近一年使用:0次
3 . 某废合金的主要成分为Sn、Cu、Pb、Fe,一种综合回收的工艺流程如图所示:

已知:常温下,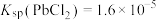 ,
, ,
, 。
。
回答下列问题:
(1)“氯化浸出”浸出液中金属阳离子主要有 、
、 、
、_______ ;浸渣的主要成分为_______ (填化学式)。“氯化没出”时温度不宜过高或过低的原因是_______ 。
(2)写出“还原”中Fe与 反应的化学方程式:
反应的化学方程式:_______ 。
(3)常温下,为使 完全沉淀,“调pH”时应使溶液pH不低于
完全沉淀,“调pH”时应使溶液pH不低于_______ (结果保留1位小数)。
(4)“氧化”时为检验 是否已被充分氧化,可取样滴加
是否已被充分氧化,可取样滴加_______ (填化学式)溶液。
(5)写出“沉铁”时发生反应的离子反应方程式:_______ 。
(6) 受热后可制得物质A,写出物质A的一种用途:
受热后可制得物质A,写出物质A的一种用途:_______ 。

已知:常温下,
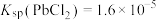 ,
, ,
, 。
。回答下列问题:
(1)“氯化浸出”浸出液中金属阳离子主要有
 、
、 、
、(2)写出“还原”中Fe与
 反应的化学方程式:
反应的化学方程式:(3)常温下,为使
 完全沉淀,“调pH”时应使溶液pH不低于
完全沉淀,“调pH”时应使溶液pH不低于(4)“氧化”时为检验
 是否已被充分氧化,可取样滴加
是否已被充分氧化,可取样滴加(5)写出“沉铁”时发生反应的离子反应方程式:
(6)
 受热后可制得物质A,写出物质A的一种用途:
受热后可制得物质A,写出物质A的一种用途:
您最近一年使用:0次
2023-02-27更新
|
604次组卷
|
2卷引用:重庆市乌江新高考协作体2023-2024学年高二上学期1月期末化学试题
名校
4 . 已知X是一种黄绿色气体,X、Y、Z都是有刺激性气味的气体,M是人类使用最多的一种金属单质,D是一种盐,受热易分解。现有以下转化关系,部分产物未标出。

试回答下列问题:
(1)写出下列物质的化学式:X_______ 、Y_______ 、M_______ 、D_______ 。
(2)写出下列反应的离子方程式。
①X+Y—A+B:_______ ;
②Z+C—红褐色沉淀:_______ 。
(3)Z是合成硝酸的重要原料,请写出其与氧气在催化剂的作用下反应的化学方程式:_______ 。
(4)大苏打(Na2S2O3)在照相、电影、纺织、化纤、造纸、皮革、农药等方面均有重要用途。现欲在实验室制备大苏打,从氧化还原角度分析,合理的是_______(填字母选项)。

试回答下列问题:
(1)写出下列物质的化学式:X
(2)写出下列反应的离子方程式。
①X+Y—A+B:
②Z+C—红褐色沉淀:
(3)Z是合成硝酸的重要原料,请写出其与氧气在催化剂的作用下反应的化学方程式:
(4)大苏打(Na2S2O3)在照相、电影、纺织、化纤、造纸、皮革、农药等方面均有重要用途。现欲在实验室制备大苏打,从氧化还原角度分析,合理的是_______(填字母选项)。
A. | B. |
C. | D. |
您最近一年使用:0次



