名校
解题方法
1 . 已知:SO2+I2+2H2O=SO +2I—+4H+。现将101.6mgI2固体溶于水配成400mL溶液,(为了便于观察,可以加几滴淀粉)用于吸收空气管道中的SO2,若管道中空气流量为40L/min,经过5min溶液恰好褪色,请计算:
+2I—+4H+。现将101.6mgI2固体溶于水配成400mL溶液,(为了便于观察,可以加几滴淀粉)用于吸收空气管道中的SO2,若管道中空气流量为40L/min,经过5min溶液恰好褪色,请计算:
(1)所用碘水溶液的物质的量浓度_____ mol/L。
(2)空气样品中SO2的含量_____ mg/L。
(3)若空气中SO2的浓度不超过0.02mg/L为合格,则上述空气质量_____ (填“合格”或“不合格”)。
 +2I—+4H+。现将101.6mgI2固体溶于水配成400mL溶液,(为了便于观察,可以加几滴淀粉)用于吸收空气管道中的SO2,若管道中空气流量为40L/min,经过5min溶液恰好褪色,请计算:
+2I—+4H+。现将101.6mgI2固体溶于水配成400mL溶液,(为了便于观察,可以加几滴淀粉)用于吸收空气管道中的SO2,若管道中空气流量为40L/min,经过5min溶液恰好褪色,请计算:(1)所用碘水溶液的物质的量浓度
(2)空气样品中SO2的含量
(3)若空气中SO2的浓度不超过0.02mg/L为合格,则上述空气质量
您最近一年使用:0次
2 . 玻璃仪器内壁残留的硫单质可用热的NaOH溶液洗涤除去,可能发生如下反应:
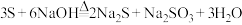
 ;
;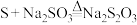
请计算:
(1)0.9600g硫单质与VmL1.000 热的NaOH溶液恰好完全反应,若只生成
热的NaOH溶液恰好完全反应,若只生成 和
和 ,则V=
,则V=______ 。
(2)6.400g硫单质与120.0mL1.000 热的NaOH溶液恰好完全反应,若只生成
热的NaOH溶液恰好完全反应,若只生成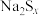 和
和 ,则x=
,则x=______ 。
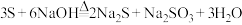
 ;
;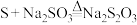
请计算:
(1)0.9600g硫单质与VmL1.000
 热的NaOH溶液恰好完全反应,若只生成
热的NaOH溶液恰好完全反应,若只生成 和
和 ,则V=
,则V=(2)6.400g硫单质与120.0mL1.000
 热的NaOH溶液恰好完全反应,若只生成
热的NaOH溶液恰好完全反应,若只生成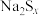 和
和 ,则x=
,则x=
您最近一年使用:0次
3 . 已知锌跟浓硫酸反应生成SO2,跟稀硫酸反应生成H2,32.5 g的锌与50 mL18.4 mol/L浓硫酸充分反应,锌完全溶解,同时收集到标准状况下的混合气体V L。将反应后的溶液稀释到500 mL,测得溶液中氢离子的浓度为0.08 mol/L。
(1)锌的物质的量为_______ 。
(2)反应过程中消耗的H2SO4的物质的量是_______ 。
(3)混合气体中SO2和H2的体积比为_______ 。
(1)锌的物质的量为
(2)反应过程中消耗的H2SO4的物质的量是
(3)混合气体中SO2和H2的体积比为
您最近一年使用:0次
2022-04-29更新
|
1138次组卷
|
3卷引用:浙江省宁波市六校2021-2022学年高一下学期期中联考化学试题
名校
4 . 200 mL NaOH与 的混合液中含
的混合液中含 ,现用此混合液处理尾气
,现用此混合液处理尾气 ,吸收一定量氯气后经检测吸收液中的溶质只有3种钠盐。现往吸收液滴加足量
,吸收一定量氯气后经检测吸收液中的溶质只有3种钠盐。现往吸收液滴加足量 溶液,产生白色沉淀,再滴加足量稀盐酸,白色沉淀减少,剩余白色沉淀质量为2.33g。求原溶液中NaOH和
溶液,产生白色沉淀,再滴加足量稀盐酸,白色沉淀减少,剩余白色沉淀质量为2.33g。求原溶液中NaOH和 的物质的量之比
的物质的量之比_______ 。(写出简要的计算过程)
 的混合液中含
的混合液中含 ,现用此混合液处理尾气
,现用此混合液处理尾气 ,吸收一定量氯气后经检测吸收液中的溶质只有3种钠盐。现往吸收液滴加足量
,吸收一定量氯气后经检测吸收液中的溶质只有3种钠盐。现往吸收液滴加足量 溶液,产生白色沉淀,再滴加足量稀盐酸,白色沉淀减少,剩余白色沉淀质量为2.33g。求原溶液中NaOH和
溶液,产生白色沉淀,再滴加足量稀盐酸,白色沉淀减少,剩余白色沉淀质量为2.33g。求原溶液中NaOH和 的物质的量之比
的物质的量之比
您最近一年使用:0次
2021-07-02更新
|
302次组卷
|
3卷引用:浙江省金华十校2020-2021学年高二下学期期末调研考试化学试题
5 . 实验室有一瓶部分被氧化的硫酸亚铁,为测定其被氧化程度,取10.0g样品溶于水配成100mL溶液。取两份溶液各10.0mL,第一份加入14.0mL0.500mol•L-1BaCl2溶液恰好完全反应;第二份恰好与8.0mL0.100mol•L-1的酸性KMnO4溶液完全反应。
(1)100mL溶液中SO 的物质的量浓度是
的物质的量浓度是____ mol•L-1。
(2)该样品中硫酸亚铁的质量分数是____ 。
(1)100mL溶液中SO
 的物质的量浓度是
的物质的量浓度是(2)该样品中硫酸亚铁的质量分数是
您最近一年使用:0次
2021-06-25更新
|
825次组卷
|
3卷引用:浙江省杭州市余杭、临平、萧山2020-2021学年高一下学期期末学业水平测试化学试题
20-21高一·浙江·阶段练习
解题方法
6 . 按要求完成下列空格:
(1)4.9 g硫酸的物质的量___________ mol;标准状况下,3.612×1023个氯气分子的物质的量为___________ mol。
(2)一定量的铜片与200 mL18 mol/L 的浓H2SO4充分反应,如果该反应过程中转移了0.2mol电子,生成的CuSO4的物质的量为___________ mol。
(3)7.8 g Na2O2投入200 mL水中,充分反应。
①该反应的化学方程式为___________ 。
②反应后溶液中溶质的物质的量浓度为___________ mol/L。(忽略反应前后溶液体积变化)
(1)4.9 g硫酸的物质的量
(2)一定量的铜片与200 mL18 mol/L 的浓H2SO4充分反应,如果该反应过程中转移了0.2mol电子,生成的CuSO4的物质的量为
(3)7.8 g Na2O2投入200 mL水中,充分反应。
①该反应的化学方程式为
②反应后溶液中溶质的物质的量浓度为
您最近一年使用:0次
20-21高一·浙江·阶段练习
解题方法
7 . 锌与100mL 18.4mol/L的浓硫酸充分反应后,锌完全溶解,同时生成混合气体31.36L (标准状况)。将反应后的溶液稀释至1L,测得溶液的c(H+ )=0.08mol/L。请计算:
(1)反应中共消耗Zn的质量为_______ g;
(2)气体的物质的量之比为n____ : n____ =______ 。
(1)反应中共消耗Zn的质量为
(2)气体的物质的量之比为n
您最近一年使用:0次
20-21高一·浙江·阶段练习
8 . 将一块锌片投入到100 mL18.5 mol·L-1浓H2SO4中,使之充分反应,观察到锌片完全溶解,同时生成气体33.6 L(标准状况下)。将反应后的溶液稀释至1 L,测得溶液中c(H+)为0.1 mol·L-1,求:
(1)消耗的锌的质量_________ 。
(2)气体A的成分以及含量_________ 。
(1)消耗的锌的质量
(2)气体A的成分以及含量
您最近一年使用:0次
真题
名校
9 . 玻璃仪器内壁残留的硫单质可用热KOH溶液洗涤除去,发生如下反应:
3S+6KOH 2K2S+K2SO3+3H2O
2K2S+K2SO3+3H2O
(x-1)S+K2S K2Sx(x=2~6)
K2Sx(x=2~6)
S+ K2SO3 K2S2O3
K2S2O3
请计算:
(1)0.480 g硫单质与V mL 1.00 mol·L-1热KOH溶液恰好完全反应,只生成K2S和K2SO3,则V=______ 。
(2)2.560 g硫单质与60.0 mL 1.00 mol·L-1热KOH溶液恰好完全反应,只生成K2Sx和K2S2O3,则x=______ 。(写出计算过程)
3S+6KOH
 2K2S+K2SO3+3H2O
2K2S+K2SO3+3H2O(x-1)S+K2S
 K2Sx(x=2~6)
K2Sx(x=2~6)S+ K2SO3
 K2S2O3
K2S2O3请计算:
(1)0.480 g硫单质与V mL 1.00 mol·L-1热KOH溶液恰好完全反应,只生成K2S和K2SO3,则V=
(2)2.560 g硫单质与60.0 mL 1.00 mol·L-1热KOH溶液恰好完全反应,只生成K2Sx和K2S2O3,则x=
您最近一年使用:0次
2021-01-09更新
|
4101次组卷
|
12卷引用:2021年1月新高考浙江化学高考真题
2021年1月新高考浙江化学高考真题(已下线)解密02 物质的量(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)专题18.化学计算-十年(2012-2021)高考化学真题分项汇编(浙江专用)(已下线)2021年1月浙江高考化学试题变式题26-31(已下线)解密02 物质的量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)浙江省金华市曙光学校2021-2022学年高三下学期5月模拟考试化学试题浙江省宁波市北仑中学2022-2023学年高一下学期期初返校考试化学(学考)试题浙江省宁波市鄞州中学(宁波鄞州蓝青高级中学)2023-2024学年高一上学期12月月考化学学科试题(已下线)解密02 物质的量(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)考向02 物质的量浓度及其相关计算-备战2022年高考化学一轮复习考点微专题(已下线)解密02 物质的量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题03 阿伏加德罗常数与化学计算 -2023年高考化学真题题源解密(新高考专用)
解题方法
10 . 实验室有一瓶部分被氧化的硫酸亚铁,取一定量样品溶于水配成100mL溶液。取两份溶液各10.00mL,第一份加入14.00mL0.5000mol•L-1BaCl2溶液恰好完全反应;第二份用0.1000mol•L-1KMnO4溶液(酸性)滴定,达到滴定终点时消耗KMnO48.00mL。
(1)100mL溶液中硫酸亚铁的物质的量浓度是_______ mol•L-1。
(2)若向剩余80mL原溶液中,加入NaOH溶液至反应完全,过滤所得沉淀在空气中充分灼烧。最后残渣的质量是_______ g。
(1)100mL溶液中硫酸亚铁的物质的量浓度是
(2)若向剩余80mL原溶液中,加入NaOH溶液至反应完全,过滤所得沉淀在空气中充分灼烧。最后残渣的质量是
您最近一年使用:0次



