名校
1 . 通常情况下,微粒A和B为分子,C和E为阳离子,D为阴离子,它们都含有10个电子;B溶于A后所得的物质可电离出C和D;A、B、E三种微粒反应后可得C和一种白色沉淀。请回答:
(1)用化学符号表示下列2种微粒: C:____________ D :_______________
(2)写出A、B、E三种微粒反应的离子方程式:______________ 和_______________________
(1)用化学符号表示下列2种微粒: C:
(2)写出A、B、E三种微粒反应的离子方程式:
您最近一年使用:0次
2019-04-15更新
|
128次组卷
|
2卷引用:江西省宜春市上高二中2018-2019学年高一下学期第一次月考化学试题
名校
2 . 现有A、B、C、D四种短周期元素,A分别与B、C、D结合生成甲、乙、丙三种化合物,且甲、乙、丙三分子中含有的质子数都为10,C、D结合生成化合物丁。有关元素的单质和甲、乙、丙、丁四种化合物的转化关系如下图所示:
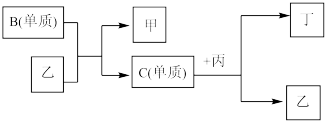
(1)写出B+乙―→甲+C的化学反应方程式______________________________________ 。
(2)根据以上条件可以确定A、B、C、D四种元素中的三种,不能被确定的第四种元素是________ (填写序号)。
①A ②B ③C ④D
(3)依据下列条件可以进一步确定上述第四种元素:
①甲与丙以及乙与丙均能够发生反应,②甲、丙都是无色、有刺激性气味的物质。
据此,请回答下列问题:
写出上述第四种元素在周期表中的位置________________ 。写出C+丙―→乙+丁的化学反应方程式_________________________________________ 。

(1)写出B+乙―→甲+C的化学反应方程式
(2)根据以上条件可以确定A、B、C、D四种元素中的三种,不能被确定的第四种元素是
①A ②B ③C ④D
(3)依据下列条件可以进一步确定上述第四种元素:
①甲与丙以及乙与丙均能够发生反应,②甲、丙都是无色、有刺激性气味的物质。
据此,请回答下列问题:
写出上述第四种元素在周期表中的位置
您最近一年使用:0次
2019-04-15更新
|
140次组卷
|
2卷引用:江西省宜春市上高二中2018-2019学年高一下学期第一次月考化学试题
3 . A、B、C为中学常见单质,其中一种为金属;通常情况下A为固体、B为黄绿色气体、C为无色气体。D、E、F、G、H、X均为化合物,其中X常温下是无色气体,其水溶液是一种无氧强酸溶液,E为黑色固体,H在常温下为液体。它们之间的转化如图所示(某些反应条件和部分反应产物已略去)。

(1)写出下列物质的化学式:D____________ X_______________ 。
(2)反应⑥的离子方程式为:___________________________ 。
(3)往G溶液中加入NaOH溶液观察到的现象是__________________ 。
(4)反应⑦的化学方程式为_____________________________________ ;
反应③的化学方程式为_____________________________________ ;
(5)除去G溶液中混有的少量D的方法是:_______________________________ 。

(1)写出下列物质的化学式:D
(2)反应⑥的离子方程式为:
(3)往G溶液中加入NaOH溶液观察到的现象是
(4)反应⑦的化学方程式为
反应③的化学方程式为
(5)除去G溶液中混有的少量D的方法是:
您最近一年使用:0次
名校
4 . A、B、C、D四种不同物质之间具有如图所示转化关系(反应条件及部分产物已略去)。下列有关物质的推断不正确 的是 ( )


| 选项 | 假设 | 结论 |
| A | A为NaOH溶液 | D可能是CO2 |
| B | B为CO | C可能是CO2 |
| C | C为FeCl2 ,D为Fe | A可能是盐酸 |
| D | C为SO2 | A可能是H2S |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2019-03-10更新
|
335次组卷
|
3卷引用:江西省宜丰中学2018-2019学年高一下学期第一次月考化学试题
5 . (1)下列各物质的转化关系如下图所示,其中A是高熔点物质,B是空气成分之一,D是红棕色固体,G是黄绿色气体,K是红褐色固体

回答下列问题:
①F的化学式是__________ 。D的化学式是__________ 。
②反应①的化学方程式是____________ 。
③反应②的离子反应方程式是_______________ 。
(2)有一瓶无色澄清溶液,可能含NH4+ 、K+、Na+、Mg2+、Ba2+、Al3+、Fe3+、SO42-、CO32-、Cl-、I-中的一种或几种,取该溶液进行如下实验:
①用pH试纸检验,表明溶液呈酸性;
②取部分溶液,加入少量CCl4及数滴新制的氯水,经振荡后静置,CCl4层呈紫红色;
③取部分溶液,加入少量稀NaOH溶液,使溶液从酸性逐渐转变为碱性,在滴加过程中及滴加完毕后,溶液中均无沉淀生成;
④取部分上述呈碱性的溶液,加Na2CO3溶液,有白色沉淀生成;
⑤将③得到的碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝。
根据上述实验事实确定并回答:在溶液中肯定存在的离子有__________ ,肯定不存在的离有___________ 。要确定是否存在的阴离子的实验方法是____________ 。

回答下列问题:
①F的化学式是
②反应①的化学方程式是
③反应②的离子反应方程式是
(2)有一瓶无色澄清溶液,可能含NH4+ 、K+、Na+、Mg2+、Ba2+、Al3+、Fe3+、SO42-、CO32-、Cl-、I-中的一种或几种,取该溶液进行如下实验:
①用pH试纸检验,表明溶液呈酸性;
②取部分溶液,加入少量CCl4及数滴新制的氯水,经振荡后静置,CCl4层呈紫红色;
③取部分溶液,加入少量稀NaOH溶液,使溶液从酸性逐渐转变为碱性,在滴加过程中及滴加完毕后,溶液中均无沉淀生成;
④取部分上述呈碱性的溶液,加Na2CO3溶液,有白色沉淀生成;
⑤将③得到的碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝。
根据上述实验事实确定并回答:在溶液中肯定存在的离子有
您最近一年使用:0次
解题方法
6 . 现有失去标签的CaCl2、AgNO3、HCl和Na2CO3四瓶溶液.为了确定四种溶液的成分,将它们编号为A、B、C、D后进行化学实验.实验记录如下:
根据上述实验完成下列各小题:
(1)A、C、D三瓶溶液分别是(用化学式表示所含溶质):A溶液________ ,C溶液________ ,D溶液________ 。
(2)写出B与D反应的离子方程式:________ ,写出B与C反应的离子方程式 :________ 。
| 实验顺序 | 实验内容 | 实验现象 |
| ① | A+B | 无明显现象 |
| ② | B+D | 有无色无味气体放出 |
| ③ | C+B | 有白色沉淀生成 |
| ④ | A+D | 有白色沉淀生成 |
(1)A、C、D三瓶溶液分别是(用化学式表示所含溶质):A溶液
(2)写出B与D反应的离子方程式:
您最近一年使用:0次
解题方法
7 . 某强酸性溶液X中仅含有Ba2+、Al3+、 、Fe2+、Fe3+、
、Fe2+、Fe3+、 、
、 、
、 、Cl-、
、Cl-、 中的一种或几种,取该溶液进行连续实验,实验过程如下
中的一种或几种,取该溶液进行连续实验,实验过程如下

根据以上信息,回答下列问题:
(1)仅根据上述连续实验不能确定溶液X中是否含有的离子分别是_______ 。
(2)若②中所用氢氧化钠浓度为2 mol/L,当加入10 mL时开始产生沉淀,55 mL时沉淀的量达到最大值0.03 mol,继续滴加沉淀的量保持不变,随后再滴加沉淀部分溶解,到60 mL时沉淀的量降为0.025 mol且保持不变,则原溶液中:c(Fe2+)为_______ mol/L、c(Fe3+)为_______ mol/L、c(Cl-)为_______ mol/L。(若有些离子不存在,请填0 mol/L)
 、Fe2+、Fe3+、
、Fe2+、Fe3+、 、
、 、
、 、Cl-、
、Cl-、 中的一种或几种,取该溶液进行连续实验,实验过程如下
中的一种或几种,取该溶液进行连续实验,实验过程如下
根据以上信息,回答下列问题:
(1)仅根据上述连续实验不能确定溶液X中是否含有的离子分别是
(2)若②中所用氢氧化钠浓度为2 mol/L,当加入10 mL时开始产生沉淀,55 mL时沉淀的量达到最大值0.03 mol,继续滴加沉淀的量保持不变,随后再滴加沉淀部分溶解,到60 mL时沉淀的量降为0.025 mol且保持不变,则原溶液中:c(Fe2+)为
您最近一年使用:0次
8 . A分解得到等物质的量的B、C、D,图中有部分生成物未标出,回答以下问题:
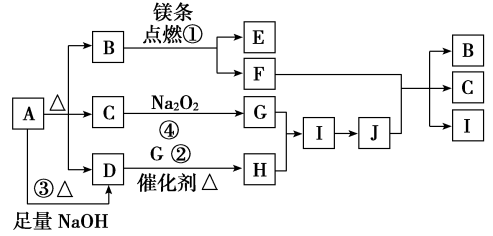
(1)A的化学式为_____________________________________ 。
(2)写出反应②的化学方程式:______________ 反应③的离子方程式:__________________
(3)J与F的反应体现出J具有______________ 的性质
(4)在反应④中,当生成标况下2.24 L G时,转移电子数目为________

(1)A的化学式为
(2)写出反应②的化学方程式:
(3)J与F的反应体现出J具有
(4)在反应④中,当生成标况下2.24 L G时,转移电子数目为
您最近一年使用:0次
名校
9 . 利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理。某工厂对制革工业污泥中Cr(Ⅲ)的处理工艺流程如下:

已知:①硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+。
②常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
(1)实验室用18.4 mol·L-1的浓硫酸配制480 mL 2 mol·L-1的硫酸,需量取浓硫酸_______ mL;配制时所用玻璃仪器除量筒、烧杯和玻璃棒外,还需_______ 。
(2)H2O2的作用是将滤液Ⅰ中的Cr3+转化为Cr2O ,写出此反应的离子方程式:
,写出此反应的离子方程式:_______ 。
(3)加入NaOH溶液使溶液呈碱性,既可以除去某些杂质离子,同时又可以将Cr2O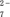 转化为
转化为______ (填微粒的化学式)
(4)钠离子交换树脂的反应原理为:Mn+ + n NaR = MRn + n Na+,则利用钠离子交换树脂可除去滤液Ⅱ中的金属阳离子有_____________ 。
(5)写出上述流程中用SO2进行还原时发生反应的离子方程式____________ 。

已知:①硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+。
②常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
| 阳离子 | Fe3+ | Mg2+ | Al3+ | Cr3+ |
| 沉淀完全时的pH | 3.7 | 11.1 | 5.4(>8溶解) | 9(>9溶解) |
(1)实验室用18.4 mol·L-1的浓硫酸配制480 mL 2 mol·L-1的硫酸,需量取浓硫酸
(2)H2O2的作用是将滤液Ⅰ中的Cr3+转化为Cr2O
 ,写出此反应的离子方程式:
,写出此反应的离子方程式:(3)加入NaOH溶液使溶液呈碱性,既可以除去某些杂质离子,同时又可以将Cr2O
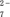 转化为
转化为(4)钠离子交换树脂的反应原理为:Mn+ + n NaR = MRn + n Na+,则利用钠离子交换树脂可除去滤液Ⅱ中的金属阳离子有
(5)写出上述流程中用SO2进行还原时发生反应的离子方程式
您最近一年使用:0次
名校
10 . 有X、Y、Z、W四种短周期元素,原子序数依次增大。X元素原子的半径最小。Z、W在周期表中处于邻位置,它们的单质在通常状况下均为无色气体。Y原子的最外层电子数是次外层子数的2倍。请回答:
(1)Z2的电子式为___________ ,YW2的结构式为____________ 。

(2)将X2、W2按上图所示通入某燃料电池中,其中,b电极的电极反应式为__________________ 。若有16gW2参加反应,转移的电子数是____________ 。
(3)由X、Y、Z、W四种元素组成的无机酸酸式盐_______ (化学式),与足量的NaOH溶液在加热条件下反应的离子方程式为________________________________________ 。
(1)Z2的电子式为

(2)将X2、W2按上图所示通入某燃料电池中,其中,b电极的电极反应式为
(3)由X、Y、Z、W四种元素组成的无机酸酸式盐
您最近一年使用:0次



