名校
1 . 劳动创造美好生活。下列化学知识正确且与相应劳动项目有关联的是
| 选项 | 化学知识 | 劳动项目 |
| A |  的活动性比 的活动性比 强 强 | 用 溶液制作印刷电路板 溶液制作印刷电路板 |
| B | 乙醇具有挥发性和还原性 | 用手持式酒精检测仪检测酒驾 |
| C | 外加电流法能减缓金属腐蚀速度 | 在船体外壳安装一定量锌块 |
| D | 铁与氯气不能发生反应 | 用钢瓶储存和运输液氯 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
2 . 下列陈述I与陈述II均正确,且具有因果联系的是
| 选项 | 陈述I | 陈述II |
| A | 小苏打可用于治疗胃酸过多 |  溶液显碱性 溶液显碱性 |
| B | 干燥的氯气可使有色鲜花褪色 |  具有漂白性 具有漂白性 |
| C | 氧化铝可用于制造耐高温材料 |  熔点高 熔点高 |
| D | 氯化铁溶液可用于刻蚀覆铜板 |  的还原性比 的还原性比 强 强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
3 . A、B、C、D、E为原子序数依次增大的五种短周期主族元素,A的核外电子总数与其周期序数相同;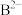 和
和 具有相同的电子构型;D、E为同周期元素,D的核外电子总数是其最外层电子数的3倍,E元素原子最外层有一个未成对电子。回答下列问题:
具有相同的电子构型;D、E为同周期元素,D的核外电子总数是其最外层电子数的3倍,E元素原子最外层有一个未成对电子。回答下列问题:
(1)酸性: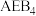
________ (填“>”“<”或“=”)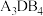 ,原因为
,原因为________ 。
(2)A和B可以形成一种含 的物质,该物质为
的物质,该物质为________ (填化学式),也可以形成一种含 的阳离子,该阳离子的电子式为
的阳离子,该阳离子的电子式为________ 。
(3)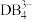 的空间结构为
的空间结构为________ 。
(4)实验室制取 时,常用CBA溶液来吸收多余的
时,常用CBA溶液来吸收多余的 ,实验室制
,实验室制 发生反应的化学方程式为
发生反应的化学方程式为________ 。
(5)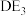 遇水可发生剧烈反应,生成大量酸性气体和D(显+3价)的含氧酸,则
遇水可发生剧烈反应,生成大量酸性气体和D(显+3价)的含氧酸,则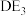 与水发生反应的化学方程式为
与水发生反应的化学方程式为________ 。
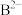 和
和 具有相同的电子构型;D、E为同周期元素,D的核外电子总数是其最外层电子数的3倍,E元素原子最外层有一个未成对电子。回答下列问题:
具有相同的电子构型;D、E为同周期元素,D的核外电子总数是其最外层电子数的3倍,E元素原子最外层有一个未成对电子。回答下列问题:(1)酸性:
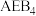
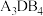 ,原因为
,原因为(2)A和B可以形成一种含
 的物质,该物质为
的物质,该物质为 的阳离子,该阳离子的电子式为
的阳离子,该阳离子的电子式为(3)
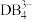 的空间结构为
的空间结构为(4)实验室制取
 时,常用CBA溶液来吸收多余的
时,常用CBA溶液来吸收多余的 ,实验室制
,实验室制 发生反应的化学方程式为
发生反应的化学方程式为(5)
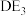 遇水可发生剧烈反应,生成大量酸性气体和D(显+3价)的含氧酸,则
遇水可发生剧烈反应,生成大量酸性气体和D(显+3价)的含氧酸,则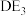 与水发生反应的化学方程式为
与水发生反应的化学方程式为
您最近一年使用:0次
2024-06-01更新
|
23次组卷
|
2卷引用:广东省部分学校2023-2024学年高二下学期期中联考化学试题
名校
解题方法
4 . 某同学利用W形管和V形管安装了下面微型实验装置,进行 的制备及探究
的制备及探究 的漂白性实验。下列说法正确的是
的漂白性实验。下列说法正确的是
 的制备及探究
的制备及探究 的漂白性实验。下列说法正确的是
的漂白性实验。下列说法正确的是
| A.固体粉末甲为二氧化锰 |
B.鲜花花瓣褪色说明 具有漂白性 具有漂白性 |
| C.W形管和V形管的玻璃泡能防止倒吸 |
D.溶液乙为碱液,与安全气球共同防止 逸出 逸出 |
您最近一年使用:0次
2024-05-31更新
|
248次组卷
|
5卷引用:广东省梅州市部分学校2024届高三下学期5月联考化学试卷
名校
5 . 臭氧是一种重要物质,是有机合成的氧化剂、替代氯气的净水剂。大气高空的臭氧层保护了地球生物的生存。下列说法正确的是
A. 与 与 互为同位素 互为同位素 | B.臭氧为含有极性共价键的极性分子 |
C.0.1mol氯气与水反应,可得到0.1mol | D.常温下,氯气是一种棕红色的有毒气体 |
您最近一年使用:0次
名校
解题方法
6 .  是重要的化工原料,某校化学实验兴趣小组同学利用如图所示装置(夹持装置已略去)进行氨气的制备实验。回答下列问题:
是重要的化工原料,某校化学实验兴趣小组同学利用如图所示装置(夹持装置已略去)进行氨气的制备实验。回答下列问题:_______ 。
(2)仪器 的名称为
的名称为_______ 。
(3)实验前,应先检查装置的气密性,检查的方法为_______ 。
(4)装置Ⅰ中发生反应的化学方程式为_______ 。
(5)用电子式表示 的形成过程:
的形成过程:_______ 。
(6)实验结束后,该兴趣小组甲同学对装置Ⅲ烧杯中所含物质的主要成分(不考虑溶剂)提出猜想:
ⅰ. 和
和 ;ⅱ.
;ⅱ. 和
和 ;ⅲ.
;ⅲ. 。
。
① 属于
属于_______ (填“离子”或“共价”)化合物。
②该小组乙同学认为猜想ⅰ错误,判断的理由为_______ 。
③乙同学认为分别向猜想ⅱ和ⅲ的溶液中滴加紫色石蕊溶液,可通过观察实验现象来区分ⅱⅲ.该兴趣小组丙同学认为不可以,原因为_______ (用离子方程式表示)。
 是重要的化工原料,某校化学实验兴趣小组同学利用如图所示装置(夹持装置已略去)进行氨气的制备实验。回答下列问题:
是重要的化工原料,某校化学实验兴趣小组同学利用如图所示装置(夹持装置已略去)进行氨气的制备实验。回答下列问题: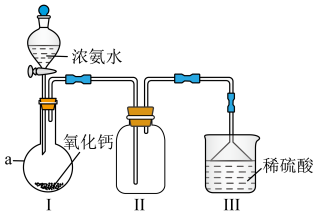
(2)仪器
 的名称为
的名称为(3)实验前,应先检查装置的气密性,检查的方法为
(4)装置Ⅰ中发生反应的化学方程式为
(5)用电子式表示
 的形成过程:
的形成过程:(6)实验结束后,该兴趣小组甲同学对装置Ⅲ烧杯中所含物质的主要成分(不考虑溶剂)提出猜想:
ⅰ.
 和
和 ;ⅱ.
;ⅱ. 和
和 ;ⅲ.
;ⅲ. 。
。①
 属于
属于②该小组乙同学认为猜想ⅰ错误,判断的理由为
③乙同学认为分别向猜想ⅱ和ⅲ的溶液中滴加紫色石蕊溶液,可通过观察实验现象来区分ⅱⅲ.该兴趣小组丙同学认为不可以,原因为
您最近一年使用:0次
2024-05-24更新
|
60次组卷
|
2卷引用:广东省部分学校2023-2024学年高二下学期期中联考化学试题
名校
7 . NA为阿伏加德罗常数的值。下列说法正确的是
A.加热条件下,含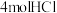 的浓盐酸与足量的 的浓盐酸与足量的 充分反应后,所得 充分反应后,所得 的分子总数为NA 的分子总数为NA |
B.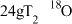 的中子数为14 NA 的中子数为14 NA |
C.常温下,将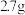 铝片投入足量的浓硝酸中,铝失去的电子数为0.3 NA 铝片投入足量的浓硝酸中,铝失去的电子数为0.3 NA |
D.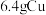 与足量S粉共热充分反应时转移电子数为0.2 NA 与足量S粉共热充分反应时转移电子数为0.2 NA |
您最近一年使用:0次
8 . 下列陈述I和陈述Ⅱ均正确,且具有因果关系的是
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | HCl的酸性强于CH3COOH | 盐酸的pH一定小于醋酸溶液 |
| B | 通过煤的干馏可获得苯、甲苯等化工原料 | 煤的干馏属于化学变化 |
| C | 将Cl2通入溴水中,溴水褪色 | Cl2具有漂白性 |
| D | 将金属Na加入CuSO4溶液中,析出红色固体 | 还原性:Na>Cu |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-04-23更新
|
840次组卷
|
2卷引用:2024届广东省肇庆市高三上学期二模化学试题
解题方法
9 . 将 分别通入下列溶液,实验现象和结论均正确的是
分别通入下列溶液,实验现象和结论均正确的是
 分别通入下列溶液,实验现象和结论均正确的是
分别通入下列溶液,实验现象和结论均正确的是| 选项 | 溶液 | 现象 | 结论 |
| A |  溶液 溶液 | 溶液由浅绿色变棕黄色 |  有还原性 有还原性 |
| B | 品红溶液 | 品红褪色 |  有漂白性 有漂白性 |
| C |  溶液 溶液 | 澄清溶液变浑浊 |  与 与 反应产生 反应产生 |
| D | 石蕊溶液 | 石蕊变红 | 氯水呈酸性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
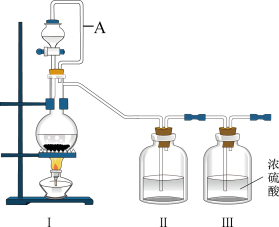
10 . 亚硝酰氯(NOCl,熔点:-64.5℃,沸点:-5.5℃)是一种黄色气体,遇水易水解。可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成。
(1)甲组同学拟用同一装置Ⅰ、Ⅱ、Ⅲ分别制备纯净干燥的NO和
_______ 。写出该装置制备氯气的离子方程式:_______ 。
(2)乙组同学利用甲组制得的NO和 制备NOCl,装置如图所示:
制备NOCl,装置如图所示:________ 。
②装置连接顺序为a→________ (按气流自左向右方向,用小写字母表示)。
③装置Ⅷ中吸收尾气时,NOCl发生反应的化学方程式为_______ 。
(3)丙组同学查阅资料,查得王水是浓硝酸与浓盐酸的混酸,一定条件下混酸可生成亚硝酰氯和氯气,该反应的化学方程式为______ 。
(4)丁组同学用以下方法测定亚硝酰氯(NOCl)纯度:取Ⅷ中所得液体m克溶于水,配制成250mL溶液,取出25.00 mL,用c mol/L 溶液反应,消耗
溶液反应,消耗 溶液的体积为bmL。亚硝酰氯(NOCl)的质量分数为
溶液的体积为bmL。亚硝酰氯(NOCl)的质量分数为________ (用代数式表示即可)。
(1)甲组同学拟用同一装置Ⅰ、Ⅱ、Ⅲ分别制备纯净干燥的NO和

(2)乙组同学利用甲组制得的NO和
 制备NOCl,装置如图所示:
制备NOCl,装置如图所示: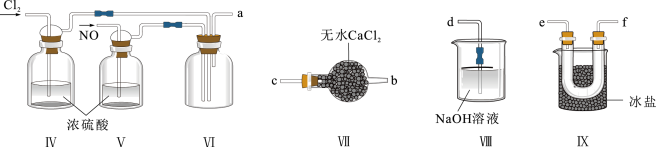
②装置连接顺序为a→
③装置Ⅷ中吸收尾气时,NOCl发生反应的化学方程式为
(3)丙组同学查阅资料,查得王水是浓硝酸与浓盐酸的混酸,一定条件下混酸可生成亚硝酰氯和氯气,该反应的化学方程式为
(4)丁组同学用以下方法测定亚硝酰氯(NOCl)纯度:取Ⅷ中所得液体m克溶于水,配制成250mL溶液,取出25.00 mL,用c mol/L
 溶液反应,消耗
溶液反应,消耗 溶液的体积为bmL。亚硝酰氯(NOCl)的质量分数为
溶液的体积为bmL。亚硝酰氯(NOCl)的质量分数为
您最近一年使用:0次



