1 . 为了探究HClO的漂白性,某同学设计了如下的实验。
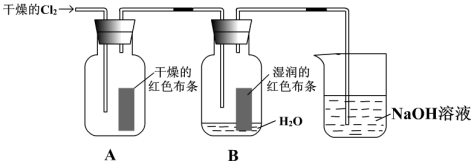
(1)写出Cl2与水反应的化学方程式_______ 。
(2)通入Cl2后,集气瓶A中的现象是_______ ,集气瓶B中的现象是_______ 。
(3)烧杯中发生反应的化学方程式是_______ 。

(1)写出Cl2与水反应的化学方程式
(2)通入Cl2后,集气瓶A中的现象是
(3)烧杯中发生反应的化学方程式是
您最近一年使用:0次
22-23高一下·上海浦东新·期中
名校
2 . 下列化合物中,能由组成该化合物的两种元素的单质直接化合而成的是
A. | B. | C.CuS | D. |
您最近一年使用:0次
3 . 按照图示装置进行实验,气体通入后使瓶中少量固体溶解,下列组合不符合要求的是


| 选项 | 气体 | 固体 | 液体 |
| A |  |  |  溶液 溶液 |
| B |  |  |  溶液 溶液 |
| C |  |  |  溶液 溶液 |
| D |  |  |  溶液 溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
4 . 如图所示,红纸①~④的大小相同,其中红纸①是干燥的,红纸②~④分别用相同体积的如表所示试剂润湿。向Ca(ClO)2粉末上滴加几滴浓盐酸,产生大量黄绿色气体,立即用玻璃片盖住培养皿,红纸的变化如表所示。已知酸性:H2CO3>HClO,且HClO与NaHCO3不反应。下列对于该实验的分析错误的是
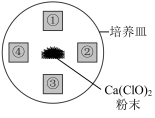

| 红纸编号 | 试剂 | 红纸的变化 |
| ① | - | 不褪色 |
| ② | 蒸馏水 | 逐渐褪色 |
| ③ | 饱和食盐水 | 几乎不褪色 |
| ④ | NaHCO溶液(调至pH=7) | 快速褪色 |
| A.对比①②的现象,说明Cl2没有漂白性 |
| B.对比②③的现象,说明能使红纸褪色的微粒是HClO |
| C.对比②④的现象,说明能使红纸褪色的微粒一定不是H+ |
| D.对比①②的现象,说明②上发生了反应:Cl2+H2O=HCl+HClO |
您最近一年使用:0次
5 .  表示阿伏加德罗常数的值,下列说法中正确的是
表示阿伏加德罗常数的值,下列说法中正确的是
 表示阿伏加德罗常数的值,下列说法中正确的是
表示阿伏加德罗常数的值,下列说法中正确的是A.1  溶液中所含钠离子数为2 溶液中所含钠离子数为2 |
B.常温常压下,22g  中含有的原子数为1.5 中含有的原子数为1.5 |
C.常温下,1mol  与足量的稀NaOH溶液反应,转移的电子数为2 与足量的稀NaOH溶液反应,转移的电子数为2 |
D.标准状况下,2.24L  中含有的共价键数目为0.4 中含有的共价键数目为0.4 |
您最近一年使用:0次
名校
6 . 已知: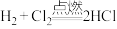 。下列说法不正确的是
。下列说法不正确的是
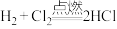 。下列说法不正确的是
。下列说法不正确的是
A. 中的 中的 键电子云轮廓图: 键电子云轮廓图: |
| B.燃烧生成的HCl气体与空气中的水蒸气结合呈雾状 |
| C.久置工业盐酸常显黄色,是因盐酸中溶解了氯气的缘故 |
D.可通过原电池将 与 与 反应的化学能转化为电能 反应的化学能转化为电能 |
您最近一年使用:0次
名校
解题方法
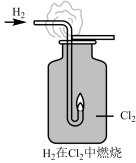
7 . 实验室采用如图所示装置制取氯气并验证其性质,下列说法错误的是
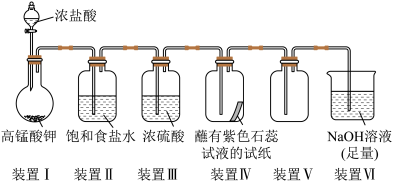

A.装置Ⅰ中反应的离子方程式为 |
| B.装置Ⅱ中饱和食盐水的作用是除去挥发出来的氯化氢气体 |
| C.装置Ⅳ中可观察到试纸先变红后褪色 |
D.每转移0.2mol电子,同时生成2.24L  |
您最近一年使用:0次
名校
解题方法
8 . 下列说法正确的是
| A.氯气与氢气在光照下反应生成HCl,工业常用此方法生产盐酸 |
| B.CO2通入氨的饱和NaCl溶液中生成Na2CO3沉淀 |
| C.控制合适的条件,可实现在铁皮表面电镀锡 |
| D.FeSO4·7H2O隔绝空气高温分解,产物为Fe2O3、O2、SO3和H2O |
您最近一年使用:0次
9 . 向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化情况如图所示。则下列说法中正确的是


| A.还原性:I-<Fe2+<Br- |
| B.原混合溶液中Br-的物质的量为4mol |
| C.线段BC表示Cl-的物质的量变化 |
| D.原溶液中:n(Fe2+):n(I-):n(Br-)=2:1:3 |
您最近一年使用:0次
10 . 下列物质不能通过单质间直接化合生成的是
| A.Cu2S | B.SO3 | C.Fe3O4 | D.FeCl3 |
您最近一年使用:0次



