1 . 溴及其化合物是重要的化工基础原料,广泛应用于制药、染料、电子、日化等行业。
Ⅰ.用图所示装置A可制取氯气。将纯净的氯气通入装置C的NaBr溶液中可以在实验室制取少量溴单质。_______ 。
(2)为了富集生成的溴单质,用热空气吹出,并在装置D中收集,则装置D中可选用的试剂为_______。
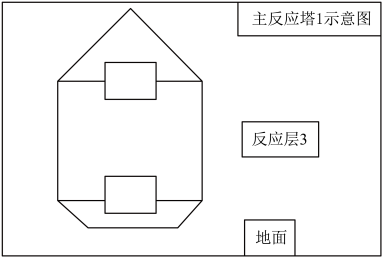
Ⅱ.工业上从海水中提取 过程更为复杂。研究集中在空气吹出法,空气吹出法提溴对原料的适应性高,但吹出设备庞大,且能耗高。某工厂针对空气吹出法的缺点进行工艺改造,提出连续双段真空提溴工艺,如图转化过程:
过程更为复杂。研究集中在空气吹出法,空气吹出法提溴对原料的适应性高,但吹出设备庞大,且能耗高。某工厂针对空气吹出法的缺点进行工艺改造,提出连续双段真空提溴工艺,如图转化过程:_______ 。主反应塔1中温度保持在82~99℃,减少了水蒸气的用量。从化学性质的角度分析这么做的主要目的有两点:①减少氯气与水的反应,②减少_______ 反应。从经济角度来看这么做还可以减少的_______ 用量。
(4)为了让原料卤水与氯气在主反应塔1中更充分反应,请将正确装置对应的选项填在图中“□”处:_______ 。_______ 。冷凝器需要铺设循环冷却水管道,循环冷却水管道中水流方向是_______ (填“从地面到顶端”或“从顶端到地面”),请说明原因_______ 。
(6)在分离器中经冷凝、分离、纯化后制得精溴。少量氯、溴与混合废气需要经过水蒸气喷射泵喷入气体吸收器。此时,还需进行酸化调节,再经过排水管通入主反应塔1中循环利用。请写出吸收器中酸化调节主要发生的离子反应方程式:_______ 。
Ⅰ.用图所示装置A可制取氯气。将纯净的氯气通入装置C的NaBr溶液中可以在实验室制取少量溴单质。
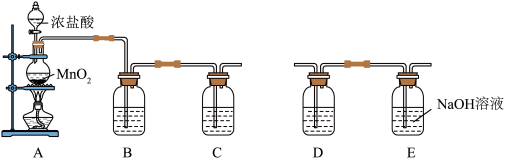
(2)为了富集生成的溴单质,用热空气吹出,并在装置D中收集,则装置D中可选用的试剂为_______。
A. | B.NaOH | C.KI | D. |
Ⅱ.工业上从海水中提取
 过程更为复杂。研究集中在空气吹出法,空气吹出法提溴对原料的适应性高,但吹出设备庞大,且能耗高。某工厂针对空气吹出法的缺点进行工艺改造,提出连续双段真空提溴工艺,如图转化过程:
过程更为复杂。研究集中在空气吹出法,空气吹出法提溴对原料的适应性高,但吹出设备庞大,且能耗高。某工厂针对空气吹出法的缺点进行工艺改造,提出连续双段真空提溴工艺,如图转化过程:
(4)为了让原料卤水与氯气在主反应塔1中更充分反应,请将正确装置对应的选项填在图中“□”处:

(6)在分离器中经冷凝、分离、纯化后制得精溴。少量氯、溴与混合废气需要经过水蒸气喷射泵喷入气体吸收器。此时,还需进行酸化调节,再经过排水管通入主反应塔1中循环利用。请写出吸收器中酸化调节主要发生的离子反应方程式:
您最近一年使用:0次
名校
解题方法
2 . 某校化学实验兴趣小组同学设计了如图所示的实验装置(支撑用的铁架台省略),探究实验室制备 并验证氯气的某些性质。
并验证氯气的某些性质。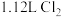 (标准状况下),则被氧化的
(标准状况下),则被氧化的
___________  ,反应中转移电子的物质的量为
,反应中转移电子的物质的量为___________ 。
(2)A中产生白色沉淀,甲同学认为是 与水反应产生
与水反应产生 的结果,写出其中发生反应的离子方程式
的结果,写出其中发生反应的离子方程式___________ ,___________ 。
(3)乙同学则认为A中的现象不足以说明白色沉淀是 与水反应产生
与水反应产生 的结果,因为生成的
的结果,因为生成的 中混有杂质
中混有杂质 ,所以应在A之前增加一个洗气瓶除去
,所以应在A之前增加一个洗气瓶除去 ,洗气瓶中所盛试剂是
,洗气瓶中所盛试剂是___________ 。
(4)装置C和D中出现的不同现象说明的问题是___________ 。
(5)装置E上面蘸有下列浓溶液的棉花可用于吸收氯气的是___________ (填字母)。
a. 溶液 b.
溶液 b. 溶液 c.
溶液 c. 溶液 d.浓硫酸 e.
溶液 d.浓硫酸 e. 溶液
溶液
(6)设计装置E、F的目的是比较 、
、 、
、 的氧化性,反应一段时间后,观察到装置E中的现象是
的氧化性,反应一段时间后,观察到装置E中的现象是___________ ,然后打开装置E的活塞,将E中的少量溶液加到装置F中,振荡,观察到的现象是___________ ,甲同学认为据上述现象可以说明氧化性 ,乙同学却认为不可以说明,理由是
,乙同学却认为不可以说明,理由是___________ 。
 并验证氯气的某些性质。
并验证氯气的某些性质。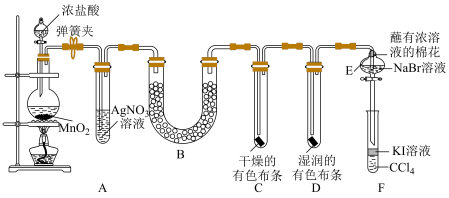
 (标准状况下),则被氧化的
(标准状况下),则被氧化的
 ,反应中转移电子的物质的量为
,反应中转移电子的物质的量为(2)A中产生白色沉淀,甲同学认为是
 与水反应产生
与水反应产生 的结果,写出其中发生反应的离子方程式
的结果,写出其中发生反应的离子方程式(3)乙同学则认为A中的现象不足以说明白色沉淀是
 与水反应产生
与水反应产生 的结果,因为生成的
的结果,因为生成的 中混有杂质
中混有杂质 ,所以应在A之前增加一个洗气瓶除去
,所以应在A之前增加一个洗气瓶除去 ,洗气瓶中所盛试剂是
,洗气瓶中所盛试剂是(4)装置C和D中出现的不同现象说明的问题是
(5)装置E上面蘸有下列浓溶液的棉花可用于吸收氯气的是
a.
 溶液 b.
溶液 b. 溶液 c.
溶液 c. 溶液 d.浓硫酸 e.
溶液 d.浓硫酸 e. 溶液
溶液(6)设计装置E、F的目的是比较
 、
、 、
、 的氧化性,反应一段时间后,观察到装置E中的现象是
的氧化性,反应一段时间后,观察到装置E中的现象是 ,乙同学却认为不可以说明,理由是
,乙同学却认为不可以说明,理由是
您最近一年使用:0次
名校
解题方法
3 . X、Y、Z、W为原子序数依次增大的短周期主族元素,X、Y同周期位置相邻,Y、Z同主族,Z、W位置相邻。若Y原子的最外层电子数是次外层电子数的3倍,下列说法中正确的是
A.原子半径: |
B.最高价氧化物对应水化物的酸性: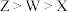 |
| C.4种元素的单质中,Z单质的熔、沸点最高 |
| D.W单质是一种具有漂白性的物质 |
您最近一年使用:0次
名校
解题方法
4 . 某兴趣小组研究铁盐的制备和性质。
实验I.制备FeCl2:装置如图所示(加持装置省略);已知FeCl2极易水解。
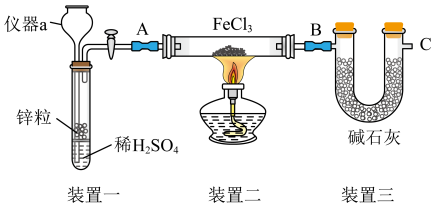
(1)仪器a的名称是_______ 。
(2)装置二中制备FeCl2的化学方程式是_____ ,装置三的作用是①_____ ;②_____ 。
(3)该装置存在一定的缺陷,可在_______ 位置(填“A”“B”或“C”)增加如下装置。如下装置中气体从_______ (填“a”或“b”)流入;洗气瓶中盛装的是_______ 。
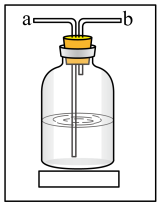
(4)为消除工业废气中的Cl2对环境的污染,将废气通过含有铁粉的FeCl2溶液,即可有效地除去Cl2,用离子方程式表示处理过程的原理_______ 。
实验Ⅱ.探究性质
(5) FeCl2溶液滴加NaOH溶液后会出现灰绿色沉淀,有同学猜测灰绿色沉淀是Fe(OH)2和Fe(OH)3的混合物。为探究是否存在Fe(OH)2,可取灰绿色沉淀,向其中加入_______ 溶液,再加入_______ 溶液,若观察到_______ 现象,证明灰绿色沉淀中含有Fe(OH)2。
实验I.制备FeCl2:装置如图所示(加持装置省略);已知FeCl2极易水解。

(1)仪器a的名称是
(2)装置二中制备FeCl2的化学方程式是
(3)该装置存在一定的缺陷,可在

(4)为消除工业废气中的Cl2对环境的污染,将废气通过含有铁粉的FeCl2溶液,即可有效地除去Cl2,用离子方程式表示处理过程的原理
实验Ⅱ.探究性质
(5) FeCl2溶液滴加NaOH溶液后会出现灰绿色沉淀,有同学猜测灰绿色沉淀是Fe(OH)2和Fe(OH)3的混合物。为探究是否存在Fe(OH)2,可取灰绿色沉淀,向其中加入
您最近一年使用:0次
名校
解题方法
5 . 某小组设计如图所示实验探究卤素的性质,实验过程中观察到乙中现象:无色→蓝色→棕黄色→无色。已知: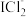 (红色)、
(红色)、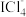 (棕色)、
(棕色)、 (无色)。
(无色)。 +5I- +6H+=3I2+3H2O。
+5I- +6H+=3I2+3H2O。
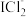 (红色)、
(红色)、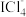 (棕色)、
(棕色)、 (无色)。
(无色)。 +5I- +6H+=3I2+3H2O。
+5I- +6H+=3I2+3H2O。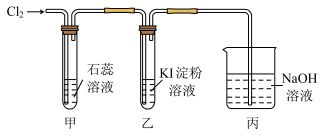
| A.丙的作用是吸收尾气,避免氯气排入空气中污染环境 |
| B.甲中现象是先变红色后褪色,微热后又变红色 |
C.乙中变棕黄色是因为I2 被氧化成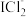 和 和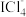 的混合物 的混合物 |
D.反应结束后,可用淀粉KI试纸和醋酸检验乙中无色溶液是否含 |
您最近一年使用:0次
2024-03-18更新
|
252次组卷
|
2卷引用:福建省福建师范大学附属中学2023-2024学年高三下学期综合测试三(4月月考)化学试题
名校
解题方法
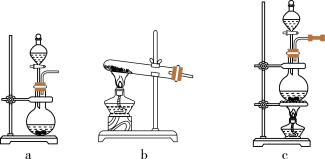
6 . 实验室用浓盐酸和MnO2制取并探究Cl2化学性质,装置图下图所示:
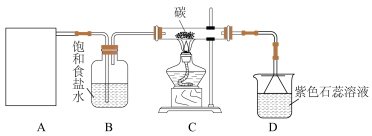
(1)A是氯气发生装置,该实验中A部分的装置是___________ (填字母),A装置中盛放浓盐酸的仪器是___________ 。
(2)现若要制备体积为448 mL的氯气(标准状况下),理论上需要MnO2的质量为___________ 反应中被氧化的HCl的物质的量为___________ ,
(3)从C装置出来的气体中含有CO2和HCl,则从B装置导出的气体成分是___________ ,请写出C装置中反应的化学方程式___________ 。
(4)D装置中可能观察到的现象是___________ ,有同学认为若要更好地吸收尾气,烧杯中溶液可以换成___________ (填字母)。
a.饱和NaHCO3溶液 b.饱和NaCl溶液 c.NaOH溶液
(5)有同学提出利用装置a,选用KMnO4与浓盐酸反应也可制备Cl2,则反应的化学方程式为___________ ,反应中氧化剂与还原剂的物质的量之比为___________ 。

(1)A是氯气发生装置,该实验中A部分的装置是

(2)现若要制备体积为448 mL的氯气(标准状况下),理论上需要MnO2的质量为
(3)从C装置出来的气体中含有CO2和HCl,则从B装置导出的气体成分是
(4)D装置中可能观察到的现象是
a.饱和NaHCO3溶液 b.饱和NaCl溶液 c.NaOH溶液
(5)有同学提出利用装置a,选用KMnO4与浓盐酸反应也可制备Cl2,则反应的化学方程式为
您最近一年使用:0次
解题方法
7 . 下列有关氯气的离子方程式书写正确的是
A.氯气与水发生反应: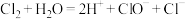 |
B.氯气通入 溶液发生反应: 溶液发生反应: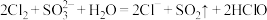 |
C.氯气通入石灰乳中制备漂白粉: |
D.氯气通入 溶液发生反应: 溶液发生反应: |
您最近一年使用:0次
8 . 实验室里可用如下图所示的装置制取氯酸钾、次氯酸钠,并验证氯水的性质。
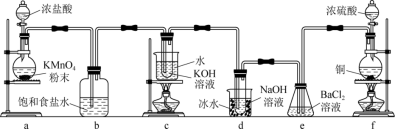
图中a为氯气发生装置,c的试管中盛有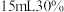 的
的 溶液,并置于热水浴中,d的试管中盛有
溶液,并置于热水浴中,d的试管中盛有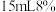 的
的 溶液,并置于冰水浴中,f为
溶液,并置于冰水浴中,f为 的发生装置。
的发生装置。
(1)制取 时,在烧瓶中先加入一定量的
时,在烧瓶中先加入一定量的 固体,再通过
固体,再通过___________ (填写仪器名称)向烧瓶中加入适量的浓盐酸。若反应中转移的电子物质的量为 ,则在标准状况下产生的
,则在标准状况下产生的 的体积为
的体积为___________ 。
(2)比较制取氯酸钾和次氯酸钠的条件,两者的差异是___________ 。
(3)将d中余气与f中产生的气体通入e中,产生的现象是___________ ,请用化学方程式表示产生此现象的原因:___________ 、___________ 。
(4)该实验有一处明显的缺点是___________ 。而工业上为了变废为宝,可用多种方式处理硫酸工业排出的尾气(主要含 ),其中一种便是用氨水来吸收。写出用过量氨水吸收尾气的离子方程式:
),其中一种便是用氨水来吸收。写出用过量氨水吸收尾气的离子方程式:___________ 。

图中a为氯气发生装置,c的试管中盛有
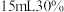 的
的 溶液,并置于热水浴中,d的试管中盛有
溶液,并置于热水浴中,d的试管中盛有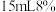 的
的 溶液,并置于冰水浴中,f为
溶液,并置于冰水浴中,f为 的发生装置。
的发生装置。(1)制取
 时,在烧瓶中先加入一定量的
时,在烧瓶中先加入一定量的 固体,再通过
固体,再通过 ,则在标准状况下产生的
,则在标准状况下产生的 的体积为
的体积为(2)比较制取氯酸钾和次氯酸钠的条件,两者的差异是
(3)将d中余气与f中产生的气体通入e中,产生的现象是
(4)该实验有一处明显的缺点是
 ),其中一种便是用氨水来吸收。写出用过量氨水吸收尾气的离子方程式:
),其中一种便是用氨水来吸收。写出用过量氨水吸收尾气的离子方程式:
您最近一年使用:0次
名校
9 . 下列说法中,正确的是
| A.液氯不导电是非电解质,氯水能导电是强电解质 |
| B.在常温常压下,11.2升氯气所含的原子数目为NA |
| C.氯气可以使湿润的有色布条褪色,但实际起漂白作用的物质是次氯酸而不是氯气 |
| D.1mol氯气参加反应,转移的电子数一定为NA |
您最近一年使用:0次
名校
10 . 简要回答下列问题
(1)氢氧化铝是典型且常用的抗酸药,具有抗酸、吸着、局部止血和保护溃疡面等作用。请用化学方程式表示其治疗胃酸过多的原理:___________ 。
(2)写出Cu在Cl2中燃烧的化学方程式:___________ 。
(3)如何用化学方法辨别溶液中是否含氯离子:___________ 。
(4)实验室浓硝酸应保存在棕色试剂瓶中并放置在阴凉处,其原因是______ (用化学方程式表示)。

(1)氢氧化铝是典型且常用的抗酸药,具有抗酸、吸着、局部止血和保护溃疡面等作用。请用化学方程式表示其治疗胃酸过多的原理:
(2)写出Cu在Cl2中燃烧的化学方程式:
(3)如何用化学方法辨别溶液中是否含氯离子:
(4)实验室浓硝酸应保存在棕色试剂瓶中并放置在阴凉处,其原因是
您最近一年使用:0次



