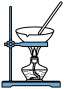
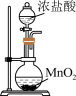
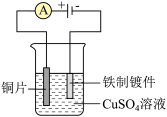
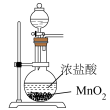
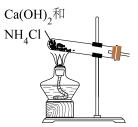
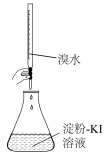
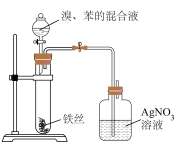
1 . 利用下列装置和试剂进行实验,能达到实验目的的是
|
|
|
|
| A | B | C | D |
A.可由 制取无水 制取无水 固体 固体 |
| B.实验室制氯气 |
| C.测定中和反应的反应热 |
| D.铁片表面镀铜 |
您最近一年使用:0次
2 . 下列实验装置(部分夹持装置略)设计或操作能够达到实验目的的是
|
|
| A.实验室制取氯气 | B.制备 |
|
|
| C.测定KI溶液的浓度 | D.验证苯与液溴发生取代反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . 设NA为阿伏加德罗常数的值,下列说法正确的是
| A.含0.4molHCl的盐酸与足量MnO2加热反应生成氯气,转移电子数为0.2NA |
| B.标准状况下,2.24LH2O中含有H-O数目为0.2NA |
| C.0.1mol·L-1的Na2CO3溶液中阴离子数目一定小于0.1NA |
| D.常温下1LpH=2的硫酸溶液中H+的数目为0.01NA |
您最近一年使用:0次
4 . 下列反应的离子方程式表述不正确 的是
A.氯化铝溶液与过量浓氨水混合: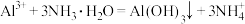 |
B.少量 通入 通入 溶液中: 溶液中: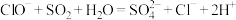 |
C.硫酸铜遇到难溶的 ,慢慢转变为铜蓝 ,慢慢转变为铜蓝 |
D.二氧化锰与浓盐酸共热: |
您最近一年使用:0次
5 . 设NA为阿伏加德罗常数的值,下列说法正确的是
| A.标准状况下,22.4LSO2和11.2LO2充分反应,生成SO3分子数为NA |
| B.0.1mol甲基(-CH3)中所含的电子数目为NA |
| C.足量的浓盐酸与8.7gMnO2充分反应,转移电子数为0.2NA |
| D.1LpH=2的硫酸溶液中含氢原子数目为0.01NA |
您最近一年使用:0次
名校
6 . 下列事实,不能用勒夏特列原理解释的是
| A.打开可乐瓶,有大量的气泡溢出 |
| B.实验室可用排饱和食盐水的方法收集Cl2 |
| C.乙酸乙酯在碱性下水解比酸性条件更充分 |
| D.工业制硫酸中,SO2与空气反应采用450℃、V2O5催化 |
您最近一年使用:0次
2023-09-17更新
|
61次组卷
|
2卷引用:浙江省海宁市高级中学2022-2023学年高二上学期10月月考化学试题
解题方法
7 . 下列关于物质制备说法不正确 的是
A.侯氏制碱法先制备 而非 而非 是为了尽可能提高原料的利用率 是为了尽可能提高原料的利用率 |
B.实验室通常用二氧化锰和浓盐酸制 |
| C.工业上用焦炭还原石英砂制备粗硅 |
D.实验室采用氯化铵受热分解法制 |
您最近一年使用:0次
22-23高二上·浙江·期中
解题方法
8 . 固体粉末X中可能含有Fe、FeO、CuO、MnO2、KCl和K2CO3中的若干种。为确定该固体粉末的成分,某同学依次进行了以下实验:
①将X加入足量水中,得到不溶物Y和溶液Z
②取少量Y加入足量浓盐酸,加热,产生黄绿色气体,并有少量红色不溶物
③向Z溶液中滴加AgNO3溶液,生成白色沉淀
④取少量Z溶液滴加紫色石蕊试液,试液呈蓝色
分析以上实验现象,下列结论正确的是
①将X加入足量水中,得到不溶物Y和溶液Z
②取少量Y加入足量浓盐酸,加热,产生黄绿色气体,并有少量红色不溶物
③向Z溶液中滴加AgNO3溶液,生成白色沉淀
④取少量Z溶液滴加紫色石蕊试液,试液呈蓝色
分析以上实验现象,下列结论正确的是
| A.X中一定不存在FeO |
| B.不溶物Y中一定含有Fe和CuO |
| C.Z溶液中一定含有KCl、K2CO3 |
| D.Y中不一定存在MnO2 |
您最近一年使用:0次
解题方法
9 . 能正确表示下列变化的离子方程式是
A.向NaClO溶液中通入少量CO2:2ClO-+CO2+H2O=2HClO+CO |
B.向Ba(OH)2溶液中加入稀硫酸: Ba2++OH– + H+ + SO =BaSO4↓+H2O =BaSO4↓+H2O |
C.MnO2和浓盐酸制取Cl2:MnO2+4HCl(浓)  Mn2++2Cl-+Cl2↑+2H2O Mn2++2Cl-+Cl2↑+2H2O |
| D.铜与氯化铁溶液反应:Cu+2Fe3+=2Fe2++Cu2+ |
您最近一年使用:0次
名校
10 . 利用Cl2氧化K2MnO4制备KMnO4的装置如下图所示(夹持装置略):

已知:锰酸钾(K2MnO4)在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:3MnO +2H2O = 2MnO
+2H2O = 2MnO +MnO2↓ +4OH−。下列说法不正确的是
+MnO2↓ +4OH−。下列说法不正确的是

已知:锰酸钾(K2MnO4)在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:3MnO
 +2H2O = 2MnO
+2H2O = 2MnO +MnO2↓ +4OH−。下列说法不正确的是
+MnO2↓ +4OH−。下列说法不正确的是| A.向仪器a中加入水,盖好玻璃塞,关闭止水夹,打开仪器a玻璃旋塞向烧瓶滴加水,若水一段时间不能滴下,则气密性良好 |
| B.装置A中发生反应的化学方程式为:Ca(ClO)2 + 4HCl = CaCl2+2Cl2↑+2H2O |
| C.若去掉装置B,可能会导致KMnO4产率降低 |
| D.装置D中的试剂用氢氧化钠溶液效果比用澄清石灰水好 |
您最近一年使用:0次