名校
1 . 二氧化氯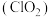 是一种新型的消毒杀剂,常用于饮用水的消毒,其消市效果优于传统的液氯消毒,除此之外,二氧化氯还具有漂白性,常用干纸浆和纸、纤维、小麦面粉、淀粉的漂白。常温常压下
是一种新型的消毒杀剂,常用于饮用水的消毒,其消市效果优于传统的液氯消毒,除此之外,二氧化氯还具有漂白性,常用干纸浆和纸、纤维、小麦面粉、淀粉的漂白。常温常压下 是一种带有辛辣气味的黄绿色气体,易溶于水和四氯化碳。工业上常用综合法制备
是一种带有辛辣气味的黄绿色气体,易溶于水和四氯化碳。工业上常用综合法制备 ,其工序包括制备氯酸钠,盐酸合成和
,其工序包括制备氯酸钠,盐酸合成和 制取,主要工艺流程如图所示。
制取,主要工艺流程如图所示。
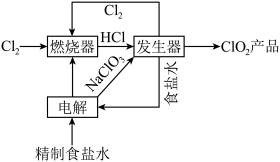
回答下列问题:
(1)工艺流程图涉及到的物质化学式或物质名称,其中能导电的是___________ ,属于电解质的是___________ 。
(2)实验室模拟“燃烧器”中发生的反应,观察到的现象有___________ 。
(3)“发生器”中发生反应的离子方程式为___________ ,若整个过程制得 ,则理论上分别向装置中补充
,则理论上分别向装置中补充___________ (填质量和物质名称)恢复至起始状态。
(4)粗盐中常常含有泥沙、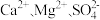 等杂质,粗盐提纯的步骤中加入稍过量的
等杂质,粗盐提纯的步骤中加入稍过量的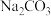 的目的是
的目的是___________ ,经一系列操作可得制食盐水,电解精制食盐水制得 同时还会获取轻质燃料氢气,则离子方程式为
同时还会获取轻质燃料氢气,则离子方程式为___________ 。
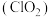 是一种新型的消毒杀剂,常用于饮用水的消毒,其消市效果优于传统的液氯消毒,除此之外,二氧化氯还具有漂白性,常用干纸浆和纸、纤维、小麦面粉、淀粉的漂白。常温常压下
是一种新型的消毒杀剂,常用于饮用水的消毒,其消市效果优于传统的液氯消毒,除此之外,二氧化氯还具有漂白性,常用干纸浆和纸、纤维、小麦面粉、淀粉的漂白。常温常压下 是一种带有辛辣气味的黄绿色气体,易溶于水和四氯化碳。工业上常用综合法制备
是一种带有辛辣气味的黄绿色气体,易溶于水和四氯化碳。工业上常用综合法制备 ,其工序包括制备氯酸钠,盐酸合成和
,其工序包括制备氯酸钠,盐酸合成和 制取,主要工艺流程如图所示。
制取,主要工艺流程如图所示。
回答下列问题:
(1)工艺流程图涉及到的物质化学式或物质名称,其中能导电的是
(2)实验室模拟“燃烧器”中发生的反应,观察到的现象有
(3)“发生器”中发生反应的离子方程式为
 ,则理论上分别向装置中补充
,则理论上分别向装置中补充(4)粗盐中常常含有泥沙、
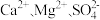 等杂质,粗盐提纯的步骤中加入稍过量的
等杂质,粗盐提纯的步骤中加入稍过量的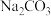 的目的是
的目的是 同时还会获取轻质燃料氢气,则离子方程式为
同时还会获取轻质燃料氢气,则离子方程式为
您最近一年使用:0次
2 . 常温下,一氧化二氯(C12O)为棕黄色气体,熔点为﹣116℃,浓度过高时易分解爆炸。为降低风险和便于贮存,制出C12O后,一般将其“固化”为固态。某小组按以下两阶段制备C12O。回答下列问题:
第一阶段:制备HgO。
配制15%的NaCl溶液和30%的HgC12溶液,将二者以一定质量比混合得到5%NaCl和20%HgC12的混合液;在室温下,边搅拌边缓慢地向混合液中加入过量NaOH溶液,生成黄色沉淀;将沉淀反复洗涤数次,直至没有氯离子;真空抽滤后将沉淀物在暗处干燥,得到干燥的HgO。
(1)配制15%NaCl溶液,除用到托盘天平和烧杯、玻璃棒外,还需要的玻璃仪器有___________ 。
(2)配制混合液时,15%NaCl溶液和30%HgC12溶液的质量比为___________ 。
(3)检验沉淀已经洗涤至没有氯离子的操作及现象为___________ 。
第二阶段:制备C12O。
制备干燥、纯净的C12;然后在干燥氮气的气流中,用C12和HgO在18~20℃条件下制备C12O;将产生的C12O气体“固化”;最后进行尾气处理。
(4)将干燥、纯净的C12通入下面装置中制备C12O并“固化”。

①制备C12O时还得到了HgC12·HgO固体,则装置I中制备反应的化学方程式为___________ 。干燥氮气的作用除将产生的C12O送入后续装置“固化”外,还有___________ 。
②常用冷却剂的数据如下表。“固化”时装置II中的冷却剂为___________ (填标号)。
A.液氯 B.液氨 C.干冰 D.液氧
第一阶段:制备HgO。
配制15%的NaCl溶液和30%的HgC12溶液,将二者以一定质量比混合得到5%NaCl和20%HgC12的混合液;在室温下,边搅拌边缓慢地向混合液中加入过量NaOH溶液,生成黄色沉淀;将沉淀反复洗涤数次,直至没有氯离子;真空抽滤后将沉淀物在暗处干燥,得到干燥的HgO。
(1)配制15%NaCl溶液,除用到托盘天平和烧杯、玻璃棒外,还需要的玻璃仪器有
(2)配制混合液时,15%NaCl溶液和30%HgC12溶液的质量比为
(3)检验沉淀已经洗涤至没有氯离子的操作及现象为
第二阶段:制备C12O。
制备干燥、纯净的C12;然后在干燥氮气的气流中,用C12和HgO在18~20℃条件下制备C12O;将产生的C12O气体“固化”;最后进行尾气处理。
(4)将干燥、纯净的C12通入下面装置中制备C12O并“固化”。

①制备C12O时还得到了HgC12·HgO固体,则装置I中制备反应的化学方程式为
②常用冷却剂的数据如下表。“固化”时装置II中的冷却剂为
| 物质 | O2 | CO2 | NH3 | Cl2 |
| 熔点/℃ | -218.4 | -78.5 | -77.3 | -101 |
| 沸点/℃ | -183 | 升华 | -33.35 | -34.6 |
您最近一年使用:0次
名校
3 . 三氯化碘 (ICl3)在药物合成中用途非常广泛,其熔点:33℃,沸点:73℃,遇水易反应。实验室可用下图装置(部分夹持装置已略去)制取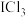 ,制备的反应原理:
,制备的反应原理: 。下列说法不正确的是
。下列说法不正确的是

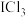 ,制备的反应原理:
,制备的反应原理: 。下列说法不正确的是
。下列说法不正确的是
| A.利用装置甲制备氯气可选用的药品为高锰酸钾和浓盐酸 |
| B.装置乙中长颈漏斗液面上升说明丙装置可能发生堵塞 |
C.装置丙中氯化钙的作用是干燥 |
D.装置丁中生成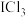 ,碘元素的化合价为-3价 ,碘元素的化合价为-3价 |
您最近一年使用:0次
2023-02-12更新
|
247次组卷
|
2卷引用:山东省滨州市北镇中学2022-2023学年高一上学期期末考试化学试题
名校
解题方法
4 . Ⅰ.二氯砜(SO2Cl2)是一种发烟液体,遇水剧烈水解,69.1℃时沸腾。某小组拟用干燥的Cl2和SO2在活性炭催化下制备二氯砜。反应的方程式为: ,实验装置如图所示(部分夹持装置略去):
,实验装置如图所示(部分夹持装置略去):

(1)装置A中发生反应的离子反应方程式为___________ 。
(2)仪器C的名称为___________ ,冷凝管的进水口为___________ (选填“a”或“b”)。
(3)分液漏斗中盛放的最佳试剂为___________ ,装置B、D的作用为___________ 。
(4)装置F的作用为___________ 。
Ⅱ.二氯亚砜(SO2Cl2)也是一种发烟液体,常用作脱水剂,遇水会形成白雾,并有刺激性气味的气体逸出。
(5)写出二氯亚砜与水反应的化学方程式___________ 。
(6)用硫磺、液氯和SO3为原料,在一定条件下合成二氯亚砜(SOCl2),原子利用率可达 ,则三者的物质的量之比为
,则三者的物质的量之比为___________ 。
 ,实验装置如图所示(部分夹持装置略去):
,实验装置如图所示(部分夹持装置略去):
(1)装置A中发生反应的离子反应方程式为
(2)仪器C的名称为
(3)分液漏斗中盛放的最佳试剂为
(4)装置F的作用为
Ⅱ.二氯亚砜(SO2Cl2)也是一种发烟液体,常用作脱水剂,遇水会形成白雾,并有刺激性气味的气体逸出。
(5)写出二氯亚砜与水反应的化学方程式
(6)用硫磺、液氯和SO3为原料,在一定条件下合成二氯亚砜(SOCl2),原子利用率可达
 ,则三者的物质的量之比为
,则三者的物质的量之比为
您最近一年使用:0次
2021-11-11更新
|
770次组卷
|
3卷引用:山东省济南市外国语学校2022届高三12月月考化学试题



