1 . 以 为原料制备
为原料制备 和
和 ,并利用
,并利用 冶炼金属钛(Ti)的工艺流程如下:
冶炼金属钛(Ti)的工艺流程如下:
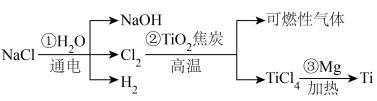
已知:高温条件下Ti的性质很活泼。
回答下列问题:
(1)在实际生产中,应避免步骤①的产物 与
与 接触发生副反应,降低
接触发生副反应,降低 纯度,解释其原因,用离子方程式表示为
纯度,解释其原因,用离子方程式表示为___________ 。
(2) 在
在 中燃烧的现象是
中燃烧的现象是___________ ,恰好完全反应后,将产物溶于水制得密度为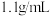 ,质量分数为
,质量分数为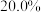 的盐酸溶液,其物质的量浓度为
的盐酸溶液,其物质的量浓度为___________ 。
(3)步骤②发生反应的化学方程式为___________ ,该反应中氧化产物与还原产物的物质的量之比为___________ 。
(4)步骤③须在稀有气体(如氩)的氛围下进行,稀有气体的作用是___________ 。
 为原料制备
为原料制备 和
和 ,并利用
,并利用 冶炼金属钛(Ti)的工艺流程如下:
冶炼金属钛(Ti)的工艺流程如下:
已知:高温条件下Ti的性质很活泼。
回答下列问题:
(1)在实际生产中,应避免步骤①的产物
 与
与 接触发生副反应,降低
接触发生副反应,降低 纯度,解释其原因,用离子方程式表示为
纯度,解释其原因,用离子方程式表示为(2)
 在
在 中燃烧的现象是
中燃烧的现象是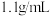 ,质量分数为
,质量分数为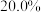 的盐酸溶液,其物质的量浓度为
的盐酸溶液,其物质的量浓度为(3)步骤②发生反应的化学方程式为
(4)步骤③须在稀有气体(如氩)的氛围下进行,稀有气体的作用是
您最近一年使用:0次
2 . 某化学兴趣小组利用NaI溶液中通入少量Cl2得到含碘废液,再利用含碘废液获取NaI固体,实验流程如图: +H2O=2CuI↓+SO
+H2O=2CuI↓+SO +2H+
+2H+
回答下列问题:
(1)过滤实验所需要的玻璃仪器有普通漏斗、烧杯、_______ 。
(2)反应③中CuI被氧化,还原产物只有NO2,当有95.5gCuI参与反应,产生的NO2在标况下的体积为_______ 。
(3)化合物B中含两种元素,铁元素原子与另一种元素原子的物质的量之比为3:8,则化合物B的化学式为_______ 。
(4)反应⑤中生成黑色固体磁性氧化铁和无色气体,则反应⑤的化学方程式为________ 。
(5)将足量的Cl2通入含12g NaI的溶液中,一段时间后把溶液蒸干、灼烧,得到的固体是______ ,其质量为_______ g。

 +H2O=2CuI↓+SO
+H2O=2CuI↓+SO +2H+
+2H+回答下列问题:
(1)过滤实验所需要的玻璃仪器有普通漏斗、烧杯、
(2)反应③中CuI被氧化,还原产物只有NO2,当有95.5gCuI参与反应,产生的NO2在标况下的体积为
(3)化合物B中含两种元素,铁元素原子与另一种元素原子的物质的量之比为3:8,则化合物B的化学式为
(4)反应⑤中生成黑色固体磁性氧化铁和无色气体,则反应⑤的化学方程式为
(5)将足量的Cl2通入含12g NaI的溶液中,一段时间后把溶液蒸干、灼烧,得到的固体是
您最近一年使用:0次
2021-04-29更新
|
381次组卷
|
3卷引用:山东省临沂市临沂第二十四中学2020-2021学年高一下学期期中考试化学试题
2021高三·浙江·专题练习
解题方法
3 . KIO3是一种重要的无机化合物,可作为食盐中的补碘剂。回答下列问题:
(1)KIO3的化学名称是___________________________________ 。
(2)利用“KClO3氧化法”制备KIO3工艺流程如下图所示:

“酸化反应”所得产物有KH(IO3)2、Cl2和KCl。“逐Cl2”采用的方法是_______________________________ 。“滤液”中的溶质主要是____________ 。“调pH”中发生反应的化学方程式为___________________________________ 。
(1)KIO3的化学名称是
(2)利用“KClO3氧化法”制备KIO3工艺流程如下图所示:

“酸化反应”所得产物有KH(IO3)2、Cl2和KCl。“逐Cl2”采用的方法是
您最近一年使用:0次
解题方法
4 . 五氯化磷(PCl5) 常温下是一种淡黄色固体,在潮湿空气中水解产生两种酸。PCl5在有机合成中被广泛用作氯化剂、催化剂、脱水剂等,高纯度PCl5主要用于医药中间体及锂电池原材料的合成。工业生产PCl5的传统方法是在搅拌式反应釜中注入液体三氯化磷(PCl3),再通入氯气在合适的温度下发生反应:PCl3+Cl2 PCl5。某工厂对传统方法进行了改进以生产高纯度PCl5,主要流程如下图所示(循环水的作用是控制温度)。
PCl5。某工厂对传统方法进行了改进以生产高纯度PCl5,主要流程如下图所示(循环水的作用是控制温度)。

请回答下列相关问题。
(1)工业生产氯气的主要方法的离子方程式是___________ ,利用该反应所得产品可继续生产_________ (任写一种)等化工产品。
(2)浓硫酸吸收罐和硫酸镁吸收塔的作用是______________________ ,若去掉这两个设备夹套反应釜中发生的主要副反应是______________________________ 。
(3)夹套反应釜中的原料混合方式与搅拌式反应釜相比主要优点是____________________________ 。 (4)NaOH水池的作用是_______________________ ,从降低生产成本的角度考虑NaOH 溶液可更换为______ 。
(5)生产过程中PCl3的加料速率会对生产造成明显的影响,具体情况如下表。根据表中数据判断最佳的加料速率范围是_________________ kg·h-1。
 PCl5。某工厂对传统方法进行了改进以生产高纯度PCl5,主要流程如下图所示(循环水的作用是控制温度)。
PCl5。某工厂对传统方法进行了改进以生产高纯度PCl5,主要流程如下图所示(循环水的作用是控制温度)。
请回答下列相关问题。
(1)工业生产氯气的主要方法的离子方程式是
(2)浓硫酸吸收罐和硫酸镁吸收塔的作用是
(3)夹套反应釜中的原料混合方式与搅拌式反应釜相比主要优点是
(5)生产过程中PCl3的加料速率会对生产造成明显的影响,具体情况如下表。根据表中数据判断最佳的加料速率范围是
| PCl3加料速率/kg·h-1 | PCl5状态 | 热交换情况 | 生产500kg产品的周期/h |
| 40 | 致密、坚硬、造粒困难 | 快、温度可控 | 11.5 |
| 50 | 致密、坚硬、造粒困难 | 快、温度可控 | 9.2 |
| 60 | 较松散、造粒容易 | 较快、温度可控 | 7.2 |
| 70 | 松散、造粒容易 | 较快、温度可控 | 6.5 |
| 80 | 松散、造粒容易 | 慢、温度升高难以控制 | 5.3 |
您最近一年使用:0次



