1 . 下图是化学实验室浓盐酸试剂标签上的部分内容。
(1)写出工业上制 的化学方程式
的化学方程式___________ ,在实验室中进行该反应,现象是___________ 。
(2)该盐酸的物质的量浓度为___________ 。
(3)同学计划用该浓盐酸配制 的稀盐酸,现实验需要稀盐酸
的稀盐酸,现实验需要稀盐酸 ,可供选用的仪器有:A.胶头滴管 B.烧瓶 C.烧杯 D.药匙 E.玻璃棒
,可供选用的仪器有:A.胶头滴管 B.烧瓶 C.烧杯 D.药匙 E.玻璃棒
①配制稀盐酸时,选择的仪器有:___________ (填序号),还缺少的仪器有___________ 。
②经计算,配制 的稀盐酸需要用量筒量取上述浓盐酸的体积为
的稀盐酸需要用量筒量取上述浓盐酸的体积为___________ mL。
③测定所配制的稀盐酸,发现其浓度大于 ,引起误差的原因可能是
,引起误差的原因可能是___________ 。
A.量取浓盐酸时俯视刻度线
B.将量取的浓盐酸倒入烧杯后,洗涤量筒,洗涤液也注入容量瓶
C.转移溶液后,未洗涤烧杯和玻璃棒
D.定容时俯视容量瓶刻度线
E.定容摇匀后发现液面低于容量瓶的刻度线,再加水至刻度线
| 盐酸 分子式:  相对分子质量:36.5 密度约   的质量分数:36.5% 的质量分数:36.5% |
 的化学方程式
的化学方程式(2)该盐酸的物质的量浓度为
(3)同学计划用该浓盐酸配制
 的稀盐酸,现实验需要稀盐酸
的稀盐酸,现实验需要稀盐酸 ,可供选用的仪器有:A.胶头滴管 B.烧瓶 C.烧杯 D.药匙 E.玻璃棒
,可供选用的仪器有:A.胶头滴管 B.烧瓶 C.烧杯 D.药匙 E.玻璃棒①配制稀盐酸时,选择的仪器有:
②经计算,配制
 的稀盐酸需要用量筒量取上述浓盐酸的体积为
的稀盐酸需要用量筒量取上述浓盐酸的体积为③测定所配制的稀盐酸,发现其浓度大于
 ,引起误差的原因可能是
,引起误差的原因可能是A.量取浓盐酸时俯视刻度线
B.将量取的浓盐酸倒入烧杯后,洗涤量筒,洗涤液也注入容量瓶
C.转移溶液后,未洗涤烧杯和玻璃棒
D.定容时俯视容量瓶刻度线
E.定容摇匀后发现液面低于容量瓶的刻度线,再加水至刻度线
您最近半年使用:0次
解题方法
2 . 氯气与氢气在点燃条件下反应的实验现象:____________ 。
您最近半年使用:0次
名校
3 . 工业氯气通过电解饱和食盐水制得
(1)图(1)中,铁棒作_______ 极,电极反应式是_______ 。
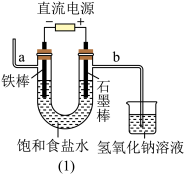
(2)检验导管b出来的气体可以用_______ ,反应的化学方程式是:_______ ;电解饱和食盐水的化学反应方程式为_______ 。
(3)图(1)方法制得的固体烧碱中可能混有少量NaCl,请写出检验是否混有NaCl的实验方法:_______ 。
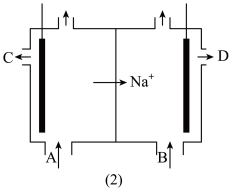
(4)下列关于图(2)的说法正确的是_______。
(5)工业上利用 与
与 反应制盐酸时使用过量的
反应制盐酸时使用过量的 ,理由是
,理由是_______ 。
A.氯气有毒 B.氯气可溶于水 C.氢气密度小
(1)图(1)中,铁棒作

(2)检验导管b出来的气体可以用
(3)图(1)方法制得的固体烧碱中可能混有少量NaCl,请写出检验是否混有NaCl的实验方法:
(4)下列关于图(2)的说法正确的是_______。

| A.A与C、B与D溶质相同 | B.A、B通入的均为浓溶液 |
| C.理论上NaCl利用率可达100% | D.图(2)是负离子交换膜法示意图 |
(5)工业上利用
 与
与 反应制盐酸时使用过量的
反应制盐酸时使用过量的 ,理由是
,理由是A.氯气有毒 B.氯气可溶于水 C.氢气密度小
您最近半年使用:0次
名校
解题方法
4 . 下表列出了①~⑨十种元素在周期表中的位置:
请按要求回答下列问题:
(1)①的名称是___________ ,②的原子结构示意图为___________ ,1molD2O含有的中子个数为___________ 。
(2)上述元素中,金属性最强的是___________ (填元素名称),最高价氧化物对应水化物酸性最强的是___________ (写出酸的化学式)。
(3)由④、⑤、⑦四种元素形成的简单离子半径由大到小的顺序是:___________ 。(用离子符号表示)
(4)④、⑧中非金属性更强的元素是___________ ,由元素①、③、④、⑧形成的一种个数比为5:1:4:1的化合物,该化合物的化学式为___________ ,该化合物与NaHCO3、KHSO3均可以归为___________ 盐。
(5)将⑨的单质滴入淀粉KI溶液中的现象为___________ ,离子方程式为______________ 。
(6)可以比较⑤、⑥两元素金属性强弱的实验是___________。
| 族周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
(1)①的名称是
(2)上述元素中,金属性最强的是
(3)由④、⑤、⑦四种元素形成的简单离子半径由大到小的顺序是:
(4)④、⑧中非金属性更强的元素是
(5)将⑨的单质滴入淀粉KI溶液中的现象为
(6)可以比较⑤、⑥两元素金属性强弱的实验是___________。
| A.比较这两种元素最高价氧化物对应的水化物的碱性 |
| B.将⑤的单质投入到⑥的盐溶液中 |
| C.将这两种元素的单质分别放入冷水中 |
| D.比较这两种元素的单质与酸反应时失电子的数目 |
您最近半年使用:0次
名校
5 . 标准状况下,将体积比为 的
的 、
、 、
、 在密闭容器中用电火花点燃充分反应,恢复到原状态后,形成溶液的质量分数为
在密闭容器中用电火花点燃充分反应,恢复到原状态后,形成溶液的质量分数为_______ (用小数表示,保留三位小数)。
 的
的 、
、 、
、 在密闭容器中用电火花点燃充分反应,恢复到原状态后,形成溶液的质量分数为
在密闭容器中用电火花点燃充分反应,恢复到原状态后,形成溶液的质量分数为
您最近半年使用:0次
名校
解题方法
6 . 氯气是氯碱工业的主要产品之一,是一种常用的消毒刹,其消毒原理是与水反应生成了次氯酸,次氯酸的强氧化性能杀死水中的病菌。但是,由于氯气贮运不方便,且具有一定的危险性,目前正逐渐被其他性能优越的消毒产品所替代。请回答:
(1)氯气与水反应的离子方程式为______________________________ 。
(2)将氯气通入淀粉 溶液中,溶液变蓝,写出反应的离子方程式
溶液中,溶液变蓝,写出反应的离子方程式____________________ ;继续通入氯气,蓝色消失,原因是: ,该反应体现了氯气的
,该反应体现了氯气的__________ 性。
(3)泳池用含氯物质消毒时,需要保证一定量的余氯,若水中的余氯以次氯酸形式存在,再加入 进行消毒反而会导致藻类生长,池水变绿。写出次氯酸与
进行消毒反而会导致藻类生长,池水变绿。写出次氯酸与 发生反应生成盐酸的化学方程式
发生反应生成盐酸的化学方程式____________________ 。
(4)84消毒液与氯气相比具有贮运方便等优点,用氯气与烧碱溶液反应制备84消毒液的离子方程式为_________________________ 。
(5)二氧化氯( )是国际上公认为安全、.无毒的绿色消毒剂。工业上制取
)是国际上公认为安全、.无毒的绿色消毒剂。工业上制取 的化学方程式如下:
的化学方程式如下: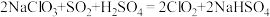 。按要求回答下列问题:
。按要求回答下列问题:
①该反应的离子方程式为____________________ 。
②另一种制备 的方法是用
的方法是用 与盐酸反应,同时有
与盐酸反应,同时有 生成,产物中
生成,产物中 与
与 的物质的量之比为
的物质的量之比为 ,则每生成
,则每生成 ,转移
,转移_________ 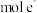 。
。
(1)氯气与水反应的离子方程式为
(2)将氯气通入淀粉
 溶液中,溶液变蓝,写出反应的离子方程式
溶液中,溶液变蓝,写出反应的离子方程式 ,该反应体现了氯气的
,该反应体现了氯气的(3)泳池用含氯物质消毒时,需要保证一定量的余氯,若水中的余氯以次氯酸形式存在,再加入
 进行消毒反而会导致藻类生长,池水变绿。写出次氯酸与
进行消毒反而会导致藻类生长,池水变绿。写出次氯酸与 发生反应生成盐酸的化学方程式
发生反应生成盐酸的化学方程式(4)84消毒液与氯气相比具有贮运方便等优点,用氯气与烧碱溶液反应制备84消毒液的离子方程式为
(5)二氧化氯(
 )是国际上公认为安全、.无毒的绿色消毒剂。工业上制取
)是国际上公认为安全、.无毒的绿色消毒剂。工业上制取 的化学方程式如下:
的化学方程式如下: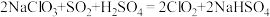 。按要求回答下列问题:
。按要求回答下列问题:①该反应的离子方程式为
②另一种制备
 的方法是用
的方法是用 与盐酸反应,同时有
与盐酸反应,同时有 生成,产物中
生成,产物中 与
与 的物质的量之比为
的物质的量之比为 ,则每生成
,则每生成 ,转移
,转移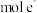 。
。
您最近半年使用:0次
名校
7 . 氯化钠是一种化工原料,可以制备多种物质,如下图所示。

请根据以上转化关系填写下列空白。
(1)氯化钠溶液通电后,发生反应的离子方程式是___________ 。氢气在氯气中燃烧的现象是___________ 。
(2)氯气与氢氧化钙反应的化学方程式是___________ 。从氧化剂和还原剂角度分析,该反应中氯气的作用是___________ 。
(3)检验某溶液中是否含有Cl-的方法是___________ 。

请根据以上转化关系填写下列空白。
(1)氯化钠溶液通电后,发生反应的离子方程式是
(2)氯气与氢氧化钙反应的化学方程式是
(3)检验某溶液中是否含有Cl-的方法是
您最近半年使用:0次
名校
8 . 如图为氯及其化合物的“价—类”二维图。
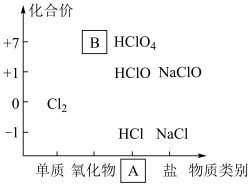
(1)缺失的类别 为
为___________ 、物质 为
为___________ (填化学式)。
(2) 在
在 中安静燃烧
中安静燃烧_______________________________ (化学方程式)。
(3) 溶于水
溶于水____________________________ (离子方程式)。
(4)工业制备漂白粉__________________________________ (化学方程式)。

(1)缺失的类别
 为
为 为
为(2)
 在
在 中安静燃烧
中安静燃烧(3)
 溶于水
溶于水(4)工业制备漂白粉
您最近半年使用:0次
名校
解题方法
9 . 自磷(P4)与氯气反应的能量变化如图所示。回答下列问题:
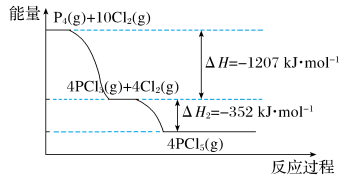
(1)白磷在氯气中燃烧的各度是放热反应,但是启动反应时需要点燃或加热,其原因是_____ 。
(2)PCl5(g)=PCl3(g)+Cl2(g) △H=_____ 88kJ/mol。
(3)写出白磷蒸气在氯气中反应生成五氯化磷气体的热化学方程式:_____ 。
(4)在密闭容器中充入1molPCl3(g)和3molCl2(g),发生反应:PCl3(g)+Cl2(g)=PCl5(g),放出热量Q的范围为_____ 。
(5)白磷在氯气中燃烧,开始引燃之后,停止加热,反应持续进行至一种物质(或两种物质)完全反应,其原因是_____ 。

(1)白磷在氯气中燃烧的各度是放热反应,但是启动反应时需要点燃或加热,其原因是
(2)PCl5(g)=PCl3(g)+Cl2(g) △H=
(3)写出白磷蒸气在氯气中反应生成五氯化磷气体的热化学方程式:
(4)在密闭容器中充入1molPCl3(g)和3molCl2(g),发生反应:PCl3(g)+Cl2(g)=PCl5(g),放出热量Q的范围为
(5)白磷在氯气中燃烧,开始引燃之后,停止加热,反应持续进行至一种物质(或两种物质)完全反应,其原因是
您最近半年使用:0次
名校
解题方法
10 . “化学——我们的生活,我们的未来”,学习化学应该明白“从生活中来,到生活中去”的道理。请填空:
(1)通过学习,我们掌握了胶体的知识,请完成下列问题:
①鉴别胶体和溶液的方法(只需写出方法名称,不用展开写)___________ ;
②请写出实验室制备氢氧化铁胶体的化学方程式为___________ 。
(2)写出下列物质在溶液中的电离方程式:Al2(SO4)3________ ,NaHCO3________ 。
(3)无色气体A在一种黄绿色气体B中可安静地燃烧,发出苍白色火焰,反应生成气体C,推断出各种物质后,回答下列问题:
①写出反应的化学方程式___________ 。
②1g物质A中含有的分子数约为___________ 。
(1)通过学习,我们掌握了胶体的知识,请完成下列问题:
①鉴别胶体和溶液的方法(只需写出方法名称,不用展开写)
②请写出实验室制备氢氧化铁胶体的化学方程式为
(2)写出下列物质在溶液中的电离方程式:Al2(SO4)3
(3)无色气体A在一种黄绿色气体B中可安静地燃烧,发出苍白色火焰,反应生成气体C,推断出各种物质后,回答下列问题:
①写出反应的化学方程式
②1g物质A中含有的分子数约为
您最近半年使用:0次



