解题方法
1 . 写出下列反应的化学方程式,标出电子转移的方向和数目,并指出氯气在反应中表现出什么性质。
(1)氢气在氯气中燃烧_______ 。
(2)氯气与氢氧化钠反应_______ 。
(3)铁在氯气中燃烧_______ 。
(1)氢气在氯气中燃烧
(2)氯气与氢氧化钠反应
(3)铁在氯气中燃烧
您最近一年使用:0次
名校
2 . NaCl用途广泛,是一种化工原料,可以制备多种物质,如图所示:
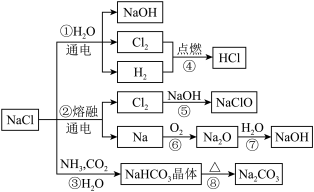
请回答下列问题:
(1)若工业上采用反应①制取NaOH,每生成1molNaOH转移的电子数目为____ 。
(2)反应④的实验现象为____ ;反应③的化学反应方程式为____ 。
(3)漂白粉的主要成分是Ca(ClO)2和CaCl2,有效成分为____ ,其久置失效的原理是____ 、___ (用化学反应方程式表示),故漂白粉须密封保存。
(4)某水产养殖场购买了某品牌的漂白粉,有效成分的质量分数约为25%。该养殖场工作人员从中取出200g漂白粉,溶解到1kg水中,用于池塘消毒,假设溶解后溶液密度为1g/cm3,则溶液中c[Ca(ClO)2]=____ mol/L(结果保留两位小数)。

请回答下列问题:
(1)若工业上采用反应①制取NaOH,每生成1molNaOH转移的电子数目为
(2)反应④的实验现象为
(3)漂白粉的主要成分是Ca(ClO)2和CaCl2,有效成分为
(4)某水产养殖场购买了某品牌的漂白粉,有效成分的质量分数约为25%。该养殖场工作人员从中取出200g漂白粉,溶解到1kg水中,用于池塘消毒,假设溶解后溶液密度为1g/cm3,则溶液中c[Ca(ClO)2]=
您最近一年使用:0次
解题方法
3 . NaCl是一种化工原料,可以制备多种物质,如下图所示。
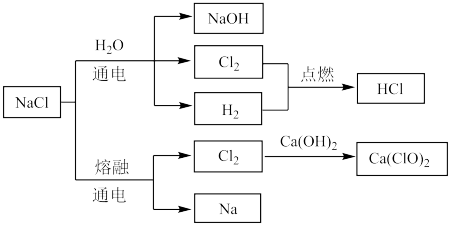
请根据以上转化关系填写下列空白。
(1)氯化钠溶液通电后,发生反应的离子方程式为_______ ;
(2)氢气在氯气中燃烧的现象是_______ 。
(3) 与
与 反应的化学方程式为
反应的化学方程式为_______ ;该反应常用于制备_______ ,从氧化剂和还原剂的角度分析,该反应中 的作用是
的作用是_______ 。

请根据以上转化关系填写下列空白。
(1)氯化钠溶液通电后,发生反应的离子方程式为
(2)氢气在氯气中燃烧的现象是
(3)
 与
与 反应的化学方程式为
反应的化学方程式为 的作用是
的作用是
您最近一年使用:0次
2022高一·上海·专题练习
解题方法
4 . 请回答下列问题:
(1)铁在氯气中燃烧,反应的化学方程式为_______ ,产生_______ 色的烟,向反应后的集气瓶中注入少量水,振荡后,溶液呈_______ 色。
(2)氢气在氯气中燃烧,火焰呈_______ 色,集气瓶口的现象为_______ 。向反应后的集气瓶中注入少量水,再滴入几滴紫色石蕊试液,溶液呈_______ 色。
(3)写出氯气和水反应的化学方程式_______ 。
(4)实验室里怎么处理尾气中的氯气(用化学方程式表示)_______ 。
(1)铁在氯气中燃烧,反应的化学方程式为
(2)氢气在氯气中燃烧,火焰呈
(3)写出氯气和水反应的化学方程式
(4)实验室里怎么处理尾气中的氯气(用化学方程式表示)
您最近一年使用:0次
2022高一·上海·专题练习
5 . 今有H2、Cl2 混合气体100毫升(标准状况下),其中一种气体体积为45毫升,另一种气体体积为55毫升,光照这两种气体发生反应后再恢复到标准状况,为证明反应后气体中H2或Cl2 有剩余,使气体通过10毫升水,并使剩余气体干燥后恢复到标准状况。若:
(1)剩余气体有_______ 毫升,证明有_______ 剩余。
(2)溶液有_______ 性,证明有_______ 剩余。
(1)剩余气体有
(2)溶液有
您最近一年使用:0次
2022高一·全国·专题练习
解题方法
6 . 实验过程中有哪些注意事项_________ ?
您最近一年使用:0次
7 . 完成下列问题
(1)①硫酸钡的化学式_______ ;
②乙醇的结构简式_______ 。
(2)氯化铁溶液腐蚀覆铜板的离子方程式为_______ 。
(3)如图所示,将纯净的氢气通入到氯气中燃烧,观察到的现象是:_______ 。
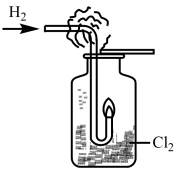
(1)①硫酸钡的化学式
②乙醇的结构简式
(2)氯化铁溶液腐蚀覆铜板的离子方程式为
(3)如图所示,将纯净的氢气通入到氯气中燃烧,观察到的现象是:

您最近一年使用:0次
名校
8 . 现有A、B、C三种气体,常温下,A是密度最小的气体,B是黄绿色单质气体,纯净的A可以在B中安静地燃烧,生成C。
(1)写出A在B中燃烧的化学方程式_______ 。
(2)把A、B、C三种气体分别通入硝酸酸化的硝酸银溶液中,出现白色沉淀的气体是_______ (用字母表示)。
(3)气体B通入NaOH溶液中,反应得到NaCl、NaClO和NaClO3的混合液,经测定Cl-与 的个数比为11:2,则所得溶液中ClO-与
的个数比为11:2,则所得溶液中ClO-与 的个数比为
的个数比为_______ 。
(4)金属Fe在B中燃烧的产物溶于水可以得到棕黄色溶液,某同学想利用该溶液来制备Fe(OH)3胶体:
①制备该胶体的离子方程式:_______ ;判断胶体制备成功的方法是_______ 。
②向制得的Fe(OH)3胶体中逐滴滴加稀盐酸,开始产生红褐色沉淀,这是因为_______ ,继续滴加,沉淀减少最终消失,写出离子反应方程式_______ 。
(1)写出A在B中燃烧的化学方程式
(2)把A、B、C三种气体分别通入硝酸酸化的硝酸银溶液中,出现白色沉淀的气体是
(3)气体B通入NaOH溶液中,反应得到NaCl、NaClO和NaClO3的混合液,经测定Cl-与
 的个数比为11:2,则所得溶液中ClO-与
的个数比为11:2,则所得溶液中ClO-与 的个数比为
的个数比为(4)金属Fe在B中燃烧的产物溶于水可以得到棕黄色溶液,某同学想利用该溶液来制备Fe(OH)3胶体:
①制备该胶体的离子方程式:
②向制得的Fe(OH)3胶体中逐滴滴加稀盐酸,开始产生红褐色沉淀,这是因为
您最近一年使用:0次
21-22高一上·全国·课前预习
9 . 氯气的化学性质
(1)氯气是很活泼的非金属单质,具有强___________ 性。
(2)与金属单质的反应
2Na+Cl2 2NaCl,产生
2NaCl,产生___________ 。
2Fe+3Cl2
___________ ,产生___________ ,加水溶解所得溶液呈___________ 色(Fe3+的颜色)。
Cu+Cl2 CuCl2,产生
CuCl2,产生___________ ,加水溶解所得溶液呈___________ 。
(3)与非金属单质的反应
[实验探究]H2在Cl2中燃烧
(4)与水的反应
①Cl2溶于水,Cl2的水溶液称为。在常温下,溶于水的氯气部分与水反应生成了盐酸和次氯酸,反应的化学方程式为___________ ,离子方程式为___________ 。
从化合价的角度看,该反应中氯元素的化合价既有升高又有降低,故Cl2既是氧化剂又是还原剂。
②氯水的性质
[注意]干燥的氯气不具有漂白性,潮湿的氯气才具有漂白性,实际上起作用的是Cl2与水反应生成的HClO。
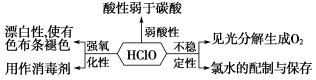
③次氯酸的性质
(5)与碱的反应
①化学方程式:Cl2+2NaOH=_________+H2O,_________ ,离子方程式:_________
漂白液的有效成分是_________ 。
②制取漂白粉
2Cl2+2Ca(OH)2=_________+2H2O_________
漂白粉的有效成分是_________ ,其主要成分是CaCl2和Ca(ClO)2。
Cl2与Ca(OH)2反应充分,并使_________ 成为主要成分,则得到漂粉精。
[注意]氯气所发生的反应均为氧化还原反应,反应中氯气通常为氧化剂,但Cl2与碱反应时,Cl2既是氧化剂又是还原剂。
(1)氯气是很活泼的非金属单质,具有强
(2)与金属单质的反应
2Na+Cl2
 2NaCl,产生
2NaCl,产生2Fe+3Cl2

Cu+Cl2
 CuCl2,产生
CuCl2,产生(3)与非金属单质的反应
[实验探究]H2在Cl2中燃烧
| 实验操作 | 实验现象 | 实验结论 |
| 在空气中点燃H2后,把导管缓慢伸入盛满氯气的集气瓶中 | 氢气在氯气中安静地燃烧,发出 | H2+Cl2 2HCl,反应生成的HCl极易溶于水,溶于水得到的溶液即为 2HCl,反应生成的HCl极易溶于水,溶于水得到的溶液即为 |
①Cl2溶于水,Cl2的水溶液称为。在常温下,溶于水的氯气部分与水反应生成了盐酸和次氯酸,反应的化学方程式为
从化合价的角度看,该反应中氯元素的化合价既有升高又有降低,故Cl2既是氧化剂又是还原剂。
②氯水的性质
| 实验操作 | 实验现象 | 结论 |
 | 有色布条 | 干燥的Cl2 |
 | 有色布条 | 氯水有漂白作用,起漂白作用的是HClO |
③次氯酸的性质

(5)与碱的反应
①化学方程式:Cl2+2NaOH=_________+H2O,
漂白液的有效成分是
②制取漂白粉
2Cl2+2Ca(OH)2=_________+2H2O
漂白粉的有效成分是
Cl2与Ca(OH)2反应充分,并使
[注意]氯气所发生的反应均为氧化还原反应,反应中氯气通常为氧化剂,但Cl2与碱反应时,Cl2既是氧化剂又是还原剂。
您最近一年使用:0次
名校
解题方法
10 . NaCl是一种化工原料,可以制备多种物质,如图所示。
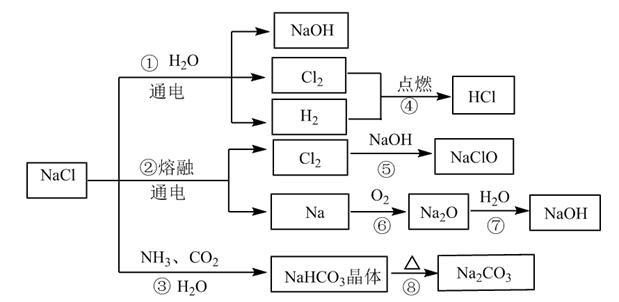
请回答下列问题:
(1)图所列物质中属于电解质的有___________ 种,转化反应中属于氧化还原反应的有___________ (填图中序号)
(2)工业上制取NaOH主要采用反应①,而不采用反应⑦的方法,主要原因是___________ 。
(3)反应④的现象是___________ ;反应⑤的化学方程式为___________ 。
(4)NaClO是“84消毒液”的有效成分,在抗击新冠肺炎疫情中发挥了重要作用。某同学购买了一瓶某品牌的“84消毒液”,查看相关资料及包装说明可获得以下信息:原液净含量为600g、密度约为1.1g/cm3、有效成分NaClO的质量分数约为1.9%(通过有效氯含量折算而得)。该同学从中取出100mL原液,按包装说明稀释30倍(体积之比)后用于家庭一般物体表面消毒,稀释后的溶液中c(NaClO)=___________ mol/L(结果保留两位小数);“84消毒液”不能与“洁厕灵(主要成分是HCl)”混合使用,否则会产生黄绿色的有毒气体引起安全事故,其反应的离子方程式是___________ 。

请回答下列问题:
(1)图所列物质中属于电解质的有
(2)工业上制取NaOH主要采用反应①,而不采用反应⑦的方法,主要原因是
(3)反应④的现象是
(4)NaClO是“84消毒液”的有效成分,在抗击新冠肺炎疫情中发挥了重要作用。某同学购买了一瓶某品牌的“84消毒液”,查看相关资料及包装说明可获得以下信息:原液净含量为600g、密度约为1.1g/cm3、有效成分NaClO的质量分数约为1.9%(通过有效氯含量折算而得)。该同学从中取出100mL原液,按包装说明稀释30倍(体积之比)后用于家庭一般物体表面消毒,稀释后的溶液中c(NaClO)=
您最近一年使用:0次
2021-11-13更新
|
356次组卷
|
2卷引用:辽宁省实验中学2021-2022学年高一上学期11月期中阶段测试化学试题



