解题方法
1 . 化学符号、化学概念是学习化学的必备知识。请按要求回答下列问题:
(1)以下为中学化学中常见的几种物质:①二氧化碳②熔融KCl③NaHSO4固体④铜⑤稀硫酸⑥蔗糖。其中属于电解质的有_______ (填序号,下同),属于非电解质的有_______ 。
(2)工业上利用电解饱和食盐水生产氯气(Cl2)、烧碱和氢气的化学方程式是: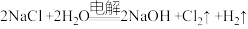 。
。
①将上述反应改写成离子方程式:_______ 。
②电解食盐水的过程中,被氧化的元素是_______ ,被还原的元素是_______ ,每生成1个Cl2分子,电路中转移_______ 个电子。
③将电解饱和食盐水的产品进一步反应可制得“洁厕灵”和“84”消毒液,写出制备“洁厕灵”的反应方程式:_______ 。
(1)以下为中学化学中常见的几种物质:①二氧化碳②熔融KCl③NaHSO4固体④铜⑤稀硫酸⑥蔗糖。其中属于电解质的有
(2)工业上利用电解饱和食盐水生产氯气(Cl2)、烧碱和氢气的化学方程式是:
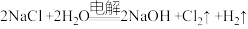 。
。①将上述反应改写成离子方程式:
②电解食盐水的过程中,被氧化的元素是
③将电解饱和食盐水的产品进一步反应可制得“洁厕灵”和“84”消毒液,写出制备“洁厕灵”的反应方程式:
您最近一年使用:0次
2 . 回答下列问题
(1)工业上以氯气和石灰乳为帮料制造漂白粉,相关化学方程式:_______ ,漂白粉的有效成分是_______ (填化学式)。
(2)帕拉米韦注射液是我国自主研发的一种新型的抗流感病毒药物,属于神经氨酸酶抑制剂,对抑制H7N9禽流感有一定的效果,其化学式为C15H28N4O4,它属于_______ (填“无机物”或“有机物”)。
(3)Cl2是一种重要化工原料,工业上采用H2和Cl2反应制取盐酸,请写出该反应的化学方程式_______ 。
(4)NaHCO3是制作糕点的常用疏松剂,写出NaHCO3受热分解的化学方程式_______ 。
(5)工业上在一定条件下可制取金属钠,写出该反应的化学方程式:_______ 。
(1)工业上以氯气和石灰乳为帮料制造漂白粉,相关化学方程式:
(2)帕拉米韦注射液是我国自主研发的一种新型的抗流感病毒药物,属于神经氨酸酶抑制剂,对抑制H7N9禽流感有一定的效果,其化学式为C15H28N4O4,它属于
(3)Cl2是一种重要化工原料,工业上采用H2和Cl2反应制取盐酸,请写出该反应的化学方程式
(4)NaHCO3是制作糕点的常用疏松剂,写出NaHCO3受热分解的化学方程式
(5)工业上在一定条件下可制取金属钠,写出该反应的化学方程式:
您最近一年使用:0次
名校
解题方法
3 . 人类的生活离不开化工产品。化工产品的生产涉及反应原理、物料选择、能源消耗、工艺流程、环境保护等许多问题。请完成下列各题:
(1)下列符合实际并用于工业生产的是_______。
(2)有关工业制硫酸的下列说法中,正确的是_______。(多选)
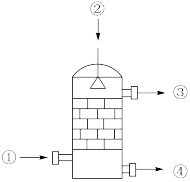
(3)在硫酸工业生产中,SO3的吸收过程是在吸收塔(如图)中进行,吸收塔里还装入了大量瓷杯。下列有关说法错误的是_______。
(1)下列符合实际并用于工业生产的是_______。
| A.NaOH与盐酸中和反应制NaCl | B.H2和Cl2光照制HCl |
| C.Cl2通入澄清石灰水中制漂白粉 | D.用硫磺制硫酸 |
| A.二氧化硫的催化氧化在转化器中发生 |
| B.吸收塔用浓度为98.3%浓硫酸吸收三氧化硫 |
| C.转化器中装有催化剂 |
| D.以硫磺为原料制硫酸使用的设备之一是沸腾炉 |

| A.从①处通入的气体中含大量SO3,整个吸收操作采取逆流的形式 |
| B.从②处喷下98.3%的硫酸,瓷环的作用是增大接触面积 |
| C.从③处导出的气体只含有少量SO2,可直接排入大气 |
| D.从④处流出的是可用水或稀硫酸稀释的硫酸 |
您最近一年使用:0次
名校
4 . 下图是化学实验室浓盐酸试剂标签上的部分内容。

(1)写出工业上制HCl的化学方程式_______ ,在实验室中进行该反应,现象是_______
(2)该盐酸的物质的量浓度为_______ ,
(3)同学计划用该浓盐酸配制 的稀盐酸,现实验需要稀盐酸470 mL,可供选用的仪器有:
的稀盐酸,现实验需要稀盐酸470 mL,可供选用的仪器有:
A.胶头滴管;B.烧瓶;C.烧杯;D.药匙;E玻璃棒。
①配制稀盐酸时,选择的仪器有:_______ (填序号),还缺少的仪器有_______ 。
②经计算,配制 的稀盐酸需要用量筒量取上述浓盐酸的体积为
的稀盐酸需要用量筒量取上述浓盐酸的体积为_______ mL。
③测定所配制的稀盐酸,发现其浓度大于 ,引起误差的原因可能是
,引起误差的原因可能是_______ 。
A.量取浓盐酸时俯视刻度线
B.将量取的浓盐酸倒入烧杯后,洗涤量筒,洗涤液也注入容量瓶
C.转移溶液后,未洗涤烧杯和玻璃棒
D.定容时俯视容量瓶刻度线
E.定容摇匀后发现液面低于容量瓶的刻度线,再加水至刻度线
(4)现有该浓盐酸100g,需要加入一定量的水将其物质的量浓度稀释为原来的1/2,则加入水的体积是_______ 。
A.大于100 mL B.小于100 mL C.等于100 mL

(1)写出工业上制HCl的化学方程式
(2)该盐酸的物质的量浓度为
(3)同学计划用该浓盐酸配制
 的稀盐酸,现实验需要稀盐酸470 mL,可供选用的仪器有:
的稀盐酸,现实验需要稀盐酸470 mL,可供选用的仪器有:A.胶头滴管;B.烧瓶;C.烧杯;D.药匙;E玻璃棒。
①配制稀盐酸时,选择的仪器有:
②经计算,配制
 的稀盐酸需要用量筒量取上述浓盐酸的体积为
的稀盐酸需要用量筒量取上述浓盐酸的体积为③测定所配制的稀盐酸,发现其浓度大于
 ,引起误差的原因可能是
,引起误差的原因可能是A.量取浓盐酸时俯视刻度线
B.将量取的浓盐酸倒入烧杯后,洗涤量筒,洗涤液也注入容量瓶
C.转移溶液后,未洗涤烧杯和玻璃棒
D.定容时俯视容量瓶刻度线
E.定容摇匀后发现液面低于容量瓶的刻度线,再加水至刻度线
(4)现有该浓盐酸100g,需要加入一定量的水将其物质的量浓度稀释为原来的1/2,则加入水的体积是
A.大于100 mL B.小于100 mL C.等于100 mL
您最近一年使用:0次
2022-12-07更新
|
464次组卷
|
5卷引用:四川省成都市第七中学2022-2023学年高一上学期12月月考化学试题
名校
5 . NaCl用途广泛,是一种化工原料,可以制备多种物质,如图所示:
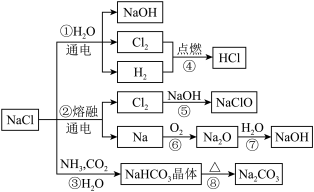
请回答下列问题:
(1)若工业上采用反应①制取NaOH,每生成1molNaOH转移的电子数目为____ 。
(2)反应④的实验现象为____ ;反应③的化学反应方程式为____ 。
(3)漂白粉的主要成分是Ca(ClO)2和CaCl2,有效成分为____ ,其久置失效的原理是____ 、___ (用化学反应方程式表示),故漂白粉须密封保存。
(4)某水产养殖场购买了某品牌的漂白粉,有效成分的质量分数约为25%。该养殖场工作人员从中取出200g漂白粉,溶解到1kg水中,用于池塘消毒,假设溶解后溶液密度为1g/cm3,则溶液中c[Ca(ClO)2]=____ mol/L(结果保留两位小数)。

请回答下列问题:
(1)若工业上采用反应①制取NaOH,每生成1molNaOH转移的电子数目为
(2)反应④的实验现象为
(3)漂白粉的主要成分是Ca(ClO)2和CaCl2,有效成分为
(4)某水产养殖场购买了某品牌的漂白粉,有效成分的质量分数约为25%。该养殖场工作人员从中取出200g漂白粉,溶解到1kg水中,用于池塘消毒,假设溶解后溶液密度为1g/cm3,则溶液中c[Ca(ClO)2]=
您最近一年使用:0次
解题方法
6 . NaCl是一种化工原料,可以制备多种物质,如下图所示。
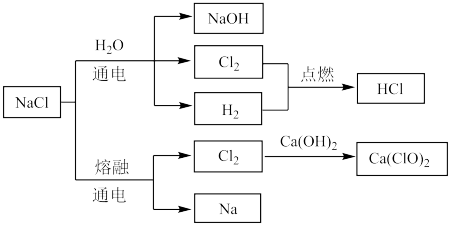
请根据以上转化关系填写下列空白。
(1)氯化钠溶液通电后,发生反应的离子方程式为_______ ;
(2)氢气在氯气中燃烧的现象是_______ 。
(3) 与
与 反应的化学方程式为
反应的化学方程式为_______ ;该反应常用于制备_______ ,从氧化剂和还原剂的角度分析,该反应中 的作用是
的作用是_______ 。

请根据以上转化关系填写下列空白。
(1)氯化钠溶液通电后,发生反应的离子方程式为
(2)氢气在氯气中燃烧的现象是
(3)
 与
与 反应的化学方程式为
反应的化学方程式为 的作用是
的作用是
您最近一年使用:0次
2022高一·上海·专题练习
解题方法
7 . 请回答下列问题:
(1)铁在氯气中燃烧,反应的化学方程式为_______ ,产生_______ 色的烟,向反应后的集气瓶中注入少量水,振荡后,溶液呈_______ 色。
(2)氢气在氯气中燃烧,火焰呈_______ 色,集气瓶口的现象为_______ 。向反应后的集气瓶中注入少量水,再滴入几滴紫色石蕊试液,溶液呈_______ 色。
(3)写出氯气和水反应的化学方程式_______ 。
(4)实验室里怎么处理尾气中的氯气(用化学方程式表示)_______ 。
(1)铁在氯气中燃烧,反应的化学方程式为
(2)氢气在氯气中燃烧,火焰呈
(3)写出氯气和水反应的化学方程式
(4)实验室里怎么处理尾气中的氯气(用化学方程式表示)
您最近一年使用:0次
2022高一·上海·专题练习
8 . 今有H2、Cl2 混合气体100毫升(标准状况下),其中一种气体体积为45毫升,另一种气体体积为55毫升,光照这两种气体发生反应后再恢复到标准状况,为证明反应后气体中H2或Cl2 有剩余,使气体通过10毫升水,并使剩余气体干燥后恢复到标准状况。若:
(1)剩余气体有_______ 毫升,证明有_______ 剩余。
(2)溶液有_______ 性,证明有_______ 剩余。
(1)剩余气体有
(2)溶液有
您最近一年使用:0次
2022高一·全国·专题练习
解题方法
9 . 实验过程中有哪些注意事项_________ ?
您最近一年使用:0次
10 . 完成下列问题
(1)①硫酸钡的化学式_______ ;
②乙醇的结构简式_______ 。
(2)氯化铁溶液腐蚀覆铜板的离子方程式为_______ 。
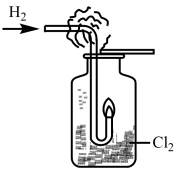
(3)如图所示,将纯净的氢气通入到氯气中燃烧,观察到的现象是:_______ 。
(1)①硫酸钡的化学式
②乙醇的结构简式
(2)氯化铁溶液腐蚀覆铜板的离子方程式为
(3)如图所示,将纯净的氢气通入到氯气中燃烧,观察到的现象是:

您最近一年使用:0次



