名校
解题方法
1 . 利用“价类二维图”研究物质的性质是化学研究的重要手段。如图是氯元素的化合价与部分物质类别的对应关系。
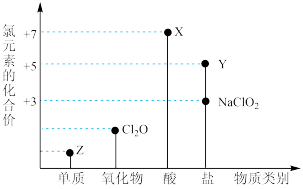
回答下列问题:
(1)X的电离方程式为_________ 。
(2)氯的某种氧化物(ClmOn)中氯、氧元素质量比为71:48,则m:n=_________ 。
(3) NaClO有较强的氧化性,所以是常用的消毒剂和漂白剂,请写出工业上用氯气和NaOH溶液生产消毒剂NaClO的离子方程式_____________ 。
(4)NaClO2具有很强的氧化性,常用作消毒剂,其消毒效率是Z的___________ 倍(还原产物都为Cl-,消毒效率以单位物质的量得到的电子数表示)。
(5)Cl2O可用潮湿的Z与Na2CO3反应制取,同时生成NaHCO3,反应中Z既体现氧化性,又体现还原性,该反应的化学方程式为_____________ 。
(6)自来水中的 对人类健康产生危害。为了降低自来水中
对人类健康产生危害。为了降低自来水中 的浓度,某研究人员提出在碱性条件下用Al粉还原
的浓度,某研究人员提出在碱性条件下用Al粉还原 ,产物是N2。发生的反应可表示如下,请完成方程式的配平:
,产物是N2。发生的反应可表示如下,请完成方程式的配平:___ Al+ ____  +
+ _____ =___  +
+ _____ N2↑ + _______ H2O

回答下列问题:
(1)X的电离方程式为
(2)氯的某种氧化物(ClmOn)中氯、氧元素质量比为71:48,则m:n=
(3) NaClO有较强的氧化性,所以是常用的消毒剂和漂白剂,请写出工业上用氯气和NaOH溶液生产消毒剂NaClO的离子方程式
(4)NaClO2具有很强的氧化性,常用作消毒剂,其消毒效率是Z的
(5)Cl2O可用潮湿的Z与Na2CO3反应制取,同时生成NaHCO3,反应中Z既体现氧化性,又体现还原性,该反应的化学方程式为
(6)自来水中的
 对人类健康产生危害。为了降低自来水中
对人类健康产生危害。为了降低自来水中 的浓度,某研究人员提出在碱性条件下用Al粉还原
的浓度,某研究人员提出在碱性条件下用Al粉还原 ,产物是N2。发生的反应可表示如下,请完成方程式的配平:
,产物是N2。发生的反应可表示如下,请完成方程式的配平: +
+  +
+
您最近一年使用:0次
2020-06-15更新
|
101次组卷
|
2卷引用:江西省南昌市八一中学2019-2020学年高一下学期期中考试化学试题
2 . 高铁酸盐在能源、环保等方面有着广泛的用途,在生产和生活中有广泛的应用。
已知:i.高铁酸钠(Na2FeO4)极易溶解于水,20℃溶解度为111克;高铁酸钾(K2FeO4)为暗紫色固体,可溶于水。
ii.高铁酸钾(K2FeO4)在中性或酸性溶液中逐渐分解,在碱性溶液中稳定。
iii.高铁酸根在水溶液中存在平衡: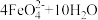 ⇌
⇌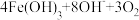 ↑
↑
(1)工业上用氯气和烧碱溶液可以制取次氯酸钠,反应的离子方程式为___________ 。
(2)高铁酸钾是一种理想的水处理剂,既可以对水杀菌消毒,又可以净化水,其原理为________ 。
(3)工业上有多种方法制备高铁酸钾。
方法1:次氯酸盐氧化法。工艺流程如图所示。
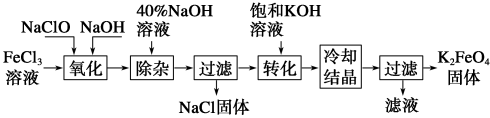
①“氧化”过程中的氧化剂为(填化学式)______________ 。
②写出“转化”过程中的化学方程式为__________________ 。
③上述工艺得到的高铁酸钾常含有杂质,可用重结晶法提纯,操作是将粗产品先用稀KOH溶液溶解,然后再加入饱和KOH溶液,冷却结晶过滤。上述操作中溶解粗产品用稀KOH溶液,不用蒸馏水,根据平衡移动原理解释__________ 。
(4)方法2:电解法
我国化学工作者还提出用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸盐Na2FeO4的方案,装置如下图所示。
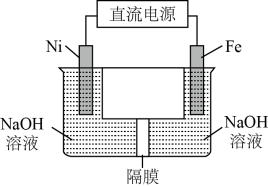
①Ni电极作________ (填“阴”或“阳”)极;
②Fe电极的电极反应式:____________ 。
已知:i.高铁酸钠(Na2FeO4)极易溶解于水,20℃溶解度为111克;高铁酸钾(K2FeO4)为暗紫色固体,可溶于水。
ii.高铁酸钾(K2FeO4)在中性或酸性溶液中逐渐分解,在碱性溶液中稳定。
iii.高铁酸根在水溶液中存在平衡:
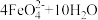 ⇌
⇌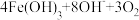 ↑
↑(1)工业上用氯气和烧碱溶液可以制取次氯酸钠,反应的离子方程式为
(2)高铁酸钾是一种理想的水处理剂,既可以对水杀菌消毒,又可以净化水,其原理为
(3)工业上有多种方法制备高铁酸钾。
方法1:次氯酸盐氧化法。工艺流程如图所示。

①“氧化”过程中的氧化剂为(填化学式)
②写出“转化”过程中的化学方程式为
③上述工艺得到的高铁酸钾常含有杂质,可用重结晶法提纯,操作是将粗产品先用稀KOH溶液溶解,然后再加入饱和KOH溶液,冷却结晶过滤。上述操作中溶解粗产品用稀KOH溶液,不用蒸馏水,根据平衡移动原理解释
(4)方法2:电解法
我国化学工作者还提出用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸盐Na2FeO4的方案,装置如下图所示。

①Ni电极作
②Fe电极的电极反应式:
您最近一年使用:0次
2020-07-05更新
|
156次组卷
|
2卷引用:北京市顺义区2019—2020学年高二下学期期末质量检测化学试题



