1 . 设 表示阿伏加德罗常数的值。下列叙述正确的是
表示阿伏加德罗常数的值。下列叙述正确的是
 表示阿伏加德罗常数的值。下列叙述正确的是
表示阿伏加德罗常数的值。下列叙述正确的是A.常温常压下,铁与稀硫酸反应生成 时,转移的电子数约为2 时,转移的电子数约为2 |
B. 与 与 充分反应生成 充分反应生成 的分子数为2 的分子数为2 |
C.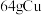 与足量硫粉反应转移的电子数目为2 与足量硫粉反应转移的电子数目为2 |
D.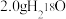 与 与 的混合物中所含电子数为 的混合物中所含电子数为 |
您最近一年使用:0次
名校
2 . 下列各组化合物中,均能由单质直接化合而得到的是
A. 、CuS、 、CuS、 、FeS 、FeS | B. 、 、 、 、 、 、 |
C. 、 、 、NO、 、NO、 | D. 、FeS、 、FeS、 、 、 |
您最近一年使用:0次
2022-04-13更新
|
151次组卷
|
3卷引用:江西省宁冈中学2022-2023学年高三上学期12月月考化学试题
19-20高一·浙江绍兴·期末
名校
解题方法
3 . 某学习小组设计实验制备氮化锂(Li3N)并测定其纯度,装置如下所示:
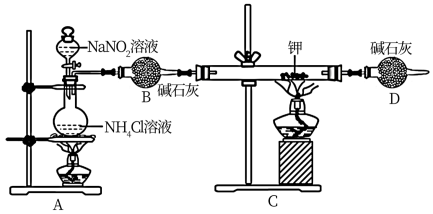
已知:i.Li3N遇水剧烈反应。
ii.实验室用NH4Cl溶液和NaNO2溶液共热制备N2。
请回答:
(1)写出制备N2的化学方程式_______ 。
(2)仪器B的名称为_______ ;D装置的作用是_______ 。
(3)实验室将金属钠和理均可保仔在_______ 中(填相应的编号)。
a.乙醇(CH3CH2OH) b.煤油c.石蜡油d.苯
(4)测定Li3N产品纯度:取m gLi3N产品按下图所示装置进行实验。
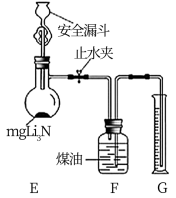
打开止水夹,向安全漏斗中加入足量水,当Li3N完全反应后,调平F和G中液面,测得气体体积为V L(已折合成标准状况下)。
①安全漏斗中“安全”含义是_______ 。
②Li3N与水反应的化学方程式_______ 。
③读数前调平F和G中液面的目的是_______ 。
④该Li3N产品的纯度为_______ %(只列出含m和V的计算式,不必计算化简)。
⑤若Li3N产品混有Li,则测得纯度_______ (选填“偏高”、“偏低”或“无影响")。(已知Li3N的相对分子质量为35)

已知:i.Li3N遇水剧烈反应。
ii.实验室用NH4Cl溶液和NaNO2溶液共热制备N2。
请回答:
(1)写出制备N2的化学方程式
(2)仪器B的名称为
(3)实验室将金属钠和理均可保仔在
a.乙醇(CH3CH2OH) b.煤油c.石蜡油d.苯
(4)测定Li3N产品纯度:取m gLi3N产品按下图所示装置进行实验。

打开止水夹,向安全漏斗中加入足量水,当Li3N完全反应后,调平F和G中液面,测得气体体积为V L(已折合成标准状况下)。
①安全漏斗中“安全”含义是
②Li3N与水反应的化学方程式
③读数前调平F和G中液面的目的是
④该Li3N产品的纯度为
⑤若Li3N产品混有Li,则测得纯度
您最近一年使用:0次
名校
解题方法
4 . 氮化钙(Ca3N2)时一种重要的化学试剂,通常条件下为棕色易水解的固体。某小组在实验室制备氮化钙并测定其纯度,设计如下实验
Ⅰ.氮化钙的制备。
(1)加热条件下,钙和氮气制备氮化钙的反应方程式为______ 。
(2)钙和氮气制备氮化钙的装置如下(夹持装置略去):

上述装置合理的连接顺序为______ (按气流方向,用接口字母表示,装置不重复使用)。
(3)按连接好的装置进行实验。
①实验步骤如下:检查装置气密性、加入药品:______ (请按正确顺序填入下列步骤的字母标号)。
a.点燃装置C处酒精灯,反应一段时间
b.打开分液漏斗活塞
c.点燃装置A处酒精灯
d.熄灭装置A处酒精灯
e.熄灭装置C处酒精灯
f.关闭分液漏斗活塞
②装置B的作用为______ 。
③装置C的硬质玻璃管中的现象为______
(4)设计实验证明Ca3N2中混有钙单质:______
Ⅱ.测定氮化钙纯度
ⅰ称取4.0g反应后的固体,加入足量水,将生成的气体全部蒸出并通入100.00mL 1.00mol/L的盐酸中,充分反应后,将所得溶液稀释到200.00mL;
ii.取20.00mL稀释后的溶液,用0.2mol/LNaOH标准溶液滴定过量的盐酸,到终点时消耗标准溶液25.00mL。
(5)所取固体中氮化钙的质量分数为______ 。
Ⅰ.氮化钙的制备。
(1)加热条件下,钙和氮气制备氮化钙的反应方程式为
(2)钙和氮气制备氮化钙的装置如下(夹持装置略去):

上述装置合理的连接顺序为
(3)按连接好的装置进行实验。
①实验步骤如下:检查装置气密性、加入药品:
a.点燃装置C处酒精灯,反应一段时间
b.打开分液漏斗活塞
c.点燃装置A处酒精灯
d.熄灭装置A处酒精灯
e.熄灭装置C处酒精灯
f.关闭分液漏斗活塞
②装置B的作用为
③装置C的硬质玻璃管中的现象为
(4)设计实验证明Ca3N2中混有钙单质:
Ⅱ.测定氮化钙纯度
ⅰ称取4.0g反应后的固体,加入足量水,将生成的气体全部蒸出并通入100.00mL 1.00mol/L的盐酸中,充分反应后,将所得溶液稀释到200.00mL;
ii.取20.00mL稀释后的溶液,用0.2mol/LNaOH标准溶液滴定过量的盐酸,到终点时消耗标准溶液25.00mL。
(5)所取固体中氮化钙的质量分数为
您最近一年使用:0次
2019-12-02更新
|
552次组卷
|
9卷引用:江西省峡江中学2021-2022学年高二上学期第一次月考化学(理科)试题
10-11高三上·江西吉安·期中
解题方法
5 . 如图是部分短周期元素的单质及其化合物的转化关系图(有关反应的条件及生成的H2O已略去).

已知:
(a)A、B、C、D是非金属单质,其中B、C、D在常温常压下是气体.
(b)反应①、②是化工生产中的重要反应.
(c)化合物E是形成酸雨的污染物之一,化合物K是常用的氮肥.
(d)化合物L具有漂白性,可由Cl2与NaOH溶液反应而制得.
(e)化合物J由两种元素组成,其相对分子质量为32.
请按要求填空:
(1)反应③的化学方程式_____________________ ;
(2)C的结构式__________________________ ;H为正盐,则H的化学式为____________________ ;
(3)L的溶液与化合物E反应的离子方程式:______________ ;
(4)化合物J的化学式____________________ .

已知:
(a)A、B、C、D是非金属单质,其中B、C、D在常温常压下是气体.
(b)反应①、②是化工生产中的重要反应.
(c)化合物E是形成酸雨的污染物之一,化合物K是常用的氮肥.
(d)化合物L具有漂白性,可由Cl2与NaOH溶液反应而制得.
(e)化合物J由两种元素组成,其相对分子质量为32.
请按要求填空:
(1)反应③的化学方程式
(2)C的结构式
(3)L的溶液与化合物E反应的离子方程式:
(4)化合物J的化学式
您最近一年使用:0次



