1 . 设 表示阿伏加德罗常数的值。下列叙述正确的是
表示阿伏加德罗常数的值。下列叙述正确的是
 表示阿伏加德罗常数的值。下列叙述正确的是
表示阿伏加德罗常数的值。下列叙述正确的是A.常温常压下,铁与稀硫酸反应生成 时,转移的电子数约为2 时,转移的电子数约为2 |
B. 与 与 充分反应生成 充分反应生成 的分子数为2 的分子数为2 |
C.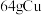 与足量硫粉反应转移的电子数目为2 与足量硫粉反应转移的电子数目为2 |
D.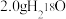 与 与 的混合物中所含电子数为 的混合物中所含电子数为 |
您最近一年使用:0次
名校
解题方法
2 . 已知NA表示阿伏加德罗常数,下列说法正确的是
A. 与S完全反应,转移的电子数为 与S完全反应,转移的电子数为 |
| B.0.1mol Na2O2与水充分反应转移的电子数目为0.2NA |
| C.1mol熔融NaHSO4电离出的阴、阳离子总数目为2NA |
D.密闭容器中,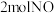 与 与 充分反应后,混合气体中分子数为2NA 充分反应后,混合气体中分子数为2NA |
您最近一年使用:0次
名校
3 . 学科思想方法是学好化学的关键,下列有关学科思想方法的理解正确 的是
| A.根据元素的性质分析,氮元素非金属较强,所以N2的化学性质较活泼 |
| B.SO2和氯水都具有漂白性,当SO2与Cl2体积比1:1通入水中所得溶液漂白性增强 |
| C.通过类比方法可知铝与稀硫酸反应生成氢气,则铝与稀硝酸反应生成氢气 |
| D.从硫的化合价角度分析,Na2SO3既有氧化性又有还原性 |
您最近一年使用:0次
名校
解题方法
4 . 下列物质的转变在给定条件下能通过一步反应实现的是
A. | B. |
C.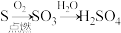 | D.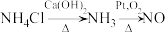 |
您最近一年使用:0次
2022-07-12更新
|
98次组卷
|
3卷引用:江西省部分学校2023-2024学年高二上学期11月期中联考化学试题
名校
解题方法
5 . 氮化镁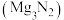 常做催化剂、添加剂。某小组设计实验制备氮化镁并探究其性质。已知:实验室用饱和
常做催化剂、添加剂。某小组设计实验制备氮化镁并探究其性质。已知:实验室用饱和 溶液和
溶液和 溶液共热制备
溶液共热制备 ,氮化镁遇水蒸气会发生反应。
,氮化镁遇水蒸气会发生反应。
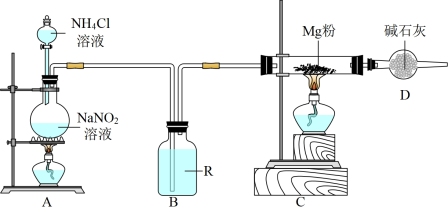
请回答下列问题:
(1)试剂R的名称是_______ ;D装置作用是_______ 。
(2)先启动A装置中的反应,一段时间后,点燃C装置处酒精灯,这样操作的目的是_______ 。
(3)A装置中发生反应的离子方程式为_______ 。
(4)C装置中发生反应的化学方程式为_______ 。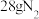 参与该反应时转移
参与该反应时转移_______  电子。
电子。
(5)取少量 样品于试管,加入足量的蒸馏水,用镊子夹一块湿润的红色石蕊试纸放置在试管口上方,试纸逐渐变蓝色;试管里产生白色沉淀,在上层清液中滴加酚酞溶液,溶液变浅红色。根据上述现象分析,氮化镁与水反应生成
样品于试管,加入足量的蒸馏水,用镊子夹一块湿润的红色石蕊试纸放置在试管口上方,试纸逐渐变蓝色;试管里产生白色沉淀,在上层清液中滴加酚酞溶液,溶液变浅红色。根据上述现象分析,氮化镁与水反应生成_______ (填化学式)。如果在稀硝酸中加入少量 粉末,生成的两种盐分别是
粉末,生成的两种盐分别是 和
和_______ (填化学式)。
(6)通过上述探究可知,在实验室里保存 时应注意:
时应注意:_______ 。
 常做催化剂、添加剂。某小组设计实验制备氮化镁并探究其性质。已知:实验室用饱和
常做催化剂、添加剂。某小组设计实验制备氮化镁并探究其性质。已知:实验室用饱和 溶液和
溶液和 溶液共热制备
溶液共热制备 ,氮化镁遇水蒸气会发生反应。
,氮化镁遇水蒸气会发生反应。
请回答下列问题:
(1)试剂R的名称是
(2)先启动A装置中的反应,一段时间后,点燃C装置处酒精灯,这样操作的目的是
(3)A装置中发生反应的离子方程式为
(4)C装置中发生反应的化学方程式为
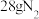 参与该反应时转移
参与该反应时转移 电子。
电子。(5)取少量
 样品于试管,加入足量的蒸馏水,用镊子夹一块湿润的红色石蕊试纸放置在试管口上方,试纸逐渐变蓝色;试管里产生白色沉淀,在上层清液中滴加酚酞溶液,溶液变浅红色。根据上述现象分析,氮化镁与水反应生成
样品于试管,加入足量的蒸馏水,用镊子夹一块湿润的红色石蕊试纸放置在试管口上方,试纸逐渐变蓝色;试管里产生白色沉淀,在上层清液中滴加酚酞溶液,溶液变浅红色。根据上述现象分析,氮化镁与水反应生成 粉末,生成的两种盐分别是
粉末,生成的两种盐分别是 和
和(6)通过上述探究可知,在实验室里保存
 时应注意:
时应注意:
您最近一年使用:0次
名校
6 . 下列各组化合物中,均能由单质直接化合而得到的是
A. 、CuS、 、CuS、 、FeS 、FeS | B. 、 、 、 、 、 、 |
C. 、 、 、NO、 、NO、 | D. 、FeS、 、FeS、 、 、 |
您最近一年使用:0次
2022-04-13更新
|
151次组卷
|
3卷引用:江西省宁冈中学2022-2023学年高三上学期12月月考化学试题
名校
解题方法
7 . 氮是生命活动不可缺少的重要元素。下列叙述错误的是
| A.氮气既可作氧化剂又可作还原剂 |
B.氮气和氧气在放电条件下直接生成 |
| C.氮气是工业合成氨的原料之一 |
| D.氮的固定是将大气中的氮气转化成氮的化合物 |
您最近一年使用:0次
2021-04-26更新
|
851次组卷
|
3卷引用:江西省贵溪市实验中学2020-2021学年高一下学期第三次月考化学试题
名校
解题方法
8 . 某学习小组设计实验制备氮化锂(Li3N)并测定其纯度,装置如下所示:
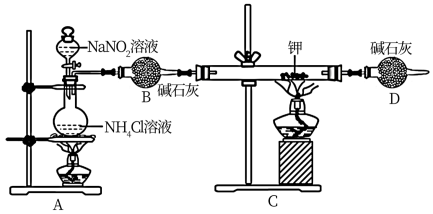
已知:i.Li3N遇水剧烈反应。
ii.实验室用NH4Cl溶液和NaNO2溶液共热制备N2。
请回答:
(1)写出制备N2的化学方程式_______ 。
(2)仪器B的名称为_______ ;D装置的作用是_______ 。
(3)实验室将金属钠和理均可保仔在_______ 中(填相应的编号)。
a.乙醇(CH3CH2OH) b.煤油c.石蜡油d.苯
(4)测定Li3N产品纯度:取m gLi3N产品按下图所示装置进行实验。
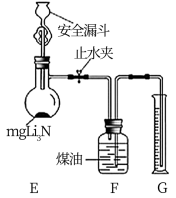
打开止水夹,向安全漏斗中加入足量水,当Li3N完全反应后,调平F和G中液面,测得气体体积为V L(已折合成标准状况下)。
①安全漏斗中“安全”含义是_______ 。
②Li3N与水反应的化学方程式_______ 。
③读数前调平F和G中液面的目的是_______ 。
④该Li3N产品的纯度为_______ %(只列出含m和V的计算式,不必计算化简)。
⑤若Li3N产品混有Li,则测得纯度_______ (选填“偏高”、“偏低”或“无影响")。(已知Li3N的相对分子质量为35)

已知:i.Li3N遇水剧烈反应。
ii.实验室用NH4Cl溶液和NaNO2溶液共热制备N2。
请回答:
(1)写出制备N2的化学方程式
(2)仪器B的名称为
(3)实验室将金属钠和理均可保仔在
a.乙醇(CH3CH2OH) b.煤油c.石蜡油d.苯
(4)测定Li3N产品纯度:取m gLi3N产品按下图所示装置进行实验。

打开止水夹,向安全漏斗中加入足量水,当Li3N完全反应后,调平F和G中液面,测得气体体积为V L(已折合成标准状况下)。
①安全漏斗中“安全”含义是
②Li3N与水反应的化学方程式
③读数前调平F和G中液面的目的是
④该Li3N产品的纯度为
⑤若Li3N产品混有Li,则测得纯度
您最近一年使用:0次
名校
9 . 已知A、B、C、D为由短周期元素组成的四种物质,它们有如图所示转化关系,且D为强电解质(其他相关物质可能省略)。下列说法错误的是( )
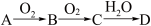
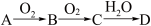
| A.若A为非金属单质,则它与Mg反应的产物中阳、阴离子个数比可能为3:2 |
| B.若A为非金属单质,则其组成元素在周期表中的位置可能处于第二周期第IVA族 |
| C.若A为金属单质,则A和C有可能发生氧化还原反应 |
| D.若A是金属或非金属单质,则常温下0.1mol·L-1的D溶液中由水电离出的c(H+)可能为10-13mol·L-1 |
您最近一年使用:0次
10 . 下列化学工艺不可行的是( )
A.N2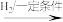 NO NO NO2 NO2  HNO3 HNO3 |
B.石英砂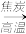 粗硅 粗硅 粗SiCl4 粗SiCl4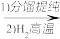 高纯硅 高纯硅 |
C.提取食盐后的母液 含Br2的溶液 含Br2的溶液 … … 粗Br2 粗Br2 Br2 Br2 |
D.铝土矿 NaAlO2(aq) NaAlO2(aq)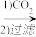 Al(OH)3 Al(OH)3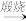 Al2O3 Al2O3 Al Al |
您最近一年使用:0次



