名校
解题方法
1 . 氮化钙(Ca3N2)时一种重要的化学试剂,通常条件下为棕色易水解的固体。某小组在实验室制备氮化钙并测定其纯度,设计如下实验
Ⅰ.氮化钙的制备。
(1)加热条件下,钙和氮气制备氮化钙的反应方程式为______ 。
(2)钙和氮气制备氮化钙的装置如下(夹持装置略去):

上述装置合理的连接顺序为______ (按气流方向,用接口字母表示,装置不重复使用)。
(3)按连接好的装置进行实验。
①实验步骤如下:检查装置气密性、加入药品:______ (请按正确顺序填入下列步骤的字母标号)。
a.点燃装置C处酒精灯,反应一段时间
b.打开分液漏斗活塞
c.点燃装置A处酒精灯
d.熄灭装置A处酒精灯
e.熄灭装置C处酒精灯
f.关闭分液漏斗活塞
②装置B的作用为______ 。
③装置C的硬质玻璃管中的现象为______
(4)设计实验证明Ca3N2中混有钙单质:______
Ⅱ.测定氮化钙纯度
ⅰ称取4.0g反应后的固体,加入足量水,将生成的气体全部蒸出并通入100.00mL 1.00mol/L的盐酸中,充分反应后,将所得溶液稀释到200.00mL;
ii.取20.00mL稀释后的溶液,用0.2mol/LNaOH标准溶液滴定过量的盐酸,到终点时消耗标准溶液25.00mL。
(5)所取固体中氮化钙的质量分数为______ 。
Ⅰ.氮化钙的制备。
(1)加热条件下,钙和氮气制备氮化钙的反应方程式为
(2)钙和氮气制备氮化钙的装置如下(夹持装置略去):

上述装置合理的连接顺序为
(3)按连接好的装置进行实验。
①实验步骤如下:检查装置气密性、加入药品:
a.点燃装置C处酒精灯,反应一段时间
b.打开分液漏斗活塞
c.点燃装置A处酒精灯
d.熄灭装置A处酒精灯
e.熄灭装置C处酒精灯
f.关闭分液漏斗活塞
②装置B的作用为
③装置C的硬质玻璃管中的现象为
(4)设计实验证明Ca3N2中混有钙单质:
Ⅱ.测定氮化钙纯度
ⅰ称取4.0g反应后的固体,加入足量水,将生成的气体全部蒸出并通入100.00mL 1.00mol/L的盐酸中,充分反应后,将所得溶液稀释到200.00mL;
ii.取20.00mL稀释后的溶液,用0.2mol/LNaOH标准溶液滴定过量的盐酸,到终点时消耗标准溶液25.00mL。
(5)所取固体中氮化钙的质量分数为
您最近一年使用:0次
2019-12-02更新
|
552次组卷
|
9卷引用:江西省新余市第一中学2019-2020学年高一下学期第一次月考化学试题
名校
2 . 给定条件下,下列选项中所示的物质间在相应条件下转化均能一步实现的是( )
A.SiO2 H2SiO3 H2SiO3 Na2SiO3(aq) Na2SiO3(aq) |
B.Ca(OH)2 Ca(ClO)2 Ca(ClO)2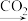 HClO HClO |
C.MgCl2•6H2O MgCl2 MgCl2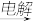 Mg Mg |
D.N2 NO2 NO2 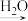 HNO3 HNO3 |
您最近一年使用:0次
2019-11-20更新
|
221次组卷
|
2卷引用:江西省南昌市第二中学2020届高三第四次月考化学试题
10-11高三上·江西吉安·期中
解题方法
3 . 如图是部分短周期元素的单质及其化合物的转化关系图(有关反应的条件及生成的H2O已略去).

已知:
(a)A、B、C、D是非金属单质,其中B、C、D在常温常压下是气体.
(b)反应①、②是化工生产中的重要反应.
(c)化合物E是形成酸雨的污染物之一,化合物K是常用的氮肥.
(d)化合物L具有漂白性,可由Cl2与NaOH溶液反应而制得.
(e)化合物J由两种元素组成,其相对分子质量为32.
请按要求填空:
(1)反应③的化学方程式_____________________ ;
(2)C的结构式__________________________ ;H为正盐,则H的化学式为____________________ ;
(3)L的溶液与化合物E反应的离子方程式:______________ ;
(4)化合物J的化学式____________________ .

已知:
(a)A、B、C、D是非金属单质,其中B、C、D在常温常压下是气体.
(b)反应①、②是化工生产中的重要反应.
(c)化合物E是形成酸雨的污染物之一,化合物K是常用的氮肥.
(d)化合物L具有漂白性,可由Cl2与NaOH溶液反应而制得.
(e)化合物J由两种元素组成,其相对分子质量为32.
请按要求填空:
(1)反应③的化学方程式
(2)C的结构式
(3)L的溶液与化合物E反应的离子方程式:
(4)化合物J的化学式
您最近一年使用:0次
名校
4 . 臭氧是常见的强氧化剂,广泛用于水处理系统。制取臭氧的方法很多,其中高压放电法和电解纯水法原理如下图所示,下列有关说法不正确的是


A.高压放电法,反应的原理为3O2 2O3 2O3 |
| B.高压放电出来的空气中,除含臭氧外还含有氮的氧化物 |
C.电解时,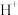 由电极 由电极 经聚合固体电解质膜流向电极 经聚合固体电解质膜流向电极 |
D.电解时,电极 周围发生的电极反应有 周围发生的电极反应有 和 和 |
您最近一年使用:0次
名校
5 . 下列实验现象预测、实验设计、仪器使用能达到目的是
A.模拟工业制氨气并检验产物 |
B.实验室采用所示装置收集SO2 |
C.验证KMnO4,Cl2,S 氧化性强弱 |
D.验证铁发生析氢腐蚀 |
您最近一年使用:0次
名校
6 . 设NA为阿伏伽德罗常数的值,下列叙述正确的是
| A.常温下,2.7g铝片投入足量的浓硫酸中,铝失去的电子数为0.3NA |
| B.标准状况下,2.24 L SO3中所含原子数为0.4NA |
| C.常温常压下,16g O2和O3的混合气体中所含原子数目为NA |
| D.在一定条件下,1mol N2与3mol H2反应生成的NH3分子数为2NA |
您最近一年使用:0次
2018-05-16更新
|
1902次组卷
|
5卷引用:江西省宜春市宜丰县宜丰中学2019-2020学年高一下学期第一次月考化学试题
7 . 化学在生活中应用广泛,下列物质性质与对应用途错误的是
| A.明矾易水解生成胶体,可用作净水剂 |
| B.晶体硅熔点高硬度大,可用作芯片 |
| C.氮气化学性质稳定,可用作粮食保护气 |
| D.NaClO具有强氧化性,可作织物漂白剂 |
您最近一年使用:0次
名校
8 . 甲、乙、丙、丁、戊五种物质中,甲、乙、丙中均含有某种相同的元素,它们之间具有如图所示转化关系(反应条件及部分产物已略去)。下列有关物质的推断不正确的是
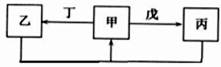

| A.若甲为Al(OH)3,则戊可能为NaOH | B.若甲为Na2CO3,则丁可能为CO2 |
| C.若甲为N2,则丁可能为O2 | D.若甲为Fe, 则戊可能为盐酸 |
您最近一年使用:0次
2017-03-21更新
|
473次组卷
|
2卷引用:江西省新余市第一中学2018届高三毕业年级第二次模拟考试化学试题
名校
9 . 下列有关氮气的说法正确的是
| A.氮气是由氮原子构成的双原子分子,所以化学性质不活泼 |
| B.1 mol N2可与3 mol H2完全反应生成2 mol NH3 |
| C.电闪雷鸣的雨天,雨水中会含有一定量的硝酸,其中发生的反应之一是N2+2O2 = 2NO2 |
| D.NO、NO2在一定条件下可相互转化,且二者都是引起光化学烟雾的大气污染物 |
您最近一年使用:0次
2017-03-08更新
|
395次组卷
|
4卷引用:江西省丰城市第二中学2023-2024学年高一上学期11月期中考试化学试题
10 . 以下物质间的每步转化通过一步反应就能实现的是
| A.N2→NO2→HNO3 |
| B.Fe→FeCl3→FeCl2 |
| C.Si→H2SiO3→Na2SiO3 |
| D.Al2O3→Al(OH)3→NaAlO2 |
您最近一年使用:0次



