21-22高一下·全国·单元测试
解题方法
1 . 1.氮的氧化物
(1)氮的氧化物
简介:氮元素有_______ 五种正价态,对应有六种氧化物
(2)NO和 的重要性质和制法(横线部分书写化学方程式)
的重要性质和制法(横线部分书写化学方程式)
①性质:_______ (易被氧气氧化,无色气体转化为红棕色);
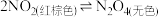 (平衡体系);
(平衡体系);
_______ (工业制硝酸);
_______ (尾气吸收);
 有较强的氧化性,能使湿润的KI淀粉试纸
有较强的氧化性,能使湿润的KI淀粉试纸_______ 。
②制法:
NO: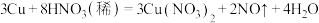 (必须
(必须_______ 法收集NO);
 :
: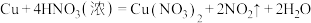 (必须
(必须_______ 法收集 )
)
(3)氮的氧化物溶于水的计算
① 或
或 与
与 (非
(非 )的混合气体溶于水可依据
)的混合气体溶于水可依据 利用气体体积变化差值进行计算。
利用气体体积变化差值进行计算。
② 和O2的混合气体溶于水时,由
和O2的混合气体溶于水时,由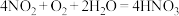 进行计算,当体积比
进行计算,当体积比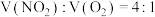 时,恰好反应;
时,恰好反应; 时,
时, 过量,剩余NO;
过量,剩余NO; 时,
时, 过量,剩余
过量,剩余 。
。
③NO和 同时通入水中时,由
同时通入水中时,由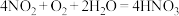 进行计算,原理同②。
进行计算,原理同②。
④NO、 、
、 的混合气体通入水中,先按①求出NO的体积,再加上混合气体中NO的体积再按③方法进行计算。
的混合气体通入水中,先按①求出NO的体积,再加上混合气体中NO的体积再按③方法进行计算。
(1)氮的氧化物
简介:氮元素有
| 种类 | 色态 | 化学性质 |
 | 无色气体 | 较不活泼 |
| NO | 活泼,不溶于水 | |
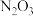 (亚硝酸酐) (亚硝酸酐) | 蓝色液体(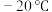 ) ) | 常温极易分解为NO, |
 | 较活泼,与水反应 | |
 | 无色气体 | 较活泼,受热易分解 |
 (硝酸酸酐) (硝酸酸酐) | 无色固体 | 气态时不稳定,易分解 |
 的重要性质和制法(横线部分书写化学方程式)
的重要性质和制法(横线部分书写化学方程式)①性质:
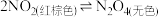 (平衡体系);
(平衡体系); 有较强的氧化性,能使湿润的KI淀粉试纸
有较强的氧化性,能使湿润的KI淀粉试纸②制法:
NO:
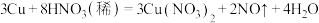 (必须
(必须 :
: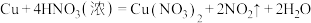 (必须
(必须 )
)(3)氮的氧化物溶于水的计算
①
 或
或 与
与 (非
(非 )的混合气体溶于水可依据
)的混合气体溶于水可依据 利用气体体积变化差值进行计算。
利用气体体积变化差值进行计算。②
 和O2的混合气体溶于水时,由
和O2的混合气体溶于水时,由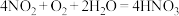 进行计算,当体积比
进行计算,当体积比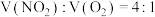 时,恰好反应;
时,恰好反应; 时,
时, 过量,剩余NO;
过量,剩余NO; 时,
时, 过量,剩余
过量,剩余 。
。③NO和
 同时通入水中时,由
同时通入水中时,由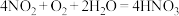 进行计算,原理同②。
进行计算,原理同②。④NO、
 、
、 的混合气体通入水中,先按①求出NO的体积,再加上混合气体中NO的体积再按③方法进行计算。
的混合气体通入水中,先按①求出NO的体积,再加上混合气体中NO的体积再按③方法进行计算。
您最近一年使用:0次
名校
解题方法
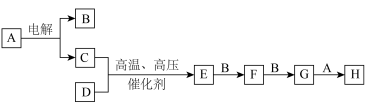
2 . 某些无机物的转化关系(部分反应物和生成物未列出)如图。已知化合物A为常见液体,气体E能使湿润的红色石蕊试纸变蓝。_____________ (填标号)。
a. b.
b.
(2)B、D在常温下难以发生反应,其主要原因为____________ 。
(3)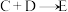 对人类的意义为
对人类的意义为_________________ (任写一点即可)。
(4)少量的E与氯气反应有白雾出现,写出该反应的化学方程式:______________ ;试推测过量的E与氯气反应的现象:_____________ 。
(5)用 溶液可吸收F与G的混合气体,反应产物为水和一种钠盐,写出该反应的离子方程式:
溶液可吸收F与G的混合气体,反应产物为水和一种钠盐,写出该反应的离子方程式:_________________ ,该反应中氧化产物与还原产物的物质的量之比为______________ 。
(6)常温常压下(气体摩尔体积为 ),将
),将 盛满B、G混合气体(体积比为1:1)的试管倒立于水槽中,反应完全后,试管中剩余气体的体积为
盛满B、G混合气体(体积比为1:1)的试管倒立于水槽中,反应完全后,试管中剩余气体的体积为______________  ,试管中所得溶液的物质的量浓度为
,试管中所得溶液的物质的量浓度为_____________  (用含
(用含 的代数式表示,假设溶质不向试管外扩散)。
的代数式表示,假设溶质不向试管外扩散)。
a.
 b.
b.
(2)B、D在常温下难以发生反应,其主要原因为
(3)
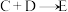 对人类的意义为
对人类的意义为(4)少量的E与氯气反应有白雾出现,写出该反应的化学方程式:
(5)用
 溶液可吸收F与G的混合气体,反应产物为水和一种钠盐,写出该反应的离子方程式:
溶液可吸收F与G的混合气体,反应产物为水和一种钠盐,写出该反应的离子方程式:(6)常温常压下(气体摩尔体积为
 ),将
),将 盛满B、G混合气体(体积比为1:1)的试管倒立于水槽中,反应完全后,试管中剩余气体的体积为
盛满B、G混合气体(体积比为1:1)的试管倒立于水槽中,反应完全后,试管中剩余气体的体积为 ,试管中所得溶液的物质的量浓度为
,试管中所得溶液的物质的量浓度为 (用含
(用含 的代数式表示,假设溶质不向试管外扩散)。
的代数式表示,假设溶质不向试管外扩散)。
您最近一年使用:0次
2024-05-03更新
|
58次组卷
|
3卷引用:河南省南阳市社旗县第一高级中学2023-2024学年高一下学期4月期中考试化学试题
名校
3 . 绿水青山,保护环境是当今社会发展必须关注的重要课题。氮氧化物和硫氧化物是造成大气污染的主要原因之一,消除氮氧化物有多种方法。
 催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术,反应原理如图1所示。
催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术,反应原理如图1所示。___________ (任写一点)。
(2) 与
与 反应的化学方程式
反应的化学方程式___________ 。
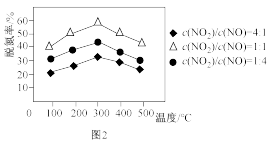
(3)用Fe做催化剂时,在氨气足量的情况下,不同 对应的脱氮率如图2所示,脱氮效果最佳的
对应的脱氮率如图2所示,脱氮效果最佳的
___________ 。 B.
B. C.
C.
 催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术,反应原理如图1所示。
催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术,反应原理如图1所示。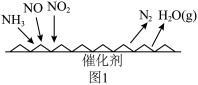
(2)
 与
与 反应的化学方程式
反应的化学方程式(3)用Fe做催化剂时,在氨气足量的情况下,不同
 对应的脱氮率如图2所示,脱氮效果最佳的
对应的脱氮率如图2所示,脱氮效果最佳的
 B.
B. C.
C.
您最近一年使用:0次
2024-05-01更新
|
42次组卷
|
2卷引用:上海市南洋中学2023-2024学年高一下学期期中考试化学试题
4 . 亚硝酰氯(NOCl)是重要的有机合成试剂,可由NO与Cl2在常温下合成。NOCl可与氧气反应,易水解生成一种氧化物和氯化氢,已知各物质的沸点:NOCl为-5.5℃,Cl2为-34℃,NO为-152℃,某学习小组在实验室利用如图装置制备亚硝酰氯。
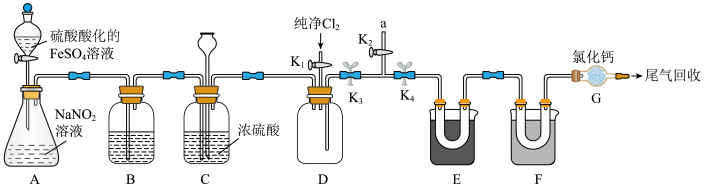
回答下列问题:
(1)A装置的作用是制取NO,反应的离子方程式为
(2)实验时利用装置B除去某些杂质气体并通过观察B中的气泡来判断反应速率,则装置B中所盛试剂为
(3)C中长颈漏斗的作用是
(4)实验室用二氧化锰和浓盐酸制取Cl2的反应中氧化剂和还原剂的比例为
(5)实验开始时,先关闭K3,打开K2、K4,从a处通一段时间氩气将E、F装置中的空气排尽,然后在a处接废气处理装置,关闭K1、K4,打开K3,再打开分液漏斗的活塞,滴加酸性FeSO4溶液,当观察到D中
(6)为收集产物和分离未反应的两种原料,E、F装置采用不同温度的低温浴槽,其中装置E的温度T区间应控制在
您最近一年使用:0次
名校
5 . 下列气体可用如图所示方法收集的是
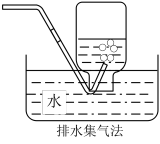
| A.NO | B.HCl | C.SO2 | D.NH3 |
您最近一年使用:0次
2024-03-23更新
|
189次组卷
|
3卷引用:5.2.2 氨气的物理性质 随堂练习
23-24高一下·全国·课前预习
解题方法
6 . 工业上用水吸收NO2制取硝酸的反应过程中,常需要不断地补充一些空气,其目的是什么_______ ?
您最近一年使用:0次
23-24高一下·全国·课前预习
解题方法
7 . 一氧化氮属于氧化物,其颜色________ ,状态________ ,气味________ ,水溶性________ ,毒性________ 。
您最近一年使用:0次
名校
8 . 汽车尾气催化转化装置的工作原理如图所示。下列说法中,不正确 的是


A.汽车尾气中含有的 和 和 是大气污染物 是大气污染物 |
| B.使用催化转化装置可减少汽车尾气对大气的污染 |
C.该过程中 的作用是作氧化剂 的作用是作氧化剂 |
D.该过程中会发生反应: |
您最近一年使用:0次
名校
解题方法
9 . 下列污染是以NO、NO2为主的氮氧化物造成的有
①温室效应②雾霾③光化学烟雾④酸雨⑤白色污染⑥臭氧空洞
①温室效应②雾霾③光化学烟雾④酸雨⑤白色污染⑥臭氧空洞
| A.②③④⑥ | B.①②③④ | C.③④⑤⑥ | D.②③④⑤ |
您最近一年使用:0次
2024-02-01更新
|
466次组卷
|
3卷引用:新疆乌鲁木齐市新疆生产建设兵团第二中学2023-2024学年高一上学期期末考试化学试卷
解题方法
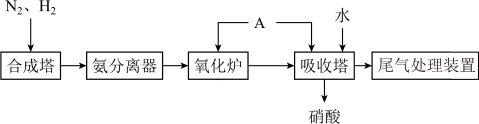
10 . 氨既是一种重要的化工产品,又是一种重要的化工原料。下图为合成氨以及氨氧化制硝酸的流程示意图。
(1) 和
和 必须经过净化才能进入合成塔,最主要的原因是
必须经过净化才能进入合成塔,最主要的原因是______________ 。
(2)简述氨分离器中,将氨从平衡混合物中分离出去的方法:______________ 。
(3)氧化炉中主要反应的化学方程式为______________ 。
(4)向吸收塔中通入 的作用是
的作用是______________ 。
(5)工业上常用碱液来进行尾气处理,有关的化学反应为
①
②
现有一定条件下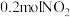 和
和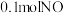 的混合气体恰好被
的混合气体恰好被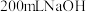 溶液完全吸收,则
溶液完全吸收,则 溶液的物质的量浓度为
溶液的物质的量浓度为_______  。
。
(6)实验室中硝酸一般盛放在棕色试剂瓶中,用化学方程式说明其原因:______________ 。
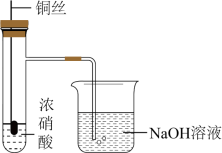
(7)利用下图所示装置进行铜与稀硝酸反应的实验可以观察到的实验现象为______________ 。
(1)
 和
和 必须经过净化才能进入合成塔,最主要的原因是
必须经过净化才能进入合成塔,最主要的原因是(2)简述氨分离器中,将氨从平衡混合物中分离出去的方法:
(3)氧化炉中主要反应的化学方程式为
(4)向吸收塔中通入
 的作用是
的作用是(5)工业上常用碱液来进行尾气处理,有关的化学反应为
①

②

现有一定条件下
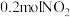 和
和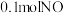 的混合气体恰好被
的混合气体恰好被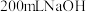 溶液完全吸收,则
溶液完全吸收,则 溶液的物质的量浓度为
溶液的物质的量浓度为 。
。(6)实验室中硝酸一般盛放在棕色试剂瓶中,用化学方程式说明其原因:
(7)利用下图所示装置进行铜与稀硝酸反应的实验可以观察到的实验现象为
您最近一年使用:0次



