21-22高一下·全国·单元测试
解题方法
1 . 硝酸( )
)
(1)物理性质:无色、_______ 气味、_______ 挥发液体,能与水以任意比例互溶,常用浓硝酸的质量分数大约为69%。
(2)化学性质
硝酸为_______ 酸,具有以下性质:
①具有酸的通性;
②不稳定性:_______ ;
③强氧化性:无论浓、稀硝酸均具有强氧化性,与金属反应时不放出_______ 。
A.与金属反应:
铜与浓硝酸:_______ ;
铜与稀硝酸:_______ ;
银与浓硝酸:_______ ;
常温下浓硝酸与铁、铝发生_______ 。
B.与非金属反应:
碳与浓硝酸:_______ 。
C.与其他还原剂反应,如H2S、SO2、Fe2+等。
D.与有机物反应:硝化反应、酯化反应、与蛋白质发生颜色反应等。
(3)制法
①实验室制法:硝酸盐与浓硫酸微热,_______ (不能用强热和稀硫酸);
②工业制法:
氨的催化氧化法:_______ ;_______ ;_______ ;
尾气处理:_______ (用NaOH溶液吸收尾气)。
(4)用途:_______ 等。
 )
)(1)物理性质:无色、
(2)化学性质
硝酸为
①具有酸的通性;
②不稳定性:
③强氧化性:无论浓、稀硝酸均具有强氧化性,与金属反应时不放出
A.与金属反应:
铜与浓硝酸:
铜与稀硝酸:
银与浓硝酸:
常温下浓硝酸与铁、铝发生
B.与非金属反应:
碳与浓硝酸:
C.与其他还原剂反应,如H2S、SO2、Fe2+等。
D.与有机物反应:硝化反应、酯化反应、与蛋白质发生颜色反应等。
(3)制法
①实验室制法:硝酸盐与浓硫酸微热,
②工业制法:
氨的催化氧化法:
尾气处理:
(4)用途:
您最近一年使用:0次
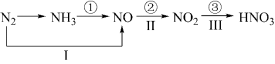
2 . 氮及其化合物的转化关系如图所示: ___________ ,其中氧化剂与还原剂的质量之比是___________ 。
(2)某研究小组为了探究硝酸的性质,进行如下实验操作。
①从试剂柜中取一瓶浓硝酸,发现其保存在___________ 色试剂瓶中,取少量浓硝酸于试管中,发现其溶液呈“黄色”,其原因是___________ (用化学方程式表达)。该研究小组尝试将显“黄色”的浓硝酸恢复到原本的无色。下列措施合理的是___________ (填字母)。
a.加热浓硝酸 b.向硝酸中加水
c.向浓硝酸中通入适量空气 d.向浓硝酸中加入适量的NaOH固体
②向浓硝酸中加入稍过量铜片,在反应中硝酸体现的性质为___________ 。当实验完毕,该小组同学向试管中滴入少量稀硫酸,发现铜片又逐渐溶解,产生无色气体,请写出反应的离子方程式___________ 。
(2)某研究小组为了探究硝酸的性质,进行如下实验操作。
①从试剂柜中取一瓶浓硝酸,发现其保存在
a.加热浓硝酸 b.向硝酸中加水
c.向浓硝酸中通入适量空气 d.向浓硝酸中加入适量的NaOH固体
②向浓硝酸中加入稍过量铜片,在反应中硝酸体现的性质为
您最近一年使用:0次
2024-05-07更新
|
74次组卷
|
2卷引用:名校期末好题汇编-非金属元素(非选择题)
2024高三·全国·专题练习
3 . 下列关于元素及其化合物的性质说法错误的是
| A.浓硫酸遇胆矾变“白”,体现了浓硫酸的吸水性 |
| B.硝酸见光受热易分解,一般保存在棕色试剂瓶中,放置在阴凉处 |
| C.燃油发动机产生的NO2、NO与CO反应能生成N2和CO2,因此可以直接排放 |
| D.铝制餐具不宜用来蒸煮或长时间存放酸性或者碱性食物 |
您最近一年使用:0次
名校
4 . 硫酸工业在国民经济中占有重要地位。
(1)在18世纪40年代以前,生产硫酸最古老的方法是:以绿矾( )为原料在蒸馏釜中煅烧(隔离空气),除有水蒸气生成外,还有两种气体生成,然后再冷凝至室温,得到一种液体,称之为“绿矾油”,其主要成分为
)为原料在蒸馏釜中煅烧(隔离空气),除有水蒸气生成外,还有两种气体生成,然后再冷凝至室温,得到一种液体,称之为“绿矾油”,其主要成分为___________ (填化学式)。该方法中“煅烧”反应方程式为:___________ (补全反应化学方程式)。
 ___________
___________
(2)“铅室法”[使用了大容积铅室制备硫酸(76%以下)]与“塔士法”制硫酸的主要反应有:
___________ ___________
___________ ___________+___________
___________+___________
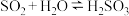
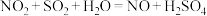


副反应: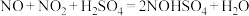
①补全反应化学方程式___________ 。
___________ ___________
___________ ___________+___________
___________+___________
② 在上述过程中作用为
在上述过程中作用为___________ 。
③上述方法生产硫酸的总反应为___________ 。
④为了适应化工生产的需求 “铅室法”、“塔式法”最终被接触法所代替,其主要原因是___________ (答出一点即可)。
(3)有关接触法制硫酸的叙述,其中错误的是___________。
(1)在18世纪40年代以前,生产硫酸最古老的方法是:以绿矾(
 )为原料在蒸馏釜中煅烧(隔离空气),除有水蒸气生成外,还有两种气体生成,然后再冷凝至室温,得到一种液体,称之为“绿矾油”,其主要成分为
)为原料在蒸馏釜中煅烧(隔离空气),除有水蒸气生成外,还有两种气体生成,然后再冷凝至室温,得到一种液体,称之为“绿矾油”,其主要成分为 ___________
___________(2)“铅室法”[使用了大容积铅室制备硫酸(76%以下)]与“塔士法”制硫酸的主要反应有:
___________
 ___________
___________ ___________+___________
___________+___________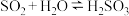
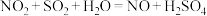


副反应:
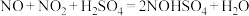
①补全反应化学方程式
___________
 ___________
___________ ___________+___________
___________+___________②
 在上述过程中作用为
在上述过程中作用为③上述方法生产硫酸的总反应为
④为了适应化工生产的需求 “铅室法”、“塔式法”最终被接触法所代替,其主要原因是
(3)有关接触法制硫酸的叙述,其中错误的是___________。
| A.用硫黄或含硫矿石均可作为原料 |
| B.尾气含有二氧化硫,在排入大气前需进行净化处理 |
| C.硫酸生产中涉及的化学反应全部是氧化还原反应 |
| D.硫酸生产中涉及的化学反应都需要使用催化剂 |
您最近一年使用:0次
5 . 下列关于浓硝酸和浓硫酸说法错误的是
| A.常温下,可用铁制容器储存浓硫酸、浓硝酸 |
| B.等量的铜分别溶于足量的浓硝酸、浓硫酸中,还原产物的物质的量相等 |
| C.浓硝酸通常保存在棕色试剂瓶中 |
| D.浓硫酸能与灼热的木炭反应,生成二氧化碳、二氧化硫和水 |
您最近一年使用:0次
2024-03-05更新
|
543次组卷
|
6卷引用:5.2.3硝酸和酸雨的防治课后作业提高篇
(已下线)5.2.3硝酸和酸雨的防治课后作业提高篇(已下线)专题02 氮及其化合物(考题猜想)(8大题型)-2023-2024学年高一化学下学期期中考点大串讲(人教版2019必修第二册)5.2.3 硝酸、酸雨及防治 随堂练习黑龙江省哈尔滨市第六中学校2023-2024学年高一下学期4月测试化学试卷新疆阿克苏市实验中学2022-2023学年高一下学期第三次月考化学试题宁夏吴忠市青铜峡市宁朔中学2023-2024学年高一下学期3月月考化学试题
23-24高一下·全国·课前预习
6 . 硝酸化学性质
(1)硝酸是一元强酸,具有酸的通性。
硝酸与CaCO3反应的化学方程式为:______ 。
(2)不稳定性
硝酸不稳定,______ 或______ 易分解,化学方程式为:______ 。
硝酸的保存方法是______ 。
(3)强氧化性
硝酸是一种氧化性很强的酸,能与大多数金属(除Au、Pt等少数金属以外)、许多非金属以及有机物发生氧化还原反应。
①HNO3与金属反应
分别写出浓硝酸、稀硝酸分别与Cu的反应方程式:______ ,______ 。
②硝酸与非金属的反应
写出C与浓硝酸反应的方程式:______ 。
③常温下浓硝酸可以使______ 、______ 等金属发生钝化。可以用______ 或______ 容器盛放浓硝酸。
(1)硝酸是一元强酸,具有酸的通性。
硝酸与CaCO3反应的化学方程式为:
(2)不稳定性
硝酸不稳定,
硝酸的保存方法是
(3)强氧化性
硝酸是一种氧化性很强的酸,能与大多数金属(除Au、Pt等少数金属以外)、许多非金属以及有机物发生氧化还原反应。
①HNO3与金属反应
分别写出浓硝酸、稀硝酸分别与Cu的反应方程式:
②硝酸与非金属的反应
写出C与浓硝酸反应的方程式:
③常温下浓硝酸可以使
您最近一年使用:0次
名校
解题方法
7 . 为了探究浓硝酸的性质,进行以下五组实验,均观察到红棕色气体。下列分析错误的是
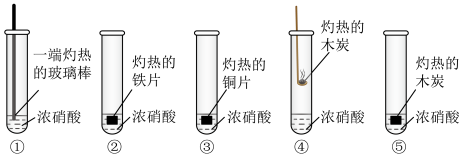
| A.将带火星的木条靠近①的试管口,木条复燃,说明NO2能支持燃烧 |
| B.②中的铁片钝化,红棕色气体由浓硝酸分解产生,③中溶液变为绿色 |
| C.①④⑤实验对比,④中的红棕色气体可能是由挥发的浓硝酸受热分解产生的 |
| D.五支试管中的红棕色气体均为还原产物 |
您最近一年使用:0次
2023-12-20更新
|
1467次组卷
|
6卷引用:第五章 化工生产中的重要非金属元素 单元测试
8 . 下列试剂的保存方法不正确的是
| A.浓硫酸保存在无色玻璃瓶中 |
| B.硫黄粉保存在无色广口瓶中 |
| C.浓硝酸保存在棕色试剂瓶中 |
| D.氢氧化钠溶液保存在带磨口玻璃塞的玻璃试剂瓶中 |
您最近一年使用:0次
9 . 用 表示阿伏加德罗常数的值,下列叙述错误的是
表示阿伏加德罗常数的值,下列叙述错误的是
 表示阿伏加德罗常数的值,下列叙述错误的是
表示阿伏加德罗常数的值,下列叙述错误的是A.2.0g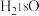 与 与 的混合物中所含质子数、中子数均为 的混合物中所含质子数、中子数均为 |
B.标准状况下,11.2L 中含有S原子的数目为 中含有S原子的数目为 |
C.1mol 中含阴、阳离子总数为 中含阴、阳离子总数为 |
D.浓硝酸受热分解生成 、 、 共23g,转移电子数为 共23g,转移电子数为 |
您最近一年使用:0次
解题方法
10 . 化工工程师设计流程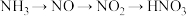 ,实现了硝酸的工业生产。下列说法错误的是
,实现了硝酸的工业生产。下列说法错误的是
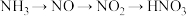 ,实现了硝酸的工业生产。下列说法错误的是
,实现了硝酸的工业生产。下列说法错误的是| A.NH3中氮元素的化合价为-3价 | B.HNO3热稳定性良好 |
| C.NO遇空气变为红棕色的NO2 | D.可用NaOH溶液处理硝酸工业产生的尾气 |
您最近一年使用:0次



