解题方法
1 . 请回答:
(1)①氧化铝的化学式_______ ,②氯气的电子式是_______ 。
(2)向FeCl3溶液中滴加NaOH,产生_______ 色沉淀。
(3)浓硝酸见光分解的化学方程式是_______ 。
(1)①氧化铝的化学式
(2)向FeCl3溶液中滴加NaOH,产生
(3)浓硝酸见光分解的化学方程式是
您最近一年使用:0次
解题方法
2 . 下列关于氮及其化合物的说法正确的是
| A.镁、锌等活泼金属可与稀硝酸反应,生成氢气 |
| B.氮的固定只有在高温、高压、催化剂存在的条件下才能实现 |
| C.向浓HNO3中插入红热的炭,产生红棕色气体,不能证明炭可与浓HNO3反应生成NO2 |
| D.浓硝酸氧化性强,不能用铁质或铝质容器贮运 |
您最近一年使用:0次
3 . 下列说法正确的是
| A.医疗上常用95%的乙醇溶液作消毒剂 |
| B.浓硝酸应保存在棕色试剂瓶,放置在阴凉处 |
| C.可用排空气法收集NO |
| D.淀粉和纤维素互为同分异构体 |
您最近一年使用:0次
4 . 下列关于浓硝酸和浓硫酸说法错误的是
| A.常温下,可用铁制容器储存浓硫酸、浓硝酸 |
| B.等量的铜分别溶于足量的浓硝酸、浓硫酸中,还原产物的物质的量相等 |
| C.浓硝酸通常保存在棕色试剂瓶中 |
| D.浓硫酸能与灼热的木炭反应,生成二氧化碳、二氧化硫和水 |
您最近一年使用:0次
2024-03-05更新
|
543次组卷
|
6卷引用:新疆阿克苏市实验中学2022-2023学年高一下学期第三次月考化学试题
新疆阿克苏市实验中学2022-2023学年高一下学期第三次月考化学试题(已下线)5.2.3硝酸和酸雨的防治课后作业提高篇(已下线)专题02 氮及其化合物(考题猜想)(8大题型)-2023-2024学年高一化学下学期期中考点大串讲(人教版2019必修第二册)宁夏吴忠市青铜峡市宁朔中学2023-2024学年高一下学期3月月考化学试题5.2.3 硝酸、酸雨及防治 随堂练习黑龙江省哈尔滨市第六中学校2023-2024学年高一下学期4月测试化学试卷
5 . 下列表述正确的是
①浓硝酸通常保存在棕色试剂瓶中
②检验亚硫酸钠溶液在空气中放置是否变质可以通过先加稀硝酸,再加氯化钡溶液的方法
③锌与稀硝酸反应主要产物有氢气
④足量的铁与稀硝酸反应后溶液呈浅绿色,说明稀硝酸不能氧化Fe2+
⑤将浓硫酸滴到纸上,纸变黑,说明浓硫酸具有脱水性
⑥二氧化硫和二氧化氮都能形成酸雨,酸雨的pH≥7
①浓硝酸通常保存在棕色试剂瓶中
②检验亚硫酸钠溶液在空气中放置是否变质可以通过先加稀硝酸,再加氯化钡溶液的方法
③锌与稀硝酸反应主要产物有氢气
④足量的铁与稀硝酸反应后溶液呈浅绿色,说明稀硝酸不能氧化Fe2+
⑤将浓硫酸滴到纸上,纸变黑,说明浓硫酸具有脱水性
⑥二氧化硫和二氧化氮都能形成酸雨,酸雨的pH≥7
| A.①③④ | B.①②⑥ | C.①⑤ | D.①⑤⑥ |
您最近一年使用:0次
2024-03-05更新
|
578次组卷
|
4卷引用:新疆阿克苏市实验中学2022-2023学年高一下学期第二次月考化学试题
名校
解题方法
6 . 宇航员出舱时呼吸所需氧气主要来自太空服中的呼吸面具。下列反应均能产生氧气,其中最适宜用于呼吸面具中提供氧的反应是
| A.4HNO3=4NO2↑+O2↑+2H2O | B.2H2O2=2H2O+O2↑ |
| C.2CO2+2Na2O2=2Na2CO3+O2 | D.2KClO3=2KCl+3O2↑ |
您最近一年使用:0次
解题方法
7 . 下列有关实验操作和现象都正确的是
| 选项 | 实验操作 | 现象 |
| ① | 过量的Fe粉中加入稀HNO3,充分反应后,滴入KSCN溶液 | 溶液呈红色 |
| ② | 浓HNO3久置或光照 | 变黄色 |
| ③ | Al箔插入稀HNO3 | 无现象 |
| ④ | 用玻璃棒蘸取浓HNO3点到蓝色石蕊试纸上 | 试纸先变红色后褪色 |
| A.①② | B.①③ |
| C.②③ | D.②④ |
您最近一年使用:0次
8 . 从物质类别和元素化合价两个维度研究物质的性质及转化是重要的化学学习方法。以下是氮元素的“价 类”二维图的部分信息。请回答下列问题:
类”二维图的部分信息。请回答下列问题:
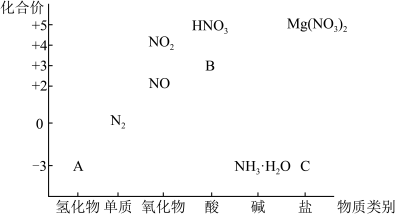
(1)亚硝酸(HNO2)在工业上用于有机合成,根据上述元素价态图写出其在上图中的字母标号为___________ 。
(2)工业上制备A的化学方程式为___________ ,检验C中含氮阳离子的方法是___________ 。
(3)2023年2月14日,美国亚利桑那州图森市外,公路上一辆商用罐车发生侧翻事故,导致危险物质液态硝酸泄露,事发地点很快升腾起恐怖的红棕色烟雾。产生这种烟雾的原因是:___________ (用化学方程式表示),汽车尾气中常含有氮氧化物,会污染空气。在汽车尾气排放管处安装一个催化转化器,可以使尾气中的有害气体CO和NO转化为两种无毒气体,该反应的化学方程式是:___________
(4)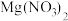 受热会分解,有同学猜想分解产物为
受热会分解,有同学猜想分解产物为 、
、 、
、 ,这种猜想不合理的理由是
,这种猜想不合理的理由是___________ 。
 类”二维图的部分信息。请回答下列问题:
类”二维图的部分信息。请回答下列问题:
(1)亚硝酸(HNO2)在工业上用于有机合成,根据上述元素价态图写出其在上图中的字母标号为
(2)工业上制备A的化学方程式为
(3)2023年2月14日,美国亚利桑那州图森市外,公路上一辆商用罐车发生侧翻事故,导致危险物质液态硝酸泄露,事发地点很快升腾起恐怖的红棕色烟雾。产生这种烟雾的原因是:
(4)
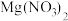 受热会分解,有同学猜想分解产物为
受热会分解,有同学猜想分解产物为 、
、 、
、 ,这种猜想不合理的理由是
,这种猜想不合理的理由是
您最近一年使用:0次
解题方法
9 . 通过对实验现象的观察、分析推理得出正确的结论是化学学习的方法之一、对下列实验事实的解释不正确 的是
| 选项 | 现象 | 解释或结论 |
| A | 铝片放入浓硫酸中,无明显变化 | 说明铝与冷的浓硫酸不发生化学反应 |
| B | SO2使酸性高锰酸钾溶液褪色 | SO2表现还原性 |
| C | 浓HNO3在光照条件下变黄 | 浓HNO3不稳定,生成有色产物能溶于浓硝酸 |
| D | 某溶液中加入NaOH溶液加热,放出气体能使湿润红色石蕊试纸变蓝 | 该溶液中一定含有NH |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
10 . 亚硝酸钠(NaNO2)可用作建筑钢材的缓蚀剂,也可用作食品添加剂,抑制微生物,保持肉制品的结构和营养价值,但是过量摄入会导致中毒。
I.某工厂以浓HNO3、SO2、Na2CO3溶液等为原料生产NaNO2,其流程如图:
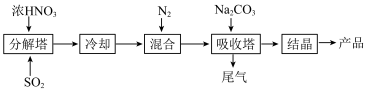
(1)在“分解塔”中,按一定比通入SO2和喷入浓HNO3,产生NO和NO2。操作时将SO2从塔底通入,浓HNO3从塔顶向下喷淋,这种加料操作的目的是_______ 。
(2)“分解塔”中的温度不宜过高,其主要原因是_______ 。
Ⅱ.某化学研究小组在实验室用稀HNO3、Cu、Na2O2为原料制备NaNO2,实验装置如图(夹持装置已省略)。
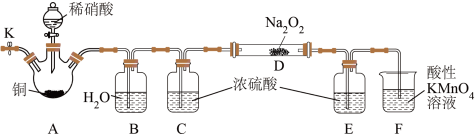
已知:①2NO+Na2O2=2NaNO2,2NO2+Na2O2=2NaNO3
②酸性条件下,NO、NO2或NO ,都能与MnO
,都能与MnO 反应生成NO
反应生成NO 和Mn2+
和Mn2+
(3)实验开始加入稀HNO3前,需要先打开止水夹K,向装置中通入一段时间N2,目的是_______ 。
(4)装置A中发生反应的离子方程式为_______ 。
(5)装置B、D不可省去,否则会导致产品中混有杂质_______ (填化学式)。
Ⅲ.NaNO2含量测定
工业亚硝酸钠产品中往往混有少量NaNO3等杂质,可以采用KMnO4测定含量。称取5.000g该亚硝酸钠产品溶于水配制成250mL的样品溶液。取25.00mL该样品溶液于锥形瓶中,用稀H2SO4酸化后,再向锥形瓶中滴加0.1000mol•L-1KMnO4溶液,至恰好完全反应时,消耗28.00mLKMnO4溶液。
(6)计算该产品中NaNO2的质量分数_______ 。(写出计算过程)
I.某工厂以浓HNO3、SO2、Na2CO3溶液等为原料生产NaNO2,其流程如图:

(1)在“分解塔”中,按一定比通入SO2和喷入浓HNO3,产生NO和NO2。操作时将SO2从塔底通入,浓HNO3从塔顶向下喷淋,这种加料操作的目的是
(2)“分解塔”中的温度不宜过高,其主要原因是
Ⅱ.某化学研究小组在实验室用稀HNO3、Cu、Na2O2为原料制备NaNO2,实验装置如图(夹持装置已省略)。

已知:①2NO+Na2O2=2NaNO2,2NO2+Na2O2=2NaNO3
②酸性条件下,NO、NO2或NO
 ,都能与MnO
,都能与MnO 反应生成NO
反应生成NO 和Mn2+
和Mn2+(3)实验开始加入稀HNO3前,需要先打开止水夹K,向装置中通入一段时间N2,目的是
(4)装置A中发生反应的离子方程式为
(5)装置B、D不可省去,否则会导致产品中混有杂质
Ⅲ.NaNO2含量测定
工业亚硝酸钠产品中往往混有少量NaNO3等杂质,可以采用KMnO4测定含量。称取5.000g该亚硝酸钠产品溶于水配制成250mL的样品溶液。取25.00mL该样品溶液于锥形瓶中,用稀H2SO4酸化后,再向锥形瓶中滴加0.1000mol•L-1KMnO4溶液,至恰好完全反应时,消耗28.00mLKMnO4溶液。
(6)计算该产品中NaNO2的质量分数
您最近一年使用:0次



