1 . 氮元素的单质和常见化合物在工、农业生产中用途广泛。(请用氮元素的单质或常见化合物化学式填空)
(1)化学性质很稳定,可用作灯泡填充气的是___________ 。
(2)汽车产生污染空气的尾气是___________ 。
(3)通常用___________ (填名称)干燥氨气。
(4)见光或受热会分解产生二氧化氮的强酸是___________ 。
(5)铵盐大多在农业上用作化肥,实验室用固体___________ 与固体Ca(OH)2加热反应可制取氨气。
(1)化学性质很稳定,可用作灯泡填充气的是
(2)汽车产生污染空气的尾气是
(3)通常用
(4)见光或受热会分解产生二氧化氮的强酸是
(5)铵盐大多在农业上用作化肥,实验室用固体
您最近一年使用:0次
2 . 硝酸被称为“国防工业之母”,是因为它是制取炸药的重要原料。氨氧化法制硝酸过程如图:

| A.浓硝酸和氯水用棕色试剂瓶保存,原理相同 |
B. 固体能溶于稀硝酸,生成 固体能溶于稀硝酸,生成 ,放出 ,放出 气体 气体 |
| C.将分别蘸有浓硝酸和浓氨水的玻璃棒相互靠近时,有白烟生成 |
D.转化④中,当 时,理论上 时,理论上 全部转化为 全部转化为 |
您最近一年使用:0次
3 . 下列关于元素及其化合物的性质说法不正确的是
| A.浓硫酸与蔗糖反应,观察到蔗糖变黑,体现了浓硫酸的吸水性 |
| B.硝酸见光受热易分解,一般保存在棕色试剂瓶中,放置在阴凉处 |
C.燃油发动机产生的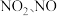 与 与 反应能生成 反应能生成 和 和 ,因此可直接排放 ,因此可直接排放 |
| D.铝制餐具不宜用来蒸煮或长时间存放酸性或者碱性食物 |
您最近一年使用:0次
名校
解题方法
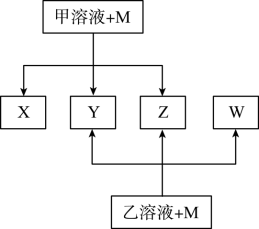
4 . 常温下,X是红棕色气体;Y能使澄清石灰水变浑浊但不能使品红溶液褪色。
②甲、乙是两种酸
③将甲的浓溶液露置在空气中一段时间,质量减小浓度降低;将乙的浓溶液露置在空气中一段时间,质量增加浓度降低。
请完成下列空白:
(1)M的化学式为___________
(2)甲的浓溶液需盛放在棕色试剂瓶中,其原因是___________ (用化学方程式表示)。
(3)在X与H2O的反应中,被氧化的X与被还原的X的物质的量之比是___________ 。
(4)欲除去Y中混有的W,下列试剂可供选用的是___________。
(5)写出M与乙的浓溶液在加热条件下反应的化学方程式:___________ 。
(6)工业上运输甲、乙两种浓溶液可选用___________ (金属名称)制运输罐,所选用的金属能做运输罐的理由是___________ 。
②甲、乙是两种酸
③将甲的浓溶液露置在空气中一段时间,质量减小浓度降低;将乙的浓溶液露置在空气中一段时间,质量增加浓度降低。
请完成下列空白:
(1)M的化学式为
(2)甲的浓溶液需盛放在棕色试剂瓶中,其原因是
(3)在X与H2O的反应中,被氧化的X与被还原的X的物质的量之比是
(4)欲除去Y中混有的W,下列试剂可供选用的是___________。
| A.品红溶液 | B.酸性高锰酸钾溶液 | C.氢氧化钠溶液 | D.饱和 溶液 溶液 |
(6)工业上运输甲、乙两种浓溶液可选用
您最近一年使用:0次
名校
5 . 利用图所示装置进行铜与硝酸反应的实验。 ___________ 。
(2)使用稀硝酸进行实验:反应开始后,铜丝逐渐变细,有气泡产生,溶液变蓝。
① 铜与稀硝酸反应的离子方程式为___________ 。
② 实验中观察到试管中的气体略有红棕色,其原因是___________ (用化学方程式表示)。
(3)使用浓硝酸进行实验:反应剧烈进行,铜丝逐渐变细,溶液变绿,试管上方出现红棕色气体。 铜与浓硝酸反应的化学方程式为___________ 。

(2)使用稀硝酸进行实验:反应开始后,铜丝逐渐变细,有气泡产生,溶液变蓝。
① 铜与稀硝酸反应的离子方程式为
② 实验中观察到试管中的气体略有红棕色,其原因是
(3)使用浓硝酸进行实验:反应剧烈进行,铜丝逐渐变细,溶液变绿,试管上方出现红棕色气体。 铜与浓硝酸反应的化学方程式为
您最近一年使用:0次
名校
解题方法
6 . 根据下列实验操作和现象所得到的结论不正确的是
选项 | 实验操作和现象 | 结论 |
| 将红热木炭加入浓硝酸中,产生红棕色气体 | 加热条件下,浓硝酸能氧化碳单质 |
| 乙烯通入溴的四氯化碳溶液后,溶液褪色 | 生成的1,2-二溴乙烷无色、可溶于四氯化碳 |
| 在 溶液中滴加 溶液中滴加 溶液,再加入苯,振荡,有白色沉淀生成,苯层呈紫色 溶液,再加入苯,振荡,有白色沉淀生成,苯层呈紫色 | 白色沉淀可能为 |
| 向某溶液中滴加盐酸酸化的 溶液,生成白色沉淀 溶液,生成白色沉淀 | 该溶液中不一定含有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
7 . 某学习小组探究稀HNO3、浓HNO3与铜的反应。
(1)试管I中Cu与稀HNO3反应的离子方程式是_______ 。
(2)II中反应的速率比I中的快,原因是_______ 。
(3)针对II中溶液呈绿色的原因,提出假设:
假设1:Cu2+的浓度较大所致;
假设2:溶解了生成的NO2。
探究如下:取II中绿色溶液,分为两等份。
①取一份加入如图所示装置中,_______ (填“操作”和“现象”),证实II中溶解了NO2。_______ (填化学试剂),溶液变为蓝色。证实假设1不成立,假设2成立。
(4)对于稀HNO3与铜生成NO、浓HNO3与铜生成NO2的原因,提出两种解释:
解释1:HNO3;浓度越稀,溶液中 的数目越少,被还原时,每个
的数目越少,被还原时,每个 从还原剂处获得较多电子的机会
从还原剂处获得较多电子的机会_______ (填“增多”或“减少”),因此被还原为更低价态。
解释2:浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO。
实验验证浓硝酸能将NO氧化成NO2,实验装置如下图:_______ 。
②C中盛放 和
和_______ 。
③该小组证实推测的合理性所依据的实验现象是_______ 。
装置(尾气处理装置略) | 现象 |
| I中开始无明显现象,渐有小气泡生成,越来越剧烈,液面上方出现浅红棕色气体,溶液呈蓝色。 |
| II中反应剧烈,迅速生成大量红棕色气体,溶液呈绿色。 |
(1)试管I中Cu与稀HNO3反应的离子方程式是
(2)II中反应的速率比I中的快,原因是
(3)针对II中溶液呈绿色的原因,提出假设:
假设1:Cu2+的浓度较大所致;
假设2:溶解了生成的NO2。
探究如下:取II中绿色溶液,分为两等份。
①取一份加入如图所示装置中,

(4)对于稀HNO3与铜生成NO、浓HNO3与铜生成NO2的原因,提出两种解释:
解释1:HNO3;浓度越稀,溶液中
 的数目越少,被还原时,每个
的数目越少,被还原时,每个 从还原剂处获得较多电子的机会
从还原剂处获得较多电子的机会解释2:浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO。
实验验证浓硝酸能将NO氧化成NO2,实验装置如下图:
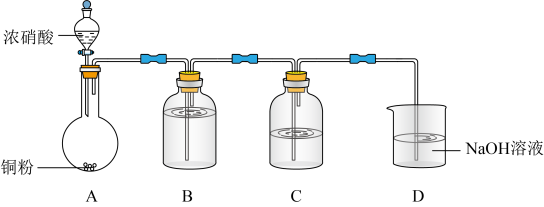
②C中盛放
 和
和③该小组证实推测的合理性所依据的实验现象是
您最近一年使用:0次
名校
解题方法
8 . 关于硝酸说法正确的是
| A.NO2溶于水生成硝酸,所以NO2是酸性氧化物 |
| B.冷的稀硝酸可以保存在铝、铁的容器中 |
| C.浓硝酸久置溶液会变黄是因为硝酸分解产生NO2 |
| D.硝酸与铜的反应中,硝酸只表现氧化性 |
您最近一年使用:0次
名校
9 . 氮元素在地球上含量丰富,是构成生命体的基本元素之一。回答下列问题:
(1)下列变化中,属于固氮的是_______ (填字母)。
A.豆科植物把空气中的氮气转化为化合态的氮
B.分离液态空气获得氮气
C.用NH4Cl和熟石灰制备氨气
D.NO2溶于水得到HNO3
E.土壤中的硝酸盐被细菌分解转化为氮气
(2)受到阳光照射浓硝酸会变黄的原因是_______ (用化学方程式表示)。
(3)近几年来关于氮污染的治理倍受关注,根据氮的性质回答以下问题:
①氮氧化物是空气的主要污染物,用碱液脱硝是目前研究的课题之一。将NO2通入氢氧化钠溶液中可得到NaNO3和NaNO2,写出其反应方程式:_______ 。
②向酸性工业废水中加入次氯酸钠溶液,可将其中的NH 完全转化为N2,而次氯酸钠被还原为NaCl。写出上述反应的离子方程式:
完全转化为N2,而次氯酸钠被还原为NaCl。写出上述反应的离子方程式:_______ 。
(4)潜艇中使用的液氨-液氧燃料电池工作原理如图所示:_______ (填“正极”或“负极”)。
②电极b的电极反应式为_______ 。
(1)下列变化中,属于固氮的是
A.豆科植物把空气中的氮气转化为化合态的氮
B.分离液态空气获得氮气
C.用NH4Cl和熟石灰制备氨气
D.NO2溶于水得到HNO3
E.土壤中的硝酸盐被细菌分解转化为氮气
(2)受到阳光照射浓硝酸会变黄的原因是
(3)近几年来关于氮污染的治理倍受关注,根据氮的性质回答以下问题:
①氮氧化物是空气的主要污染物,用碱液脱硝是目前研究的课题之一。将NO2通入氢氧化钠溶液中可得到NaNO3和NaNO2,写出其反应方程式:
②向酸性工业废水中加入次氯酸钠溶液,可将其中的NH
 完全转化为N2,而次氯酸钠被还原为NaCl。写出上述反应的离子方程式:
完全转化为N2,而次氯酸钠被还原为NaCl。写出上述反应的离子方程式:(4)潜艇中使用的液氨-液氧燃料电池工作原理如图所示:
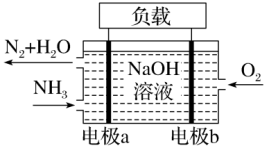
②电极b的电极反应式为
您最近一年使用:0次
10 . 下列关于氮及其化合物的性质和用途具有对应关系的是
| A.N2性质稳定,可用于合成NH3 | B.NO2的密度比空气的大,可用于制硝酸 |
| C.液氨汽化时吸收大量的热,可用于作制冷剂 | D.硝酸见光易分解,可用于制氮肥 |
您最近一年使用:0次